Современные возможности паклитаксела в лечении рака молочной железы
- Аннотация
- Статья
- Ссылки


Паклитаксел является одним из основных препаратов в терапии целого ряда злокачественных новообразований, в частности рака молочной железы, яичников, легких, эпителиальных опухолей головы и шеи, т.е. наиболее часто встречающихся нозологических форм.
Рак молочной железы – одна из первых локализаций, при которой паклитаксел проявил выраженную противоопухолевую активность сначала в монотерапии у многократно леченных ранее больных, в том числе резистентных к антрациклинам, а затем в первой линии химиотерапии, а также в комбинациях с другими цитостатиками. Как и следовало ожидать, наиболее эффективными оказались режимы с включением паклитаксела и антрациклинов, однако при высокой непосредственной эффективности в большинстве исследований не удалось существенно улучшить отдаленные результаты лечения. В связи с этим целесообразность использования подобных комбинаций в первой линии химиотерапии по-прежнему остается спорным вопросом. Очевидно, в первую очередь такие режимы должны назначаться больным с массивным опухолевым процессом и быстрым темпом прогрессирования болезни.
Итоги многочисленных работ, посвященных использованию паклитаксела в различных клинических ситуациях, подробно освещены в литературе предыдущих лет (1), поэтому в нашей статье мы сделаем акцент на новых аспектах использования препарата, а также подведем итоги некоторых крупных сравнительных исследований, результаты которых стали доступны в последнее время.
Следует отметить, что комбинации паклитаксела с другими цитостатиками относительно хорошо охарактеризованы, хотя исследования в этом направлении продолжаются. Перспективы же дальнейших исследований с участием паклитаксела видятся в изучении его комбинаций с таргетными препаратами и, соответственно, поиске оптимальных сочетаний такого рода, а также в осмыслении роли паклитаксела как одного из представителей группы таксанов в лечении раннего рака молочной железы.
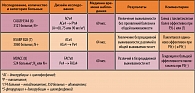
Что касается комбинаций с таргетными препаратами, то сегодня сравнительно хорошо изученными являются комбинации паклитаксела с трастузумабом, единственным пока препаратом этой группы, разрешенным к клиническому применению при раке молочной железы в России. Еще на этапе доклинического изучения было отмечено аддитивное взаимодействие паклитаксела и трастузумаба (2). В дальнейшем эти факты нашли подтверждение в соответствующих клинических исследованиях. Наиболее показательными являются данные рандомизированного исследования H0648g, в котором приняли участие 469 больных метастатическим раком молочной железы с гиперэкспрессией Her-2/neu (3). Все больные были рандомизированы на две группы: в первой проводилась стандартная химиотерапия (паклитаксел 175 мг/м2 1 раз в 3 нед. для больных, получавших антрациклины адъювантно, или стандартные режимы АС/ЕС для больных, не получавших ранее химиотерапии); во второй группе эти же режимы химиотерапии назначались в сочетании с трастузумабом в стандартной дозе 2 мг/кг еженедельно. Оказалось, что комбинация паклитаксела с трастузумабом обладает большей эффективностью как в отношении непосредственных, так и отдаленных результатов (таблица 1).
Комментируя это исследование, следует отметить, что антрациклинсодержащие комбинации были также более эффективными в комбинации с трастузумабом, однако, такого рода режимы не рекомендованы сегодня для использования в повседневной клинической практике по причине суммирования кардиотоксических эффектов, свойственных как трастузумабу, так и антрациклинам.
Высокоэффективными оказались еженедельные схемы введения паклитаксела в дозе 90 мг/м2 и трастузумаба в стандартной дозе. При продолжительности лечения 25 недель объективные противоопухолевые эффекты были получены у 67-81% больных с гиперэкспрессией Her-2/neu в зависимости от метода определения уровня экспрессии. В противоположность этому эффективность такого режима лечения у больных с нормальным уровнем экспрессии Her-2/neu составила всего 41-46% (4).
Чрезвычайно интересными представляются данные рандомизированного исследования III фазы Е2100, в котором проведено сравнение эффективности и токсичности монотерапии паклитакселом (90 мг/м2 1, 8 и 15 дни 1 раз в 4 нед.) с комбинацией паклитаксела и бевацизумаба (10 мг/кг 1 и 15 дни 1 раз в 4 нед.) в первой линии лечения. В исследовании приняли участие 722 больных распространенным раком молочной железы. Комбинированный режим позволил существенно улучшить показатели непосредственной эффективности (частота объективных эффектов 28,2% vs. 14,2%; р<0,0001) и отдаленные результаты лечения (время до прогрессирования 6,11 мес. vs. 10,97 мес.). Данные относительно общей выживаемости также свидетельствуют о преимуществе комбинированного режима, хотя и являются предварительными (5).
Таким образом, комбинированное применение паклитаксела с таргетными препаратами существенно расширяет возможности химиотерапии рака молочной железы.
Важное направление в изучении таксанов вообще и паклитаксела в частности связано с оценкой роли этих препаратов в лечении раннего рака молочной железы. Этот вопрос в настоящее время продолжает интенсивно изучаться. Достаточно сказать, что сегодня в литературе имеются сообщения как минимум о 19 исследованиях, посвященных раннему раку молочной железы, где в адъювантных режимах используются таксаны; общее количество участниц в этих исследованиях составляет 35500. Результаты 8 исследований имеют достаточный для анализа срок наблюдения. Остановимся подробнее на работах, в которых в режимах адъювантной терапии был использован паклитаксел (таблица 2).
В исследовании CALGB 9344, одном из наиболее влиятельных в истории медицинской онкологии, приняли участие 3121 больных с положительными подмышечными лимфоузлами. Целью работы было выяснить, повлияет ли увеличение дозы доксорубицина или добавление паклитаксела к стандартному режиму АС на отдаленные результаты лечения. При медиане времени наблюдения 69 мес. выявлено статистически значимое снижение риска рецидива (на 17%) и смерти (на 18%) в группе больных, получавших паклитаксел. При анализе результатов лечения в различных подгруппах больных существенное увеличение безрецидивной выживаемости отмечено только у пациенток с РЭ (-) опухолями. Доза доксорубицина не оказала существенного влияния на результаты лечения (6).
Проект NSABP B-28 с участием 3060 больных с метастазами в подмышечные лимфоузлы предполагал сравнение в качестве адъювантной терапии 4 курсов АС и сочетания 4 курсов АС с последующими 4 курсами паклитаксела. При медиане времени наблюдения 64 мес. в группе больных, получавших паклитаксел, выявлено статистически значимое снижение риска рецидива; существенного влияния на общую выживаемость не отмечено. Паклитаксел был одинаково эффективным независимо от рецепторного статуса опухоли (7).
В небольшом исследовании MD Andersen приняли участие 524 больных, которые получали либо 4 курса паклитаксела с последующими 4 курсами FAC, либо 8 курсов FAC. При медиане времени наблюдения 60 мес. статистически значимых различий в общей и безрецидивной выживаемости выявлено не было, хотя имелась тенденция к улучшению этих показателей в группе паклитаксела (8).
Данные исследований по адъювантной терапии с включением таксанов были проанализированы экспертами и отражены в очередном консенсусе по лечению раннего рака молочной железы, принятом в Сан Галлене в 2005 г. (9). Было отмечено, что имеющиеся данные пока не позволяют рекомендовать таксаны в качестве адъювантной терапии у больных с N(-). Что касается больных с N(+), то экспертами отмечено несовершенство дизайна ряда исследований, в частности обусловленное включением больных с различным рецепторным статусом, что могло исказить истинную картину эффективности химиотерапии. Поэтому значение таксанов, и в частности паклитаксела в адъювантной терапии рака молочной железы, по-прежнему требует уточнения. Между тем, выбор в пользу дополнения антрациклиновых режимов таксанами, в т.ч. паклитакселом, может быть сделан, во-первых, в подгруппе больных с повышенным риском рецидива (высокая экспрессия Her-2/neu, отрицательный рецепторный статус), а во-вторых, в тех клинических ситуациях, когда мы по каким-то причинам предполагаем наличие повышенного риска развития кардиотоксичности.
Высокая противоопухолевая активность паклитаксела, особенно в сочетании с антрациклинами, у больных диссеминированным раком молочной железы сделала обоснованной попытку применения его в режимах неоадъювантной химиотерапии. Как известно, при проведении такого варианта лечения в наибольшей степени выигрывают те больные, у которых в результате химиотерапии достигнута полная морфологическая регрессия опухоли. Возможности паклитаксела в неоадъювантной химиотерапии раннего рака молочной железы были оценены в соответствующих клинических исследованиях (таблица 3).
Впечатляющие результаты были получены группой итальянских ученых, использовавших у больных с T2-3N0-1 в качестве неоадъювантной химиотерапии комбинацию цисплатина 30 мг/м2, эпирубицина 50 мг/м2 и паклитаксела 120 мг/м2 еженедельно в течение 8 недель с поддержкой колониестимулирующими факторами. Объективные противоопухолевые эффекты были получены у 98% больных, в том числе у 50% – полные, при этом у 35% больных полная морфологическая регрессия опухоли была достигнута не только в молочной железе, но и в подмышечных лимфоузлах (!) (17).
Поистине сенсационными являются первые данные, полученные в небольшом исследовании с участием 42 больных с T1-4N0-2 и гиперэкспрессией Her-2/neu при использовании последовательно 4 курсов FEC и 4 курсов паклитаксела в сочетании с трастузумабом: сообщается о 66,7% полных морфологических регрессий (!) (18).
Результаты применения паклитаксела в неоадъювантной химиотерапии, безусловно, выразительны, но требуют дальнейшего подтверждения при долгосрочном наблюдении за больными. Однако подобные комбинации уже сейчас могут применяться на дооперационном этапе, особенно у больных с большими опухолями, а также другими факторами повышенного риска.
Стремление улучшить результаты лечения раннего рака молочной железы заставляет продолжать поиск новых эффективных стратегий и в адъювантной терапии, особенно в группе больных с неблагоприятным прогнозом. Эффективность адъювантной химиотерапии с включением наиболее эффективных препаратов (антрациклинов, паклитаксела, трастузумаба) интенсивно изучается сегодня в соответствующих рандомизированных исследованиях. Предварительные данные двух из них - NCCTG №9831, NSABP B-31 – уже опубликованы.
Дизайн этих исследований был схожим и предполагал проведение 4 курсов химиотерапии по схеме АС, после которых проводились 4 курса паклитаксела в сочетании или без трастузумаба, который назначался на срок
1 год. Абсолютный выигрыш при использовании трехкомпонентного варианта лечения (АС + паклитаксел + трастузумаб) в течение 3 и 4 лет составил соответственно для безрецидивной выживаемости 12% и 18%, для отдаленного метастазирования – 9% и 16%, для общей выживаемости – 2,5% и 4,8%. Следует отметить, что 19% больных прекратили лечение трастузумабом в связи с кардиотоксичностью (19).
Кроме того, протоколом исследования NSABP B-31 было предусмотрено сравнение одновременного и последовательного c паклитакселом назначения трастузумаба. Оказалось, что одновременное с паклитакселом назначение трастузумаба улучшило безрецидивную выживаемость на 36% (р=0,014) по сравнению с последовательным (20).
Таким образом, паклитаксел является сегодня неотъемлемой составной частью лечебных программ при диссеминированном и раннем раке молочной железы, ощутимо влияя на эффективность терапии. Интенсивное развитие фармакотерапии рака молочной железы и появление принципиально новых классов противоопухолевых средств открывает дополнительные перспективы использования препарата, требующие его изучения в новых условиях применения. Основной тенденцией современности в лечении опухолей и в частности рака молочной железы является индивидуальный подбор лечебной тактики, основывающийся на детальной характеристике опухоли на генном уровне. Такой подход, возможно, позволит более четко обозначить круг больных, которым показано назначение таксанов, в том числе паклитаксела, что должно сделать терапию более эффективной.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.