Возможности современных метаболических препаратов
- Аннотация
- Статья
- Ссылки


При этом следует отметить масштабность палитры показаний к применению этой группы лекарств: острые и хронические нарушения мозгового кровообращения, нейропатии (в т.ч. диабетическая автономная нейропатия и диабетическая дистальная полинейропатия), хронический болевой синдром, метаболическая энцефалопатия, пред- и постинтервенционное ведение тромболитических процедур и т.д.
С позиций медицины, основанной на доказательствах, сегодня ни один препарат, претендующий на фармакологическую метаболическую, в частности, нейропротективную активность, за исключением цитиколина, не продемонстрировал своих преимуществ в широкомасштабных плацебо-контролируемых исследованиях. Однако это не может явиться поводом к отказу от назначения подобных средств в связи, как минимум, с многолетним отечественным опытом применения этих лекарственных препаратов (например, Актовегина) и большого числа российских и зарубежных открытых сравнительных проспективных исследований, демонстрирующих большую выживаемость, лучший уровень восстановления неврологического дефицита, снижение инвалидизации в группах пациентов, которым назначались метаболические средства. Другим аргументом является наличие коморбидных состояний российского пациента, где назначение метаболической терапии играет важную роль в компенсации сопутствующей патологии.
При этом в большой группе метаболических препаратов, в частности, нейрометаболических средств, существуют принципиальные различия в фармакологическом действии. Для понимания различий фармакологического действия необходимо представлять биохимические нарушения метаболизма клеток, в частности, нейронов, приводящие к их гибели.
В целом для адекватного физиологического функционирования любой клетки, в том числе нейронов, принципиальным является адекватный энергетический статус, т.е. синтез 38 молекул АТФ.
Это возможно при наличии следующих условий.
- Адекватное поступление глюкозы в клетку.
- Адекватная утилизация кислорода клеткой.
- Низкий уровень активности свободных радикалов, образующихся в процессе окисления глюкозы. В норме высокая активность супероксиддисмутазы инактивирует свободные радикалы.
- Адекватное соотношение фосфолипидов мембраны для активности мембраны клетки и митохондрий.
При ишемии клетки различных органов и тканей, в частности, нейронов в надежде на восстановление нормального кровотока начинают приспосабливаться к условиям ишемии, в первую очередь, перестраиваясь на анаэробное окисление глюкозы. Однако резервные возможности, исчерпав себя, приводят к апоптозу клетки.
Перестройка метаболизма клетки для анаэробного окисления глюкозы в общих чертах заключается в следующем:
- системный синтез антиинсулиновых антител, блокирующих рецепторы к инсулину на мембране (физиологический смысл – уменьшить потребление глюкозы в условиях ишемии);
- снижение числа и активности переносчиков глюкозы на мембране;
- снижение активности пируватдегидрогеназы и замедление цикла Кребса (физиологический смысл – снизить потребление кислорода в условиях ишемии);
- снижается активность супероксиддисмутазы, соответственно, увеличивается число свободных радикалов, повреждающих мембрану (физиологический смысл – «убить» больше клеток для снижения потребности в кислороде и глюкозе);
- снижение синтеза фосфолипидов клеточной мембраны и нарушение ее транспортных и физиологических функций;
- избыточное накопление возбуждающих аминокислот.
В соответствии с описанными патологическими изменениями формируется список требований к препаратам, претендующим на метаболическую, в частности, нейропротективную активность. В идеале лекарственный препарат должен обладать фармакологической активностью в отношении всех патологических изменений в метаболизме клетки при ишемии. Однако ни один из препаратов не отвечает полному списку требований.
В целом фармакологическая активность наиболее часто использующихся метаболических препаратов представлена в таблице 1.
Особо стоит остановиться на инсулиноподобном действии препаратов этой группы. Подчеркнем, что нарушение транспорта и утилизации глюкозы является ведущим патогенетическим механизмом апоптоза клетки. Подобным фармакологическим эффектом обладает лишь препарат Актовегин.
Активная фракция препарата оказывает инсулиноподобное действие. Об отличном от инсулина действии Актовегина свидетельствует то, что антитела к инсулину не блокируют этот эффект и не нарушают транспорт глюкозы, который под влиянием Актовегина усиливается в 5, а не в 10 раз, как под воздействием инсулина (1, 2). Показано, что инсулиноподобное действие оказывают выделенные из Актовегина инозитолфосфат-олигосахариды (ИФО), активирующие переносчики глюкозы в плазматической мембране. К настоящему времени обнаружены 5 носителей глюкозы (GLUT 1-5).
Инсулиноподобное действие Актовегина было подтверждено и в клинических исследованиях. Так, в рандомизированное двойное слепое исследование, проведенное Heidrich и соавт. (1979), было включено 20 пациентов с сахарным диабетом и 20 лиц с нормальным метаболизмом углеводов (3). Исследовалось влияние на гликемию и сывороточный инсулин 14-дневного курса терапии Актовегином (0,5 мл/кг/день в/в), в качестве плацебо использовали эквивалентное количество физиологического раствора. У больных сахарным диабетом Актовегин значительно улучшал толерантность к глюкозе, не влияя на концентрацию сывороточного инсулина, при нормальном метаболизме углеводов содержание сахара крови и инсулина сыворотки под воздействием Актовегина не изменилось.
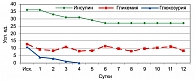
По данным В.Н. Оболенского и соавторов (2002) (4), у 21 пациента с диабетической стопой, которым проводилось внутривенное введение 1000 мг Актовегина, было отмечено снижение среднесуточного уровня гликемии с первых суток применения препарата, повлекшее за собой уменьшение суточной потребности в инсулине, а также купирование глюкозурии на третьи сутки (рисунок 1).
Одним из самых универсальных механизмов жизнедеятельности клетки и процессов, реализующихся в межклеточном пространстве, является образование свободных радикалов – неотъемлемых спутников окислительных реакций, обладающих мощной химической и биологической активностью.
Свободнорадикальное окисление следует рассматривать как необходимое метаболическое звено в окислительном фосфорилировании, биосинтезе простагландинов и нуклеиновых кислот, иммунных реакциях и т. д. В частности, свободные радикалы образуются в процессе перекисного окисления жирных кислот с изменением при этом физических свойств биологических мембран. Свободнорадикальное окисление является универсальным патофизиологическим феноменом при многих патологических состояниях, а также обязательной и существенной составляющей механизмов возрастных изменений организма и повреждающего действия хронического стресса.
Типичным явлением для всех перечисленных процессов является тканевой дефицит кислорода. При этом в условиях нарушений энергообразующих реакций и неполного восстановления кислорода происходит образование высокореактивных и потому токсичных свободных радикалов или продуктов, которые их генерируют. Патологическое воздействие свободных радикалов связано с их влиянием на структурно-функциональные характеристики биологических мембран, что приводит к нарушениям их естественной транспортно-защитной функции, повышению микровязкости, изменению проницаемости для различных ионов, а следовательно, изменениям в жизнедеятельности клетки и в дальнейшем – ее деструкции и гибели.
Особо опасны свободные радикалы для митохондрий, в частности, митохондриальной ДНК (мтДНК). Поскольку митохондрии используют 85-99% всего кислорода, потребляемого клетками (5), самые большие количества супероксидрадикала образуются именно в них. В результате отмечается окислительное повреждение молекулы мтДНК и, соответственно, повышение вероятности развития мутаций (6).
Исключительно важны упомянутые процессы для головного мозга, принимая во внимание последствия повреждения ДНК в постмитотических клетках, каковыми являются нейроны (7).
Повышенная продукция свободных радикалов – одна из существенных причин длительного спазма церебральных сосудов, прогрессирования постишемического отека и дегенерации нейронов вследствие нарушения целостности мембран.
В последнее время оксидативный стресс рассматривается как один из ведущих факторов патогенеза поражения головного мозга при сосудистых, метаболических и дегенеративных заболеваниях.
Именно антиоксидантная фармакотерапия является одним из оптимальных направлений развития стратегии нейропротекции, поскольку позволяет обеспечить защиту нейронов от действия универсальных повреждающих факторов, лежащих в основе большинства клинических форм патологии ЦНС.
По механизму действия все препараты с антиоксидантными и антигипоксантными свойствами делятся на первичные, препятствующие образованию новых свободных радикалов (это преимущественно средства ферментной природы), и вторичные, способные захватывать уже образовавшиеся радикалы, то есть работающие по принципу «ловушки» (scavengers). В настоящее время, несмотря на свою перспективность, прямые антиоксиданты редко используются в клинической практике вследствие быстрой инактивации ферментов, большого молекулярного веса и неспособности проникать через гематоэнцефалический барьер, высокого риска развития побочных эффектов.
В связи с этим наиболее широкое применение в практической медицине нашли антиоксиданты с непрямым механизмом действия. Единой классификации непрямых антиоксидантов в настоящее время не существует. В настоящее время в клинической практике применяются витамин Е (Токоферол) и его синтетические аналоги (азотокоферол и др.), ароматические фенолы и полифенолы (Ионол, Пробукол, Дибунол), пептидные препараты (Карнозин), органические кислоты и их производные (аскорбиновая, тиопропионовая, ретиноевая, липоевая и др. кислоты), коэнзим Q (Убихинон), b-каротин, производные 3-оксипиридина (Эмоксипин, Мексидол), производные мочевины (Мебикар), фитопрепараты (препараты гинкго) и т. д.
Детальная характеристика фармакологического действия метаболических препаратов, в частности, нейропротекторов в отношении свободнорадикального окисления является особо важной. В литературе представлена активность в отношении супероксиддисмутазы лишь небольшого числа препаратов.
Как видно из таблицы, Актовегин обладает самым мощным стимулирующим эффектом в отношении активности супероксиддисмутазы.
Резюмируя приведенные данные, необходимо отметить, что наиболее адекватным действием в отношении комплекса метаболических нарушений в клетках разных органов и тканей, в том числе нейронов, обладает Актовегин, который непосредственно влияет на энергетическое обеспечение клеток в условиях гипоксии, оказывая, помимо этого, антиоксидантное действие.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.