Взаимосвязь состояния сердечно-сосудистой системы и заболеваний щитовидной железы. Научно-практическая конференция «Кардиологические „маски“ соматических заболеваний». Сателлитный симпозиум компании «Берлин-Хеми/А. Менарини»
- Аннотация
- Статья
- Ссылки


Влияние гормонов щитовидной железы на функцию сердечно-сосудистой системы в норме и патологии
Физиологические эффекты тиреоидных гормонов в организме человека многообразны: регуляция роста и развития всех видов обменных процессов (энергетического, белкового, углеводного, жирового), влияние на психику, костно-мышечную, репродуктивную и, конечно, сердечно-сосудистую системы.
Связь состояния сердечно-сосудистой системы и заболеваний щитовидной железы известна давно. Еще в начале XX в. H. Zondek предложил термины «микседематозное сердце» и «тиреотоксическое сердце». Эти термины используются и в настоящее время для обозначения поражений миокарда при гипотиреозе и манифестном тиреотоксикозе.
Механизмы влияния тиреоидных гормонов на сердечно-сосудистую систему хорошо изучены. Тиреоидные гормоны оказывают действие:
- на уровне генома;
- негеномное (прямое) – на мембраны, саркоплазматический ретикулум и митохондрии;
- на периферическую циркуляцию (сосудорасширяющее действие, изменение пред- и постнагрузки, влияющих на сердечный выброс).
Таким образом, изменение функциональной активности щитовидной железы (тиреотоксикоз или гипотиреоз) приводит к изменению деятельности сердечно-сосудистой системы, в том числе таких параметров, как системное сосудистое сопротивление, сердечный выброс, частота сердечных сокращений, объем циркулирующей крови и др.
Гипотиреоз обусловлен уменьшением продукции тиреоидных гормонов щитовидной железой. Докладчик подчеркнула, что, несмотря на простоту и доступность диагностики гипотиреоза, очень часто в клинической практике данный диагноз ставится несвоевременно из-за доминирования симптомов заболевания другой системы организма. В такой ситуации говорят о клинической «маске» гипотиреоза.
Так, у первичного гипотиреоза можно выделить несколько «масок»: терапевтические (полиартрит, полисерозит, миокардит, ишемическая болезнь сердца (ИБС), артериальная гипертензия, нейроциркуляторная дистония, артериальная гипотензия, пиелонефрит, гепатит, гипокинезия желчевыводящих путей и кишечника), гематологические (гипохромная, нормохромная, пернициозная и фолиеводефицитная анемии), хирургические (желчнокаменная болезнь), гинекологические (бесплодие, поликистоз яичников, миома матки, менометроррагии, опсоменория, аменорея, галакторея-аменорея, гирсутизм), эндокринологические (акромегалия, ожирение, пролактинома, преждевременный псевдопубертат, задержка полового развития), неврологические (миопатия), дерматологические (алопеция) и психиатрические (депрессия, микседематозный делирий, гиперсомния, агрипния). Типичной кардиологической «маской» субклинического гипотиреоза являются стойкая гиперхолестеринемия, атерогенная дислипидемия, прогрессирующий атеросклероз, ИБС, аритмия, цереброваскулярная болезнь, артериальная гипертензия, пролапс митрального клапана, гидроперикард.
Причиной позднего диагностирования гипотиреоза у пациентов пожилого возраста является схожесть симптомов заболевания и признаков физиологической старости: утомляемость, зябкость, сухость кожи, снижение аппетита, снижение когнитивных функций, нарушение слуха, сердечная недостаточность.
Дефицитом тиреоидных гормонов обусловлено развитие такого серьезного заболевания, как гипотиреоидная кардиомиопатия. Данное заболевание связано с нарушением обменных процессов. При этом поражается как сократительный миокард, так и строма. В сердце происходят дистрофические изменения, сопровождающиеся снижением интенсивности окислительного фосфорилирования, замедлением синтеза белка, уменьшением поглощения кислорода миокардом и электролитными сдвигами. В кардиомиоцитах откладывается креатинфосфат, и возникает псевдогипертрофия миокарда. В сердце, как и в других тканях, депонируются кислые глюкозаминогликаны, вызывающие отек миокарда и стромы.
Изменения сердечно-сосудистой системы при гипотиреозе проявляются в виде одышки, особенно во время нагрузки, повышенной утомляемости, снижения толерантности к физическим нагрузкам, преимущественно диастолической артериальной гипертензии, брадикардии, экссудативного перикардита (часто с плевритом), сердечной недостаточности, прогрессирования атеросклероза, ИБС.
Синусовая брадикардия является характерным, но не абсолютным клиническим признаком гипотиреоза. Тахисистолическая форма фибрилляции и трепетания предсердий проявляется, как правило, в виде пароксизмов. Чередование пароксизмов фибрилляции/трепетания предсердий с брадикардией часто ошибочно принимают за синдром слабости синусового узла при ИБС. Клиническим признаком гипотиреоза может быть и политопная экстрасистолия.
Изменение липидного обмена у пациентов с субклиническим гипотиреозом приводит к накоплению в крови атерогенных фракций липопротеинов, а именно липопротеинов низкой плотности (ЛПНП), при снижении уровня липопротеинов высокой плотности (ЛПВП). Это является доказанным фактором риска развития атеросклероза и ИБС, особенно при наличии умеренного ожирения, артериальной гипертензии.
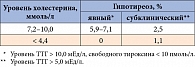
Торможение распада ЛПНП, снижение экскреции холестерина и желчных кислот с желчью, уменьшение активности липопротеиновой липазы – механизмы возникновения гиперлипидемии. Результаты исследований показывают взаимосвязь гипотиреоза и уровня холестерина в крови (табл. 1).
Поэтому гиперхолестеринемия может свидетельствовать о наличии у пациента гипотиреоза и должна быть основанием для оценки функции щитовидной железы.
Взаимосвязь функционального состояния щитовидной железы с риском развития атеросклероза подтвердили результаты исследования A.E. Hak и соавт. Было показано, что у пациенток с субклиническим гипотиреозом чаще наблюдаются атеросклероз аорты и инфаркты миокарда. Авторы сделали вывод, что субклинический гипотиреоз – существенный фактор риска развития инфаркта миокарда и атеросклероза аорты. Так, при гипотиреозе скорректированная по возрасту распространенность инфаркта миокарда возрастает в 2,3 раза (доверительный интервал (ДИ) 1,3–4,0)1.
Помимо изменений липидного обмена при субклиническом гипотиреозе снижается уровень эндотелиальных факторов вазодилатации, что в свою очередь является маркером раннего атеросклероза, нарушается диастолическая функция левого желудочка, увеличивается периферическое сопротивление и ригидность стенок сосудов, уменьшается толерантность к физической нагрузке.
При эхокардиографии у пациентов с субклиническим гипотиреозом может обнаружиться пролапс митрального клапана, который иногда сочетается с пролапсом трикуспидального и/или аортального клапанов, а также гидроперикард, протекающий бессимптомно. Эти изменения являются одними из первых выявляемых при обследовании признаков гипотиреоза, особенно у пожилых пациентов.
Профессор Н.А. Петунина отметила, что вопрос о терапии гипотиреоза по-прежнему остается дискутабельным. При субклиническом гипотиреозе решение о назначении заместительной терапии принимается индивидуально. Целью лечения гипотиреоза является нормализация уровня тиреотропного гормона (ТТГ). Это, как правило, достигается назначением левотироксина в дозе 1 мкг на 1 кг массы тела в сутки (50–75 мкг). По данным исследований, на фоне заместительной терапии отмечается коррекция метаболических сдвигов в организме (снижается уровень общего холестерина и ЛПНП), улучшаются когнитивные функции, сократительная функция миокарда, уменьшается тревожность, снижается внутриглазное давление. Следует отметить, что лечение не влияет на минеральную плотность костной ткани. Назначение заместительной терапии при субклиническом гипотиреозе может быть показано пожилым пациентам. При этом подбирается минимально эффективная доза. Особую осторожность следует проявлять у больных с сопутствующими заболеваниями и у лиц старше 65 лет, у которых может быть не диагностировано заболевание сердечно-сосудистой системы.
В то же время манифестный гипотиреоз – абсолютное показание для терапии тиреоидными гормонами. Противопоказаниями для применения левотироксина при манифестном гипотиреозе являются острый инфаркт миокарда, нестабильная стенокардия, острая фаза миокардита, пароксизм мерцательной аритмии, декомпенсированная надпочечниковая недостаточность.
В ряде работ показано, что левотироксин оказывает положительное влияние на сердечно-сосудистую систему. На фоне заместительной терапии улучшаются систолическая и диастолическая функции, эндотелиальная функция, снижается периферическая резистентность, повышается эластичность сосудов, нормализуется диастолическое артериальное давление2.
У пожилых пациентов ИБС и гипотиреоз часто сосуществуют. Это обусловлено тем, что характерные для гипотиреоза повышение уровня ЛПНП, снижение уровня ЛПВП и повышение артериального давления являются независимыми факторами риска сердечно-сосудистых заболеваний. При появлении симптомов стенокардии после начала лечения левотироксином или усилении симптомов предшествующей стенокардии показаны снижение дозы или отмена препарата, оценка коронарного кровотока, а также оптимизация лечения фонового заболевания миокарда. В противном случае повышается риск прогрессирования ишемии миокарда, инфаркта миокарда, аритмии, внезапной смерти.
Следующий синдром нарушения функциональной активности щитовидной железы – тиреотоксикоз. К сердечно-сосудистым изменениям, сопровождающим тиреотоксикоз, относятся систолическая артериальная гипертензия, суправентрикулярная аритмия, фибрилляция предсердий, сердечная недостаточность, увеличение массы левого желудочка и нарушение диастолического наполнения, снижение толерантности к физическим нагрузкам.
Наиболее частая причина развития тиреотоксикоза – болезнь Грейвса, которая является системным аутоиммунным заболеванием. У пациентов с болезнью Грейвса тиреотоксикоз обычно сопровождается аутоиммунным поражением сердечно-сосудистой системы, легочной гипертензией, миксоматозной дегенерацией створок клапанов сердца и обратимой или необратимой аутоиммунной кардиомиопатией.
Диагностика заболевания у лиц пожилого возраста затруднена в связи со стертой клинической картиной. Единственным проявлением тиреотоксикоза может быть фибрилляция предсердий (постоянная или пароксизмальная). Поэтому наличие у пациента фибрилляции предсердий является основанием для обследования больного на наличие тиреотоксикоза.
Для тиреотоксической тахикардии характерно укорочение диастолы. Из-за этого развивается кислородная недостаточность миокарда, повышается общий расход энергии в единицу времени. Увеличивается риск возникновения эктопических импульсов, что ведет к нарушению сердечного ритма и с течением времени развитию сердечно-сосудистой недостаточности. Сердечная недостаточность при тиреотоксикозе развивается прежде всего по правожелудочковому типу.
При некомпенсированном тиреотоксикозе могут поражаться органы-мишени, такие как головной мозг, костная ткань и сердце. У пациентов с некомпенсированным тиреотоксикозом снижается плотность костей. Наличие даже субклинического тиреотоксикоза увеличивает в три – пять раз риск возникновения фибрилляции предсердий.
На фоне некомпенсированного тиреотоксикоза наблюдается ускоренный кровоток и повышенный сердечный индекс вне зависимости от получаемой терапии. Увеличение размеров сердца отмечается только при появлении фибрилляции предсердий. Оно обусловлено дилатацией желудочков. Фибрилляция предсердий развивается чаще у больных пожилого возраста.
Существует три способа лечения тиреотоксикоза: консервативный, радиоактивным йодом и хирургический. Для достижения эутиреоидного состояния при консервативной терапии используют тиреостатики, в частности тиамазол (препарат Тирозол). Лечение кардиальных проявлений тиреотоксикоза проводится по показаниям. При частотно-зависимой сердечной недостаточности и для регуляции частоты сердечных сокращений при фибрилляции предсердий пациентам показан прием бета-адреноблокаторов, диуретиков, сердечных гликозидов (дигоксин в дозах, превышающих обычные поддерживающие и насыщающие дозы), антикоагулянтов, особенно пациентам пожилого возраста. У пациентов молодого возраста терапия тиреотоксикоза способствует нормализации сердечного ритма.
При использовании препаратов, содержащих фармакологические дозы йода, необходимо контролировать функциональное состояние щитовидной железы, поскольку наличие латентных нарушений функции щитовидной железы может спровоцировать манифестацию гипотиреоза или развитие йодиндуцированного тиреотоксикоза.
В амиодароне, рентгеноконтрастных средствах, некоторых антисептиках содержатся высокие дозы йода, влияющие на функциональную активность щитовидной железы. Однако результаты исследований показали, что пациенты без фоновых заболеваний щитовидной железы сохраняют эутиреоидное состояние даже при воздействии высоких доз экзогенного йода.
Докладчик обратила внимание аудитории на то, что вследствие длительного применения фармакологических доз йода могут развиться йодиндуцированный тиреоидит, йодиндуцированный тиреотоксикоз, йодиндуцированный зоб, йодиндуцированный гипотиреоз. Пациенты с существующими или ранее перенесенными заболеваниями щитовидной железы и ее нормальной функцией особенно предрасположены к развитию йодиндуцированного гипотиреоза.
В заключение профессор Н.А. Петунина подчеркнула, что задачами клиницистов на современном этапе являются своевременная диагностика, выбор адекватной терапевтической стратегии, улучшение качества и продолжительности жизни пациентов с нарушениями функции щитовидной железы.
Лечить или не лечить субклинические нарушения функции щитовидной железы с позиций сердечно-сосудистого риска
Л.В. Трухина отметила, что ТТГ рассматривается как наиболее значимый и чувствительный маркер изменений функциональной активности щитовидной железы. Так, при субклиническом гипотиреозе уровень ТТГ в сыворотке крови повышается при нормальных значениях свободного тироксина. Однако не всегда повышение уровня ТТГ является маркером патологического состояния. Так, проведено исследование этнической подгруппы евреев-ашкенази. В исследовании участвовали долгожители (средняя продолжительность жизни 97 лет) и их потомки (средний возраст 69 лет). Контрольная группа состояла из лиц со средней продолжительностью жизни. Результаты показали, что евреи-ашкенази и их потомки имеют более высокий уровень ТТГ.
К развитию субклинического гипотиреоза могут привести такие патологические состояния, как деструктивные тиреоидиты (послеродовой, подострый, безболевой), хронический аутоиммунный тиреоидит. Субклинический гипотиреоз может развиться в результате субтотальной резекции щитовидной железы (тиреоидэктомии), облучения головы или шеи, лечения радиоактивным йодом, приема ряда лекарственных препаратов (амиодарона, интерферонов, противовирусных препаратов).
По данным многочисленных исследований, распространенность в популяции субклинического гипотиреоза составляет 2–20%, причем она особенно высока среди женщин пожилого возраста.
При этом результаты большинства метаанализов показали повышение риска смерти и сердечно-сосудистых событий у больных субклиническим гипотиреозом. Так, в метаанализе результатов 15 клинических исследований была продемонстрирована более высокая вероятность развития ишемической болезни сердца и смерти от нее на фоне субклинического гипотиреоза у пациентов моложе 65 лет по сравнению с эутиреоидной популяцией3.
Результаты метаанализа данных 11 клинических исследований показали, что смерть от сердечно-сосудистых осложнений ассоциирована с субклиническим гипотиреозом, при этом достоверной взаимосвязь становится при уровне ТТГ > 7 мЕд/л. Отмечено, что у лиц старше 80 лет связь субклинического гипотиреоза и сердечно-сосудистых событий не прослеживается4.
Один из последних метаанализов включал шесть исследований, которые были проведены в Европе и США. Данные показали, что риск возникновения сердечной недостаточности у пациентов возрастал при высоких (> 10 мЕд/л) и низких (< 0,10 мЕд/л) значениях ТТГ5.
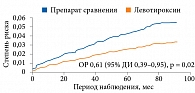
C 2001 по 2008 г. в Великобритании было проведено масштабное исследование по изучению влияния терапии левотироксином на развитие новых случаев ИБС, повышение риска сосудистой и общей смертности в течение периода наблюдения. Анализировали данные 10 млн историй болезни, лабораторных анализов, назначений и справок о смерти. Было выявлено 4735 пациентов старше 40 лет с ТТГ от 5,0 до 10,0 мЕд/л и нормальным уровнем свободного тироксина. Пациенты были рандомизированы на две группы: в первую вошли 3093 пациента в возрасте 40–70 лет, во вторую – 1642 пациента старше 70 лет. Из исследования исключались лица, которые ранее получали левотироксин, тиреостатические препараты, с заболеваниями щитовидной железы в анамнезе, ИБС, инсультами и другими сердечно-сосудистыми заболеваниями. В каждой группе пациентов было две подгруппы, одна из которых принимала левотироксин (52,9 и 49,9% соответственно). Результаты исследования продемонстрировали, что терапия левотироксином сопровождалась снижением риска смерти и сердечно-сосудистых событий у пациентов моложе 70 лет (рисунок).
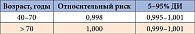
Не выявлена связь лечения левотироксином и увеличения относительного риска фибрилляции предсердий6 (табл. 2).
Докладчик отметила, что вопрос лечить или не лечить пациентов с субклиническим гипотиреозом остается открытым. Рекомендации Европейской тиреоидологической ассоциации, опубликованные в 2013 г., содержат алгоритм лечения субклинического гипотиреоза.
Эксперты советуют делить больных по возрастной категории. Если пациентам моложе 70 лет с уровнем ТТГ >10 мЕд/л назначают левотироксин, то пациентам старше 70 лет лечение левотироксином показано при наличии клинических симптомов гипотиреоза и высоком сердечно-сосудистом риске. Больным старше 70 лет с уровнем ТТГ < 10 мЕд/л рекомендовано наблюдение и повторное обследование через шесть месяцев. Если пациент моложе 70 лет, но выявлены симптомы субклинического гипотиреоза, возможно назначение заместительной терапии на три месяца. В случае положительной динамики терапию необходимо продолжить. Если симптомы заболевания отсутствуют, пациентам показано наблюдение и повторное обследование через шесть месяцев7.
Одним из вариантов заместительной терапии является препарат левотироксина – L-Тироксин Берлин-Хеми. Препарат отличается высокой эффективностью и выпускается в разных дозировках (50/75/100/125/150 мкг), что позволяет пациентам выбрать необходимую. Левотироксин, произведенный компанией «Берлин-Хеми», не содержит лактозы. Доказано, что безлактозные препараты левотироксина отличаются лучшей устойчивостью к воздействию факторов внешней среды: в препаратах, в состав которых в качестве вспомогательного вещества входит лактоза, в течение шести месяцев активность действующего вещества снижается на 30%, в безлактозных препаратах – на 15%8.
Другой вариант терапии – прием комбинированного препарата Йодокомб®, также произведенного компанией «Берлин-Хеми». Он показан для лечения диффузного эутиреоидного зоба и послеоперационной профилактики узлового зоба после резекции щитовидной железы. Препарат может применяться во время беременности и в период лактации. В состав препарата Йодокомб® входит левотироксин (50/75 мкг) и калия йодид (150 мкг). Препарат удобен для применения: суточную дозу следует принимать утром за 30 минут до еды.
Л.В. Трухина подробно рассмотрела причины возникновения и методы терапии субклинического тиреотоксикоза. Субклинический тиреотоксикоз – это тиреотоксикоз, при котором клинические симптомы могут отсутствовать, а в сыворотке крови определяется пониженный уровень ТТГ при нормальных показателях тиреоидных гормонов. Наиболее частыми причинами тиреотоксикоза являются болезнь Грейвса, функциональная автономия/узловой и многоузловой токсический зоб, деструктивные тиреоидиты.
Одна из наиболее частых причин экзогенного субклинического тиреотоксикоза – прием ТТГ-супрессивных доз левотироксина, например, у пациентов, оперированных по поводу рака щитовидной железы. По мнению некоторых исследователей, снижение уровня ТТГ может быть обусловлено старением. Так, в некоторых исследованиях было отмечено возрастное снижение уровня ТТГ у здоровых добровольцев.
В 2010 г. зарубежные авторы предложили выделить две степени субклинического тиреотоксикоза. Первая степень предполагает уровень ТТГ 0,1–0,4 мЕд/л, вторая – менее 0,1 мЕд/л. Российские авторы рекомендуют выделять сниженный и подавленный уровень ТТГ.
В ходе наблюдения за пациентами с подавленным и сниженным уровнем ТТГ было показано, что 76% больных со сниженным ТТГ в течение года вернулись в эутиреоидное состояние без лечения, тогда как при подавленном уровне у 87% пациентов сохранился уровень ТТГ менее 0,1 мЕд/л. Риск прогрессирования субклинического тиреотоксикоза в манифестный, по данным разных авторов, составляет 1–8%.
В нескольких наблюдательных исследованиях отмечено увеличение частоты фибрилляции предсердий при субклиническом тиреотоксикозе. Показана тенденция к повышению смертности от сердечно-сосудистых заболеваний в группах пациентов с субклиническим тиреотоксикозом. Следует отметить, что не все исследователи согласны с такими выводами. Так, метаанализ данных пяти популяционных исследований не показал повышения уровня риска сердечно-сосудистых заболеваний и смерти у больных субклиническим тиреотоксикозом9.
Эксперты Американской тиреоидологической ассоциации и Американской ассоциации клинических эндокринологов в 2011 г. разработали рекомендации, согласно которым при уровне ТТГ ниже 0,1 мЕд/л лечение субклинического тиреотоксикоза в обязательном порядке показано всем пациентам 65 лет и старше, женщинам в период менопаузы, которые не принимают эстрогены или бифосфонаты, а также пациентам с сердечно-сосудистыми факторами риска, заболеваниями сердца, остеопорозом и при наличии симптомов тиреотоксикоза. В случае если уровень ТТГ ≥ 0,1 мЕд/л, но ниже границы референсных значений, лечение субклинического тиреотоксикоза целесообразно у пациентов 65 лет и старше, пациентов с заболеваниями сердца или симптомами тиреотоксикоза10.
Заканчивая свое выступление, Л.В. Трухина отметила важность своевременной диагностики субклинических нарушений функции щитовидной железы. Специалисты должны индивидуально подходить к решению вопроса о необходимости назначения лекарственной терапии пациентам с субклиническими нарушениями функции щитовидной железы – на основании не только своего клинического опыта, но и имеющихся на сегодняшний день консенсусов и клинических рекомендаций эндокринологических ассоциаций.
Заключение
Комбинированный препарат Йодокомб®, производимый компанией «Берлин-Хеми», содержит левотироксин натрия и йодид калия. Он предназначен для лечения диффузного эутиреоидного зоба и профилактики рецидива зоба после резекции щитовидной железы. Препарат Йодокомб® может применяться в рекомендуемых дозах в период беременности и лактации.
Перед назначением упомянутых препаратов, пожалуйста, ознакомьтесь с утвержденной инструкцией по применению.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.