Антимикробная терапия острых гнойных средних отитов в педиатрической практике
- Аннотация
- Статья
- Ссылки



Другой путь – контактный, или транстимпанальный. В этом случае инфицирование среднего уха формируется при нарушении целостности барабанной перепонки при ее разрыве. Такая травма может случиться при попадании в слуховой проход инородного тела и его неаккуратном удалении, при использовании острых предметов для гигиены уха или при ударе (например, мячом, открытой ладонью и т. п.). Третий путь – гематогенный, т.е. по кровеносным сосудам. Так отит возникает при общих инфекционных заболеваниях (корь, скарлатина и т. п.).
В детском возрасте острый средний отит имеет ряд особенностей: во‑первых, возникает чаще, чем у взрослых за счет более широкой и короткой слуховой трубы, наличия аденоидных вегетаций, несформированного иммунитета, преимущественно горизонтального положения младенца, а также вследствие осложненного течения детских инфекционных заболеваний; во‑вторых, диагностика отита у детей раннего возраста затруднена из-за практически полного отсутствия вербального контакта с пациентом и за счет трудностей отоскопии; в‑третьих, в младенческом возрасте увеличивается риск внутричерепных осложнений за счет незаращения каменисто-чешуйчатой щели височной кости, через которую инфекция может проникать в полость черепа, поражая мозговые структуры. Таким образом, острый гнойный средний отит у детей требует к себе более скрупулезного отношения со стороны оториноларинголога по сравнению с взрослым контингентом.
Основным профилактическим мероприятием острого среднего отита является предупреждение и своевременное лечение простудных заболеваний, санация околоносовых пазух при острых и хронических синуситах, обучение правильному сморканию (поочередно через правую и левую ноздрю), аккуратное выполнение туалета ушей, отказ от авиаперелетов при воспалительных процессах верхних дыхательных путей и общеоздоровительные мероприятия.
Неблагоприятным исходом острого среднего отита является его хронизация. Для этого патологического состояния характерна стойкая, незарастающая перфорация барабанной перепонки, гноетечение из ушей, снижение слуха. Заболевание может прогрессировать, приводя к поражению внутреннего уха, следствием чего может быть потеря слуха и вестибулярные нарушения.
Лечение острого среднего отита должно представлять собой комплекс адекватных терапевтических мероприятий, которые можно подразделить на местные и общие.
Местные включают в себя, во‑первых, использование сосудосуживающих капель (нафтизин, назол, отривин и т. п.), которые необходимо закапывать в нос при запрокинутой назад голове. Это обеспечивает уменьшение отека в области носоглоточного устья слуховой трубы и восстановление ее вентиляционной и дренирующей функций.
Местнодействующие препараты, вводимые в слуховой проход, должны обладать следующими фармакологическими возможностями: противовоспалительным действием, противобактериальным и противогрибковым, антиаллергическим и обезболивающим эффектами. В медицинской практике используются однокомпонентные (обладающие одним из вышеперечисленных свойств) и многокомпонентные, комбинированные препараты с антибактериальными свойствами.
В ряде случаев, особенно при тяжелом и затяжном течении отита, необходимо прибегать к антибиотикам системного действия.
Выбор препарата обычно основывается на анализе эпидемиологической ситуации, особенностях клинической картины и тяжести заболевания, возрасте больных и наличии сопутствующих заболеваний, сведений о предшествующей антибактериальной терапии и переносимости лекарственных препаратов.
Антибиотик, применяемый для терапии отитов должен обладать следующими свойствами:
- широким спектром бактерицидного действия;
- высокой активностью против большинства наиболее вероятных возбудителей;
- низкой токсичностью;
- простотой приема;
- оптимальным соотношением цены и эффективности;
- хорошим проникновением в очаг воспаления.
Спектр значимых возбудителей и характер их антибиотикорезистентности в настоящее время таковы, что препаратами выбора для терапии острых отитов на современном этапе являются В‑лактамы и макролиды.
Если врач принимает решение назначить антибактериальную терапию, он должен помнить о двух стоящих перед ним задачах. Тактической задачей является выбор антибиотика с наибольшим терапевтическим и наименьшим токсическим потенциалом. В то же время стратегическая задача – уменьшение риска селекции и распространения резистентных штаммов бактерий в популяции. Решению тактической задачи призваны способствовать данные об устойчивости основных возбудителей внебольничных инфекций в России. В то же время для решения поставленной стратегической задачи необходимо выбирать препараты, с наименьшей вероятностью вызывающие возникновение антибиотико-резистентных штаммов. Огромный арсенал современных антибиотиков, безусловно, расширяет возможности клинициста. Успешной реализации указанных задач способствует хорошая ориентированность в спектре действия, фармакокинетике, микробиологическом влиянии препарата, а также его доказанная эффективность и безопасность. Большинство ошибок при назначении антибиотика в амбулаторной практике связано именно с неправильным выбором препарата. Главным критерием при этом по-прежнему является возможность воздействия на основных возбудителей воспаления. При этом приоритетом для выбора того или иного препарата является не широкий, а оптимальный спектр антибактериальной активности, т.е. охватывающий наиболее значимых по статистическим данным в настоящее время и наиболее вероятных именно для данного больного возбудителей. Многочисленные многолетние исследования подтверждают, что спектр возбудителей острого среднего отита остается относительно постоянным. Наиболее частой причиной воспаления являются Staph. Aureus, Staph. Epi-dermidis Sreptococcus pneumoniae и Haemophilus influenzae. Реже встречаются Streptococcus pyogenes, Moraxella catarrhalis, Streptococcus viridans, анаэробы. Выбор антибиотика для лечения инфекций дыхательных путей остается довольно трудной задачей, несмотря на обилие антимикробных средств различных химических групп. Трудности выбора определяются вынужденным эмпирическим подходом к антибиотикотерапии, изменением спектра возбудителей в зависимости от эпидемиологической ситуации и сезона, отсутствием полноценного наблюдения за течением заболевания, и, следовательно, реального маневра в тактике лечения при первых признаках его неэффективности. Все большую актуальность в наших условиях приобретает стоимостный аспект терапии. Эмпирический подход к лечению зиждется не только на отсутствии возможности идентификации возбудителя в амбулаторных условиях. Даже в хорошо оборудованных стационарах на выяснение этиологически значимого микроорганизма и определение его антибиотикочувствительности уходят 3–4 дня (а в случае «атипичных» патогенов и более), в течение которых больной не может оставаться без лечения. Существуют определенные правила применения антибиотиков. Доза препарата и длительность курса, предписанные врачом, должны быть строго соблюдены. Нормализация температуры тела, улучшение самочувствия и даже полное исчезновение симптомов болезни не должны становиться поводом для преждевременного прерывания курса или сокращения дозы антибиотиков. Ранняя отмена препаратов может стать причиной осложнений, перехода заболевания в хроническую форму, выработки резистентности к антибиотику у возбудителя. Существует и другая крайность. Некоторые люди панически боятся антибиотиков и не принимают их даже при самых тяжелых инфекциях вопреки рекомендациям врача. Вспоминая опыт предков, надеются на собственные силы.
Однако для современного жителя мегаполиса, с его стрессами, авитаминозами и иммунодефицитами, даже банальный нелеченный насморк грозит серьезными осложнениями, что уж говорить про инфекции, требующие антибиотикотерапии. В последнее время активно обсуждается проблема так называемых пенициллинорезистентных пневмококков, которая может приобретать крупномасштабный характер. В этих условиях встает вопрос об альтернативном лечении. В качестве средств, которые могут преодолеть эту нечувствительность пневмококков, рекомендуются цефалоспорины III поколения, карбапенемы, гликопептиды и фторхинолоны последнего поколения (грепафлоксацин, тровафлоксацин). Следует учесть, что увеличилась частота резистентности пневмококков и к макролидным антибиотикам; здесь мы имеем феномен перехода количества в качество – чем больше частота назначений этих антибиотиков, тем чаще появляются устойчивые к ним формы бактерий.
Гемофильная палочка высокочувствительна к “защищенным” пенициллинам, цефалоспоринам II поколения, фторхинолонам, азалидам (азитромицин) и некоторым макролидам (кларитромицин, рокситромицин). Она малочувствительна к бензилпенициллину, а ампициллин часто оказывается неэффективным из-за инактивирующего действия бета-лактамаз, частота продукции которых отмечается у 20–40% штаммов.
Хламидии считаются проблемными возбудителями, частота инфицирования ими верхних дыхательных путей и среднего уха достоверно не известна, причем данные по ней противоречивы. Это связано с трудностями идентификации хламидии, поскольку диагностика осуществляется серологически методом парных сывороток. По различным данным, частота хламидиозной этиологии ЛОР-инфекций составляет 1–10%. Учитывая, что хламидии располагаются внутриклеточно, препаратами выбора считаются азалиды и макролиды, активно проникающие в клетку. Беталактамы при хламидийной этиологии применять не следует, поскольку внутрь клеток они не проникают.
Микоплазмы, как и хламидии, при абсолютной устойчивости к беталактамным антибиотикам, проявляют чувствительность к макролидам. Учитывая основные патогены, фигурирующие в этиологии инфекций среднего уха, у детей можно выделить следующие группы препаратов, перспективные для использования: беталактамы (аминопенициллины, цефалоспорины), азалиды и макролиды. Причем наибольшее «перекрытие» спектра возбудителей прослеживается у азалидных и макролидных антибиотиков. Нет недостатка в подтверждении клинической эффективности этих средств как в отечественной, так и в зарубежной литературе.
Макролиды – большая группа антибиотиков (природных и полусинтетических), основу химической структуры которых составляет макроциклическое лактонное кольцо с одним или несколькими углеводными остатками. В зависимости от числа атомов углерода в кольце макролиды подразделяются на 14‑членные (эритромицин, кларитромицин, рокситромицин), 15‑членные (азитромицин) и 16‑членные (джозамицин, мидекамицин, спирамицин). Первый представитель этой группы – эритромицин – был открыт и внедрен в клинику в начале 50‑х годов прошлого столетия, широко применяется и в настоящее время при лечении респираторных инфекций, болезней кожи и мягких тканей, в последние годы в круг его показаний также вошли инфекции, вызываемые внутриклеточными «атипичными» бактериями. По спектру и степени антибактериальной активности представители этой группы близки, исключение составляют новые полусинтетические макролиды (азитромицин и кларитромицин), которые проявляют большую активность в отношении многих внутриклеточных бактерий, некоторых возбудителей опасных инфекций (бруцеллы, риккетсии), грамположительных и грамотрицательных неспорообразующих анаэробов и др. По механизму действия макролиды являются ингибиторами синтеза белка. Как правило, макролиды оказывают бактериостатическое действие, но в некоторых условиях: при изменении рН-среды, снижении плотности инокулума, высоких концентрациях могут действовать бактерицидно [1].
Большинство клинически значимых представителей макролидов относится к 14‑16‑членным макролидам. Азитромицин является полусинтетическим производным эритромицина А, в котором метильная группа замещена атомом азота, и образует новую 15‑членную структуру, выделенную в новую подгруппу (азалиды). По ряду свойств (большая активность против некоторых грамотрицательных бактерий, наибольшая пролонгированность действия, клеточная направленность фармакокинетики и др.) азитромицин отличается от своих предшественников [2].
На фармацевтическом рынке России азитромицин широко представлен препаратом, который выпускается под торговым названием Сумамед.
Aзитромицин характеризуется сверхшироким спектром действия: он активен против большинства грамположительных микроорганизмов, многих грамотрицательных бактерий, «атипичных» внутриклеточных возбудителей респираторных инфекций. Азитромицин обладает улучшенными фармакокинетическими свойствами: пролонгированной фармакокинетикой (Т1/2 азитромицина, в зависимости от дозы, составляет 48–60 часов), способностью накапливаться и длительно задерживаться в иммунокомпетентных клетках в течение 8–12 суток после завершения 3–5‑дневных курсов приема внутрь в стандартной дозе.
Тканевая и клеточная направленность кинетики, пролонгированное действие азитромицина, возможность эффективного применения короткими курсами без опасности развития серьезных побочных реакций обусловливают невысокий риск развития и распространения антибиотикоустойчивости. Азитромицин характеризуется высокой комплаентностью, улучшенными показателями в соотношении стоимость/эффективность. Все это подтверждает целесообразность применения Сумамеда в лечении больных острым средним отитом детей.
Несмотря на достаточно большой арсенал медикаментозных средств для лечения воспалительных заболеваний уха, их самостоятельное, без квалифицированной врачебной консультации, назначение нецелесообразно и даже вредно. Это связано, в первую очередь, с тем, что на основании одних только жалоб, без отоскопии и без бактериологического исследования, невозможно установить характер заболевания, а, следовательно, и выбрать правильную тактику лечения. Важно помнить о возможных серьезных осложнениях острого и хронического среднего отита, предупредить или купировать которые возможно только с помощью оториноларинголога. Попытки самостоятельного, часто безграмотного лечения могут привести к достаточно тяжелым негативным явлениям.
Перед исследователями была поставлена задача определить степень эффективности препарата Сумамед при лечении детей, страдающих острым средним отитом; а также безопасность использования этого лекарственного средства. Обследовано 20 больных детей в возрасте от 5 до 12 лет (девочек – 8, мальчиков – 12). Всем пациентам проведено лечение препаратом Сумамед из расчета 10 мг/кг массы тела 1 раз в день в течение 3 дней (курсовая доза 50 мг/кг).
Также для контроля под наблюдением находились и аналогичные в количественном отношении группы детей, получавшие цефазолин по 0,5 мл 2 раза в сутки парентерально в течение 3 дней.
- Критерии включения: дети старше 3 лет, страдающих острым средним отитом,
- Критерии исключения: больные, получавшие иное лечение по поводу исследуемого заболевания, имеющие почечную и печеночную выраженную патологию и отягощенные аллергическим анамнезом в отношении антибактериальных препаратов, а также пациенты с микотической этиологией заболевания.
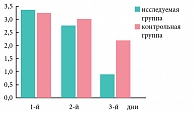
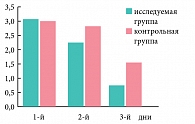
Регистрация результатов обследования и лечения регистрировалась в специально разработанной индивидуальной карте. Оценка динамики клинических проявлений заболевания производилась ежедневно в течение 3 дней по пятибальной визуально аналоговой шкале. Наряду со стандартным оториноларингологическим обследованием пациентам проводили аудиометрию, тимпанометрию, рентгенографию или компьютерную томографию околоносовых пазух, рентгенографию височных костей по Шюллеру и Майеру, общеклинический анализ крови, бактериологическое исследование отделяемого из слухового прохода при наличии перфоративного отита.
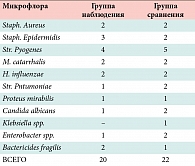
В процессе обследования и лечения отмечено уверенное уменьшение клинических проявлений и положительная динамика объективных критериев заболевания в исследуемой группе. Зарегистрирована более высокая эффективность лечения в исследуемой группе по сравнению с контрольной. В связи с тем, что вероятным путем распространения инфекции в среднее ухо была слуховая труба, то для ориентировочного представления о характере возбудителя, мы исследовали флору носоглотки и только при наличии перфорации барабанной перепонки имели возможность бактериологического анализа микробного пейзажа барабанной полости.
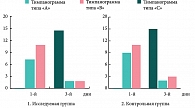
На основании тимпанометрии, проводимой в начале лечения, получены следующие результаты: в исследуемой группе тимпанограмма типа «В» выявлена у 8 больных, тимпанограмма типа «С» – у 12. По окончании курса лечения – тимпанограмма «А»- у 16, «В» – у 2, и кривая тип «С» – у 2 пациентов.
В контрольной группе: до начала лечения тимпанограмма типа «В» зафиксирована у 9‑ти больных, «С» – у 11‑ти. По завершении шестидневного курса традиционной терапии получены следующие результаты тимпанометрии: «А» – 15 человек, «В» – 2 человека и «С» –3 человека.
Полученные нами данные подтвердили высокую лечебную эффективность препарата сумамед при остром среднем отите у детей. Препарат отличается безопасностью и простотой в применении и может быть рекомендован для широкого применения в детской оториноларингологической практике.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.