Антитромботическое лечение в кардиологии: возможность использования новых средств и новых подходов к терапии
- Аннотация
- Статья
- Ссылки



Наряду с результатами крупных исследований среди новостей оказываются и изменения рекомендательных документов.
Дополнение к американскому руководству по лечению больных ОИМ с подъемами ST
В ноябре 2009 г. американские Ассоциация сердца, Коллегия кардиологов и Общество по сердечно-сосудистой ангиографии и вмешательствам выпустили обновление руководства по лечению больных острым инфарктом миокарда (ОИМ) с подъемами ST (1). В очередном документе отражено отношение экспертов к результатам исследований, появившихся после предыдущего обновления (2007), но без учета результатов наиболее «свежих» исследований, представленных во второй половине 2009 г. Изменения касаются и антитромботического лечения.
Среди ключевых моментов этого документа – появление прямого ингибитора тромбина бивалирудина как антикоагулянта, используемого при первичном чрескожном коронарном вмешательстве (ЧКВ) (класс доказательств I, уровень B), особенно у больных с высоким риском кровотечений (класс IIa, уровень B). Данное дополнение – первый рекомендательный документ, допускающий применение вместо клопидогреля нового тиенопиридина – празугреля.
Кроме того, в дополнение к действующим рекомендациям уточнены детали использования клопидогреля, расширены сроки применения тиенопиридинов (клопидогреля или празугреля) после коронарного стентирования: до 12 месяцев после установки простого металлического стента (класс I, уровень B) и более 15 месяцев после имплантации стента, выделяющего лекарства (класс IIb, уровень C).
К сожалению, при создании любых рекомендательных документов время, затраченное на многократное экспертное «взвешивание» и обсуждение новых данных, достаточно велико. И даже при очень оперативных сборе и обработке данных эта задержка ведет к тому, что публикация документа, как правило, совпадает и даже отстает от появления новой информации, делающей некоторые положения руководства устаревшими уже в момент их появления.
Наиболее значимыми событиями 2009 года в области антитромботических вмешательств следует признать достижения в профилактике эмболических осложнений и прежде всего ишемического инсульта у больных с мерцательной аритмией и появление новых антитромбоцитарных средств и новых подходов к применению уже известных средств этого класса у больных с острыми коронарными синдромами (ОКС).
Исследование Re-ly: найдена альтернатива Варфарину
Без сомнений, новостью номер один следует считать результаты исследования RE-LY (2), в которых выявлена потенциальная замена антагонистам витамина К, прежде всего варфарину, многие годы являвшимся безальтернативным средством предотвращения тромбоэмболических осложнений у больных с мерцательной аритмией. До 2009 г. общепризнанным было не только преимущество варфарина перед другими доступными к этому времени вмешательствами, но и неизбежное при применении непрямых антикоагулянтов увеличение риска геморрагических событий, в том числе крупных и угрожающих жизни. На практике менее половины больных с мерцательной аритмией, имеющих показания к антикоагулянтной терапии, получают варфарин или его аналоги. Главным ограничением широкого применения варфарина и других препаратов этого класса, наряду с обоснованной боязнью кровотечений, является сложность их использования, обусловленная выраженной вариабельностью индивидуального ответа больного, узким «терапевтическим интервалом» основного действия препарата, необходимостью в достаточно частом коагулологическом контроле для обеспечения эффективности и безопасности лечения, многочисленными лекарственными и пищевыми взаимодействиями. Большинства этих недостатков лишен дабигатран, прямой ингибитор тромбина, предназначенный, как и непрямые антикоагулянты, для приема внутрь и уже имеющий доказательства целесообразности его применения в профилактике венозных тромбоэмболий в травматологии и ортопедии.
В исследовании RE-LY (Randomized Evaluation of Long-term anticoagulant therapY – «Рандомизированная оценка длительной антикоагулянтной терапии»), задуманным с использованием гипотезы демонстрации не-превосходства (non-inferiority), или равенства, сравниваемых вмешательств, с декабря 2005 г. включено 18113 пациентов с мерцательной аритмией и высоким или умеренным риском инсульта. Они были рандомизированы в три группы. В одной из них больным открыто (без «ослепления» и плацебо-контроля) подбиралась и поддерживалась доза варфарина с целевым значением международного нормализованного отношения (МНО) от 2 до 3. В двух других больным «вслепую» назначалась одна из двух, отобранных на основании более ранних исследований, доз дабигатрана: 110 мг 2 раза в день или 150 мг 2 раза в день. Медиана продолжительности лечения и наблюдения составила 2 года. Основными событиями, частоту которых сравнивали в изучавшихся группах больных, были выбраны инсульт и системные (артериальные) эмболии. Кроме того, сопоставляли частоту кровотечений, в том числе внутричерепных, и некоторых других событий, среди которых инфаркт миокарда и смертельные исходы.
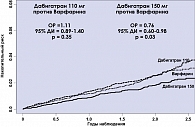
Ежегодная частота инсульта и/или системных эмболий составила 1,69% в группе варфарина; 1,53% в группе меньшей дозы дабигатрана и 1,11% в группе больных, получавших дабигатран в дозе 150 мг 2 раза в день. Полупроцентное абсолютное преимущество большей дозы дабигатрана перед варфарином оказалось статистически значимым: относительный риск составил 0,66 с 95% доверительным интервалом от 0,53 до 0,82 и, исходя из гипотезы превосходства, значением p < 0,001. Меньшая доза дабигатрана не уступала варфарину: относительный риск составил 0,91 с 95% доверительным интервалом от 0,74 до 1,11 (p < 0,001, исходя из гипотезы не-превосходства).
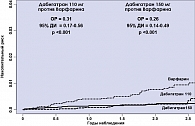
Дабигатран, используемый без какого-либо коагулологического контроля, имел преимущество перед дозируемым по результатам определения МНО варфарином не только с позиций профилактики эмболических осложнений (рисунок 1), но и с позиций геморрагической безопасности: ежегодная частота крупных кровотечений составила 3,36% в группе варфарина, 2,71% в группе 110 мг дабигатрана (p = 0,003) и 3,11% на фоне 150 мг дабигатрана (p = 0,31). Ежегодная частота геморрагических инсультов составила 0,38%, 0,12% (p < 0,001) и 0,10% (p < 0,001) соответственно (рисунок 2).
Важным итогом исследования оказалась заметная, хотя и недостоверная с позиций статистики, разница в частоте смертельных исходов. За каждый год наблюдения умирали 4,13% больных в группе варфарина, 3,75% в группе дабигатрана 110 мг (p = 0,13) и 3,64% в группе дабигатрана 150 мг (p = 0,051).
Таким образом, применение меньшей дозы дабигатрана в сравнении с использованием варфарина у больных мерцательной аритмией сопровождалось сходной частотой инсультов и эмболий, но несло с собой меньшую угрозу геморрагических осложнений, включая меньший риск внутричерепных кровоизлияний. Использование большей дозы дабигатрана (150 мг 2 раза в день) вело к наименьшему риску инсульта и эмболий (в сравнении с варфарином и дозой дабигатрана в 110 мг 2 раза в день) и формально не имело преимуществ по частоте крупных кровотечений перед варфарином: относительный риск желудочно-кишечных кровотечений увеличивался на 50% (p < 0,001), но одновременно с этим достоверно меньшей, чем в группе варфарина, была частота угрожающих жизни и внутричерепных кровотечений.
Таким образом, в одном исследовании были найдены более эффективный и более безопасный подходы к профилактике тромбоэмболических осложнений у больных с мерцательной аритмией (большая и меньшая дозы дабигатрана соответственно), что, без сомнений, расширяет возможности адаптации адекватной антикоагулянтной терапии к индивидуальным особенностям больного.
Не следует забывать и о том, что применение дабигатрана не требует контроля за коагуолологическими показателями. Последнее создает условия для более широкого применения антикоагулянта за счет присоединения его к лечению больных, у которых изменение дозы варфарина на основании регулярного определения МНО не представляется возможным. Среди возможных ограничений широкого и длительного применения дабигатрана в России может оказаться стоимость препарата. Дабигатран, в отличие от варфарина, требует приема 2 раза в день, что, наряду с более частым развитием признаков диспепсии и большей частотой преждевременного прекращения приема препарата, зарегистрированными в исследовании RE-LY, может существенно повлиять на комплаентность больных.
Следует вспомнить, что предшественник дабигатрана – ксимелагатран уже получал одобрение для применения его у больных с мерцательной аритмией на основании результатов исследований, в которых он сравнивался с варфарином. Ксимелагатран был даже зарегистрирован в России. Через очень короткое время он был отозван с рынка из-за появившихся сообщений о его гепатотоксичности, включая случаи, угрожающие жизни больных. В исследованиях, ставших основаниями для регистрации ксимелагатрана, угроза потенциальной гепатотоксичности проявлялась в лабораторных данных в виде заметного повышения активности трансаминаз у существенной части больных. Для осознания реальных последствий этого лабораторного феномена потребовался выход препарата на рынок.
В обсуждаемом исследовании RE-LY на основании регулярной оценки активности печеночных трансаминаз не было получено указаний на гепатотоксичность дабигатрана. Некоторые эксперты считают, что достаточно короткая длительность лечения (2 года) не дает оснований говорить о долгосрочной безопасности в отношении печеночных эффектов дабигатрана. Среди других «слабых мест» в замысле и результатах исследования Re-LY: открытое, а не ослепленное, сравнение варфарина и дабигатрана, а также требующая внятного объяснения большая, чем при использовании варфарина, частота развития инфаркта миокарда в каждой из групп больных, получавших дабигатран.
Как бы то ни было в будущем, результаты исследования RE-LY впервые за много лет обозначили возможность использования у больных мерцательной аритмией альтернативного непрямым антикоагулянтам антитромботического средства. Выявленные преимущества дабигатрана перед варфарином, а не равенство этих двух средств, как это предусматривалось первоначальным замыслом испытания RE-LY, существенно усложнили жизнь организаторам других, еще продолжающихся исследований по сравнению новых антикоагулянтов с варфарином у этой категории больных.
Эти сложности распространяются прежде всего на испытания пероральных ингибиторов десятого фактора (апиксабана и ривароксабана), изучение которых с участием многих тысяч больных проходит в исследованиях с использованием гипотезы non-inferiority. В случае подтверждения этой гипотезы отсутствие преимуществ этих средств перед варфарином на уровне эффективности и безопасности, заведомо более высокая, чем у варфарина, стоимость и наличие на рынке средства с уже доказанными преимуществами (дабигатран) создаст серьезные трудности с внедрением этих новых антикоагулянтов в реальную практику. Вероятность возникновения подобных трудностей достаточно велика, несмотря на большую, чем у варфарина, простоту применения новых средств (фикисрованные, как и у дабигатрана, дозы, отсутствие необходимости в коагулологическом контроле): разрешающие инстанции могут потребовать от производителей проведения новых исследований по сравнению этих средств с дабигатраном.
Исследование Plato: еще одна потенциальная замена Клопидогреля при ОКС
Следующей по значимости новостью антитромботического лечения в 2009 г. следует признать результаты исследования PLATO (PLAtelet inhibiTion and patient Outcomes – «Подавление тромбоцитов и исходы (наблюдения) у больных») (3), выполненного у больных ОКС. В нем предпринята весьма успешная попытка потеснить еще один общепризнанный антитромботический препарат – клопидогрел, безоговорочно входящий в современные стандарты лечения больных с любым вариантом и любой стратегией ведения больных ОКС. В качестве средства, призванного заменить клопидогрел, в данном исследовании выбран тикагрелор. Тикагрелор – новый антитромбоцитарный препарат, являющийся, как и клопидогрел, ингибитором тромбоцитарных P2Y12-рецепторов к аденозиндифосфату, но отличающийся от него прямой (без образования активного метаболита путем печеночного метаболизма) и обратимой блокадой рецептора. Эти различия, по данным исследований, предшествовавших PLATO, позволяют добиваться более быстрого и более выраженного, чем у стандартных доз клопидогреля, подавления активности тромбоцитов с возможностью более быстрого прекращения действия препарата в случае развития кровотечения или ситуации с высоким риском кровотечения.
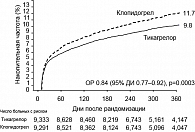
Последний факт особенно актуален для больных ОКС, подвергаемых экстренным операциям шунтирования коронарных артерий. В исследовании PLATO 18624 больные, госпитализированные с ОКС (с подъемами или без подъемов сегмента ST), с использованием двойного слепого метода и рандомизации были разделены на 2 группы. В одной из них применялось стандартное лечение, частью которого был клопидогрел (300 мг нагрузочная доза для большинства больных, затем 75 мг в сутки), в другой вместо клопидогреля использовался тикагрелор (180 мг нагрузочная доза, затем 90 мг 2 раза в сутки). Длительность сравнения – 12 месяцев. Основная конечная точка наблюдения, как это чаще всего принято в подобных исследованиях, была составной и включала смерть от сердечно-сосудистых причин, инфаркт миокарда или инсульт. В итоге исследования суммарная частота этих событий составила 9,8% у получавших тикагрелор и 11,7% у получавших клопидогрел (отношение рисков 0,84; 95% доверительный интервал 0,77 до 0,92; p < 0,001).
Анализ по предопределенным до начала исследования дополнительным конечным точкам наблюдения выявил другие достоверные отличия, включая разницу по частоте инфаркта миокарда (5,8% в группе тикагрелора против 6,9% в группе клопидогреля, p = 0,005), смерти от сердечно-сосудистых причин (4,0% против 5,1%, p = 0,001), но без достоверных различий в частоте инсульта (1,5% против 1,3%, p = 0,22). Наиболее убедительным аргументом в пользу тикагрелора следует считать меньшую частоту случаев смерти от любой причины (4,5% в группе тикагрелора против 5,9% в группе клопидогреля; p < 0,001). На современном этапе абсолютное снижение смертности на 1,5% можно признать уникальным, учитывая, что зарегистрировано оно в условиях сравнения не с плацебо, а с активным лечением, считавшимся на момент проведения исследования стандартом оказания помощи больным ОКС.
Примечательно, что снижение риска ишемических событий с помощью тикагрелора было достигнуто без статистически значимого увеличения риска крупных геморрагических осложнений (11,6% в группе тикагрелора и 11,2% в группе клопидогреля; p = 0,43) (рисунок 3). Более детальный анализ наиболее тяжелых кровотечений оставляет двойственное впечатление о геморрагической безопасности тикагрелора. С одной стороны, его применение сопровождалось несколько большей частотой внутричерепных кровотечений (26 случаев – 0,3% против 14 случаев – 0,2% в группе клопидогреля, p = 0,06), при этом разница по числу смертельных внутричерепных кровотечений была десятикратной и статистически значимой (11 случаев – 0,1% в группе тикагрелора и только 1 случай – 0,01% в группе клопидогреля, p = 0,02). Преимущество клопидогреля перед тикагрелором по этому крайне важному показателю с лихвой компенсировалось существенно большей частотой смертельных кровотечений других локализаций (9 – 0,1% в группе тикагрелора и 21 – 0,3% в группе клопидогреля; p = 0,03). Использование тикагрелора сопровождалось достоверно большей частотой крупных кровотечений, не связанных с операциями коронарного шунтирования (4,5% в группе тикагрелора и 3,8%, p = 0,03).
Несмотря на очевидное преимущество тикагрелора на уровне основной конечной точки исследования, ряд результатов PLATO требует прояснения. Так, в этом крупном исследовании подтвердилась способность тикагрелора вызывать одышку, ставшую основанием для прекращения лечения в 0,9% случаев (0,1% в группе клопидогреля). В субисследовании с суточным мониторированием ЭКГ по Холтеру подтвердилась отмеченная ранее более высокая частота возникновения пауз в работе желудочков сердца: паузы длительностью более 3 с встречались на первой неделе исследования у 5,8% больных в группе тикагрелора и у 3,6% больных в группе клопидогреля (p = 0,01). Достоверных различий между сравниваемыми группами в частоте подобных пауз на 30-й день лечения не отмечено. К настоящему времени нет никаких внятных объяснений для подобных эффектов тикагрелора, равно как и отмеченным в ходе исследования большим, чем в группе клопидогреля, уровням креатинина и мочевой кислоты.
Отдельных объяснений может потребовать целый ряд статистически значимых взаимодействий, выявленных при анализе подгрупп: на уровне основной конечной точки исследования тикагрелор не имел преимущества перед клопидогрелем у больных, не получавших гиполипидемической терапии, у больных с массой тела меньше медианы (значение p для взаимодействия с основным эффектом в обоих случаях равно 0,04). Интересны и региональные различия в сравнении эффективности тикагрелора и клопидогреля: преимущество тикагрелора перед клопидогрелем было сходным с результатами исследования в целом в таких региональных объединениях, как Азия и Австралия, Южная и Центральная Америка, Европа, Ближний Восток и Африка. На территории Северной Америки (в США и Канаде) тикагрелор не только не имел преимуществ перед клипидогрелем, но и заметно уступал ему. Относительная частота событий основной конечной точки в сравниваемых группах в этой части света была на 25% выше в группе тикагрелора, чем в группе клопидогреля (11,9% в группе тикагрелора и 9,6% в группе клопидогреля, p = 0,05 для взаимодействия основного эффекта с «регионами»). Этот факт может создать серьезные препятствия для одобрения тикагрелора в США, а значит, и во многих других странах, разрешительные органы которых действуют с оглядкой на решения FDA. Как бы то ни было, важнейшим итогом исследования PLATO является статистически значимое и очень убедительное (на уровне абсолютных значений) снижение общей смертности при использовании у больных ОКС нового антитромбоцитарного средства тикагрелора. При использовании результатов исследования PLATO на практике (в случае одобрения) не следует забывать, что они применимы только к больным, соответствующим критериям включения в исследование. Это означает, что нет и в обозримом будущем не будет оснований для применения тикагрелора у больных ОКС с подъемом сегмента ST, повергнутых тромболитической терапии и не получивших реперфузионного вмешательства, так как в исследование PLATO включались исключительно больные ОКС с подъемом сегмента ST, планируемые для первичного внутрикоронарного вмешательства.
Исследование Current-oasis-7: поиск оптимальных доз аспирина и Клопидогреля для больных с ОКС
В качестве значимой новости 2009 года в антитромботическом лечении в кардиологии следует рассмотреть и долгожданные результаты исследования CURRENT-OASIS-7, не имевшего своей целью изучение эффектов новых средств, но предназначенного расставить точки над i в вопросах дозирования двух основных антитромбоцитарных средств, широко используемых в лечении ОКС: аспирина и клопидогреля. Насколько это удалось, станет ясно из последующего изложения основных результатов исследования.
Исследование CURRENT OASIS-7 (Clopidogrel Optimal Loading Dose Usage to Reduce Recurrent Events/Optimal Antiplatelet Strategy for Interventions – «Применение оптимальной нагрузочной дозы клопидогреля для уменьшения повторных событий / Оптимальная антитромбоцитарная стратегия для вмешательств») является одним из крупнейших (n = 25087) в истории изучения антитромбоцитарных средств. Предпосылками для его выполнения стали результаты некоторых клинико-лабораторных исследований, показавших, что использование клопидогреля в дозе, большей, чем стандартная (300 мг начальная, далее 75 мг/сут.), влечет за собой большее подавление активности тромбоцитов и уменьшает долю больных, «резистентных» к антитромбоцитарным эффектам клопидогреля. Клинические данные, подтверждающие эту гипотезу, были малоубедительными, в основном из-за небольшого числа больных, участвовавших в исследованиях с высокими дозами клопидогреля. Это не помешало экспертам сразу нескольких научных сообществ еще в 2007 году рекомендовать высокую нагрузочную дозу клопидогреля для применения ее в связи с неотложными внутрикоронарными вмешательствами у больных ОКС. Представители основного производителя клопидогреля, как и некоторые из экспертов, стоящих на позициях доказательной медицины, советовали воздерживаться от использования подобных доз до получения результатов крупных исследований, подтверждающих эффективность и безопасность подобного дозирования клопидогреля.
Результаты исследования CURRENT-OASIS-7, посвященного в основной своей части проверке гипотезы о превосходстве высокой дозы клопидогреля (600 мг нагрузочная доза с последующим краткосрочным применением 150 мг/сут.) были впервые представлены на Конгрессе Европейского кардиологического общества 2009 года и к моменту написания данной статьи еще не опубликованы. Согласно замыслу исследования, больные ОКС в рамках ранней инвазивной стратегии были рандомизированы к высокой дозе клопидогреля и получали нагрузочную дозу препарата в 600 мг, после которой в течение следующих 7 дней клопидогрел в дозе 150 мг/сут., а затем до 30-го дня по 75 мг/сут. Больные, рандомизированные к получению клопидогреля по стандартной схеме, после нагрузочной дозы 300 мг в течение 30 дней принимали препарат в дозе 75 мг/сут. Кроме того, в этом исследовании была предпринята попытка разрешить давно существующий спор об эффективности и безопасности общепризнанных и так называемых «американских» доз аспирина у больных ОКС. В связи с этим в CURRENT OASIS-7 рандомизировано, но открыто сравнивались два подхода к использованию аспирина – в обычных рекомендуемых (75-100 мг) и более высоких (300-325 мг) дозах.
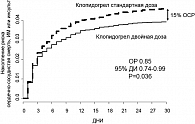
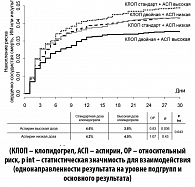
С позиций доказательной медицины результаты CURRENT-OASIS-7 следует трактовать как отрицательные для бóльших доз клопидогреля и аспирина. В исследовании в целом различий между результатами у больных, получавших стандартные и более высокие нагрузочную и поддерживающую дозы клопидогреля, не было. Как и следовало ожидать, существенная доля больных (30%), получивших большую или стандартную нагрузочную дозу клопидогреля в рамках исследования в ожидании коронарографии и возможного чрескожного коронарного вмешательства (ЧКВ), этому вмешательству повергнута не была, так как не нуждалась в нем либо из-за отсутствия субстрата для вмешательства, либо из-за наличия оснований для выполнения шунтирующей операции. Именно в этой подгруппе больных отсутствовали указания на преимущество удвоенной дозы клопидогреля перед стандартной (таблица 1). Основные организаторы исследования и интерпретаторы его результатов сочли возможным, несмотря на то что это противоречило начальному замыслу исследования (4), в качестве основного результата исследования рассматривать данные, полученные при сравнении разных доз клопидогреля в подгруппе больных, подвергнутых ЧКВ (рисунок 4).
В этой достаточно многочисленной группе (n = 17232) применение двойных нагрузочной и поддерживающей доз клопидогреля привело к достоверному снижению на 15% суммы событий, составлявших первичную конечную точку исследования (сердечно-сосудистая смерть, инфаркт миокарда или инсульт), снижением на 22% риска инфаркта миокарда (см. таблицу 1) и на 42% – риска определенного тромбоза стента.
Применение удвоенной дозы клопидогреля сопровождалось увеличением частоты крупных кровотечений, оцениваемых по созданной в рамках исследования CURRENT-OASIS-7 классификации, а также ростом потребности в переливании препаратов крови (таблица 2).
Основной вывод, касающийся сравнения двух режимов дозирования клопидогреля, в исследовании CURRENT: удвоение нагрузочной дозы клопидогреля с последующим краткосрочном удвоением его поддерживающей дозы у больных ОКС в рамках ранней инвазивной стратегии не сопровождается статистически значимым улучшением клинических результатов.
В подгруппе больных, подвергнутых в рамках ранней инвазвиной стратегии ЧКВ, подобное дозирование клопидогреля, при сравнении его со стандартным режимом, ведет к снижению риска крупных ишемических событий и тромбоза стента. Это снижение риска ишемических событий достигается ценой увеличения риска крупных кровотечений. Вполне очевидно, что именно этот режим будет призван отстаивать позиции клопидогреля в противостоянии с новыми антиагрегантами (тикагрелором, празугрелем и другими) если не в рамках исследований с прямым сравнением этих средств, то в рамках многочисленных дискуссий на эту тему.
Большое число больных, включенных в исследование CURRENT, позволило выявить ряд статистически значимых взаимодействий на уровне анализа подгрупп. Первое и главное для этого исследования взаимодействие на уровне подгрупп больных, подвергнутых и не подвергнутых ЧКВ, фактически изложено и в какой-то мере обсуждено выше. В исследовании, задуманном с применением факториала 2 ´ 2, нельзя отмести различия в эффектах удвоенной дозы клопидогреля в зависимости от использовавшейся в рандомизированном режиме дозы аспирина. Оказалось, что удвоенная доза клопидогреля оказывает выявленное в подгруппе больных, подвергнутых ЧКВ, положительное влияние на суммарный риск основных ишемических событий только в присутствии большей (из двух сравниваемых) доз аспирина (рисунок 5).
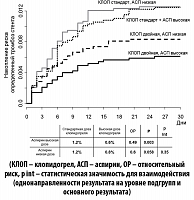
Взаимодействие доз аспирина с эффектами сравниваемых доз клопидогреля было статистически значимым, но интерпретаторы полученных результатов сочли его несущественным, так как подобное взаимодействие отсутствовало на уровне другой, более чувствительной, по их мнению, вторичной конечной точки наблюдения – частоте тромбозов стента (рисунок 6) и суммы случаев тромбоза стентов и инфарктов миокарда.
Еще одно статистически значимое взаимодействие не удалось отмести и на этом уровне. Оказалось, что удвоенная доза клопидогреля имеет преимущество перед стандартной исключительно в подгруппе курящих на момент включения в исследование больных. На уровне некурящих больных ОКС, а таковых в данном анализе было абсолютное большинство (10845 из 17232 подвергнутых ЧКВ), преимущество удвоенной дозы отсутствовало. Это взаимодействие подкреплено не только статистическими данными, но и результатами подобного анализа в ранее выполненных исследованиях, составляющих доказательную базу стандартного режима дозирования клопидогреля: польза от его использования отсутствовала в подгруппе некурящих в исследованиях CREDO и CLARITY-TIMI28.
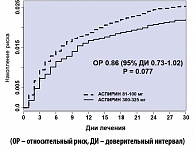
Результаты второй части исследования CURRENT, посвященные открытому сравнению двух доз аспирина, на первый взгляд, однозначны и указывают на нецелесообразность использования большей дозы: в исследовании не было обнаружено статистически значимых различий по эффективности или по частоте кровотечений при применении аспирина в дозах 75-100 мг и 300-325 мг (таблица 3). С другой стороны, большая доза была ничем не хуже рекомендуемой низкой. Более того, при беглом взгляде на таблицу 3 обращает внимание стойкая тенденция к меньшему числу неблагоприятных исходов именно в группе большей дозы (даже по частоте крупных кровотечений по ТIMI). Примечательно, что своего максимума эта тенденция, представляющаяся в графическом виде очень внушительной, достигла на уровне самого важного показателя эффективности и безопасности вмешательства – сравнения общей смертности в двух группах аспирина (рисунок 7). Эти данные, наряду с информацией о бесполезности удвоенной дозы клопидогреля на фоне стандартной (низкой) дозы аспирина, полученной в этом же исследовании, оставляют шанс на существование для большей дозы аспирина, особенно там, где эта доза была популярной до завершения исследования CURRENT-OASIS-7.
Исследования Champion-pci и Champion-platform: провал Кангрелора или неудачный замысел исследований?
Кангрелор, как и тикагрелор, являясь мощным, нетиенопиридиновым блокатором P2Y12 рецепторов тромбоцитов, предполагает наличие нескольких уникальных особенностей, среди которых возможность парентерального (внутривенного) введения, обратимость действия и короткий период полужизни (от 3 до 5 минут). Из-за отсутствия необходимости в дополнительных превращениях после попадания в организм использование кангрелора предусматривает близкое к полному подавление активности тромбоцитов с очень быстрым наступлением этого эффекта. Из-за того что антитромбоцитарное действие кангрелора может быть полностью устранено через 30-50 минут после прекращения его введения, этот препарат может иметь преимущества у тех больных, у кого по данным коронароангиографии требуется быстрое подавление активности тромбоцитов в связи с ЧКВ и у кого может потребоваться быстрое прекращение этого действия (чаще всего при возникновении необходимости в экстренной шунтирующей операции).
Оценка кангрелора на ранних стадиях изучения выявила возможность очень выраженного, быстрого и безопасного подавления активности тромбоцитов у больных с ОКС без подъемов ST, не подвергавшихся ЧКВ (6, 7). Фармакодинамическое сравнительное исследование кангрелора и абциксимаба (блокатора гликопротеиновых IIb/IIIa рецепторов тромбоцитов, широко используемого при ЧКВ с высоким риском осложнений) у больных, подвергнутых ЧКВ, показало тенденцию к меньшей продолжительности времени кровотечения при использовании кангрелора. Дальнейшее изучение этого препарата происходило в рамках плацебо-контролируемых исследований CHAMPION-PCI (Clinical Trial Comparing Cangrelor to Clopidogrel in Subjects Who Require Percutaneous Coronary Intervention) (8) и CHAMPION-PLATFORM (Clinical Trial Comparing Treatment with Cangrelor (in combination with usual care) to Usual Care, in Subject, who Require Percutaneous Coronary Intervention) (9). Оба исследования были прекращены досрочно из-за низкой вероятности статистически значимой демонстрации преимущества кангрелора перед лечением, обозначенным как стандартное. В первом из них (CHAMPION-PCI) 8877 больных ОКС, планируемых для ЧКВ, были рандомизированы к применению кангрелора (внутривенно с началом за 30 минут до процедуры и продолжением в течение двух часов после ЧКВ и применением после окончания инфузии 600 мг клопидогреля внутрь) и к применению клопидогреля (600 мг внутрь за 30 минут до ЧКВ). Внутрикоронарные вмешательства были выполнены у 8716 больных. Несмотря на тенденцию к меньшей частоте развития второй конечной точки (смерти от всех причин, Q-инфаркта миокарда, реваскуляризации при выявлении ишемии), частота главной конечной точки (смерти от всех причин, все случаи инфаркта миокарда, реваскуляризации при выявлении ишемии) через 48 часов от начала лечения составила 7,1% в группе клопидогреля и 7,5% в группе кангрелора (отношение шансов 1,05, 95% ДИ 0,88-1,24, p = 0,59). В группе кангрелора было больше крупных кровотечений (недостоверно по критериям ACUITY и TIMI), а число угрожающих жизни кровотечений (по критериям GUSTO) было практически одинаковым.
В более обнадеживающем исследовании CHAMPION-PLATFORM 5362 больных, в основном с ОКС без подъемов сегмента ST, ранее не получавших клопидогрел, были рандомизированы к применению кангрелора или плацебо во время выполнения ЧКВ с последующим применением 600 мг клопидогреля у всех больных. Через 48 часов от начала лечения зарегистрирована отчетливая тенденция к снижению частоты главной конечной точки исследования (смерти от всех причин, все случаи инфаркта миокарда, реваскуляризации при выявлении ишемии) – 7% в группе кангрелора и 8% в группе плацебо (отношение шансов 0,87, 95% ДИ 0,71-1,07, p = 0,17) и статистически значимое (трехкратное) снижение риска определенного тромбоза стента и общей смертности. В этом исследовании при использовании кангрелора отмечено существенное увеличение риска крупных кровотечений (критерии ACUITY) и тенденция к большей частоте необходимости в переливании препаратов крови.
Таким образом, оба исследования не выявили преимущества кангрелора на уровне главной конечной точки исследований. По мнению экспертов (10), одной из главных ошибок замысла исследований было применение клопидогреля не перед диагностической ангиографией, а перед или после ЧКВ, а кангрелора не сразу после диагностической ангиографии (в ожидании выбора шунтирующей или внутрисосудистой реваскуляризации), а непосредственно перед или во время ЧКВ. Изменение замысла позволило бы оценить вклад быстрого прекращения антитромбоцитарного действия препарата в снижение геморрагического риска в случае отказа от ЧКВ. Кроме того, критике подвергнута и продолжительность введения препарата. Высказано предположение, что более эффективной могла оказаться более продолжительная инфузия кангрелора с постепенным снижением дозы. Тем не менее, в свете появления тикагрелора и его успехов, большая часть преимуществ кангрелора выглядит малоубедительной и будущее этого препарата оценивается скептически (10).
Заключение
Результаты крупных исследований в области антитромботической терапии, представленные в 2009 году, демонстрируют прежде всего возможности по дальнейшему совершенствованию этой важной части лечения кардиологических больных. Наступление на стандартные средства, составляющие существующий арсенал антитромботических средств, оказалось успешным как в случае с длительной антикоагулянтной терапией при мерцательной аритмии (исследование RE-LY), так и в случае с улучшением эффективности и безопасности лечения, направленного на подавление активности тромбоцитов у больных ОКС (в основном подвергаемых раннему инвазивному лечению) (исследование PLATO). Для лекарств, представляющих действующие стандарты лечения, например аспирина и клопидогреля, также существуют возможности по улучшению их эффективности, что в какой-то мере продемонстрировано в результатах исследования CURRENT-OASIS-7. Для окончательного представления о возможностях использования новых средств для лечения больных остается дождаться информации об их стоимости, а также официальных одобрения и регистрации.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.