Дисфункция крестцово-подвздошного сочленения
- Аннотация
- Статья
- Ссылки
- English
В настоящее время для классификации боли в спине принята диагностическая триада, согласно которой выделяют боли:
- связанные с серьезной патологией (опухоли, травмы, инфекции и др.);
- вызванные компрессионной радикулопатией;
- неспецифические (скелетно-мышечные) [1–3].
В ряде исследований отмечается, что последняя группа характеризуется высокой гетерогенностью, что определяет необходимость индивидуализированного и дифференцированного подхода к ведению пациентов с такими болями [4–7].
При выявлении источников неспецифической боли в спине с помощью диагностических блокад было установлено, что в 25–42% случаев боли носили дискогенный характер, в 18–45% – фасеточный, в 10–30% боль была локализована в крестцово-подвздошном сочленении (КПС). Дискогенные боли чаще наблюдались у пациентов более молодого возраста и у мужчин. В старших возрастных группах преобладали фасеточный болевой синдром и патология КПС. Фасеточный синдром отмечался, как правило, у женщин с повышенным индексом массы тела, в то время как синдром КПС – у женщин с пониженным индексом массы тела [8, 9].
По строению КПС представляет собой частично типичный синовиальный сустав (в передних отделах), а частично – неподвижный хрящевой синостоз. Существует значительная индивидуальная изменчивость в отношении формы и размеров. Крестцовая и подвздошная поверхности сустава покрыты гиалиновым и волокнистым хрящом соответственно и имеют неровную структуру, вероятно, вследствие физиологической адаптации к нагрузке.
Основная функция КПС – опорная: поддержка верхней части тела и уменьшение нагрузки при ходьбе. Объем движений в КПС ограничен, оно хорошо укреплено связками: передней и задней крестцово-подвздошными, крестцово-остистой, крестцово-бугорной и межостистой. Связки предотвращают разъединение сустава и ограничивают движение таза вокруг различных осей крестца. КПС взаимодействует с мышцами и фасциями, например, грудопоясничной фасцией, большой ягодичной, грушевидной мышцами и широчайшей мышцей спины [10]. По мнению W. King и соавт. (2015), предпочтительнее говорить не о КПС, а о крестцово-подвздошном комплексе, который включает и собственно сустав, и поддерживающие его связки, при этом каждый из элементов может быть причиной боли [11].
Особенности иннервации КПС
По данным иммуногистохимических исследований, ноцицепторы расположены во всей суставной капсуле, связках и в меньшей степени в субхондральной кости, поэтому повреждение любой из этих структур может вызвать боль. Характер болевого паттерна был предметом экспериментальных работ с участием бессимптомных добровольцев, у которых проводилось растяжение капсулы и раздражение связок. Задняя поверхность сустава изучена лучше и является основным объектом интервенционных методов лечения (блокады, денервация). Она иннервируется в основном из дорзальных ветвей корешков S1–S3, иногда имеется дополнительная иннервация от корешков L5 и S4. Иннервация вентральной поверхности сустава более сложная, в большинстве исследований описывается участие вентральных ветвей L5–S2 и, возможно, L4, обсуждается иннервация от ветвей верхнего ягодичного и запирательного нервов [10].
Принято выделять внутри- и внесуставные источники боли в области КПС. Среди внутрисуставных причин наиболее часто отмечаются артрозо-артрит и спондилоартропатии, среди внесуставных – повреждения связок и мышц, а также энтезопатии.
Термин дисфункции предполагает дегенеративные изменения КПС в отсутствие специфических факторов поражения (опухолей, переломов, септического или аутоиммунного воспаления и т.п.). Дисфункция КПС, как правило, возникает вследствие комбинации неадекватной осевой нагрузки и вращения и характеризуется изменением подвижности в суставе (например, блокированием сустава или микронестабильностью). Это приводит к несбалансированному распределению нагрузки на окружающие ткани (капсулу, связки, мышцы, кости) [12]. В то же время в исследованиях с применением рентгеновской стереофотометрии не обнаружено связи между объемом движения в суставе и развитием болевого синдрома [13]. Нередко КПС может выступать в качестве зоны отраженных болей при поясничных грыжах диска, заболеваниях органов малого таза.
К болезненной дисфункции КПС предрасполагают следующие факторы:
- возраст (чаще встречается у пожилых лиц и молодых спортсменов);
- асимметрия длины ног;
- аномалии строения, походки и биомеханики, сколиоз;
- длительное напряжение/травмы (например, бег трусцой);
- беременность;
- предшествующие операции на позвоночнике (особенно спондилодез).
В 40–50% случаев развитие боли связано с конкретным провоцирующим фактором, наиболее часто боли в КПС возникают в результате дорожно-транспортных происшествий, падений, после повторяющихся нагрузок и при беременности [14, 15].
Набор массы тела, усиление лордоза, растяжение связок, индуцированное изменением гормонального фона, травмы таза во время родов могут предрасполагать к боли в КПС во время беременности. H.С. Ostgaard и соавт. наблюдали 855 беременных в течение девяти месяцев. Боли в спине испытывали 49%, в большинстве случаев источником являлось КПС [16]. В когортном исследовании из 313 женщин на сроках от 12 до 18 недель беременности 62% (n = 194) жаловались на боли в спине. Среди них 54% испытывали боль в области КПС, 17% описывали преимущественно боли в пояснице, а у остальных 29% наблюдалось сочетание боли в области КПС и поясницы [17].
Разница в длине ног может вызвать боль из-за повышенной нагрузки на сжатие-растяжение КПС [18]. По данным O. Friberg, пациенты с хронической болью в нижней части спины значительно чаще (75 против 43,5%) имеют несоответствие длины ног > 5 мм по сравнению с контрольной группой [19].
После операций на позвоночнике (особенно спондилодеза) меняется биомеханика позвоночника, вследствие чего повышается нагрузка на КПС [20], что приводит к развитию боли у 32–61% пациентов [21, 22].
K. Ha и соавт. сравнили пред- и постоперационные компьютерные томограммы (КТ) 32 больных, перенесших спондилодез на разных уровнях, с результатами обследования 34 пациентов группы контроля. Было отмечено двукратное увеличение дегенерации КПС в группе спондилодеза [23].
Методы диагностики
Клиническая диагностика
Боль носит чаще односторонний латерализованный характер в проекции КПС. Наиболее специфична для поражения КПС зона Fortin размером 3 × 10 см, которая располагается непосредственно книзу от задней верхней подвздошной ости [24].
Дисфункция КПС часто имитирует корешковые поражения. Клинические наблюдения и артрографические исследования с участием здоровых добровольцев показали, что в 94% случаев болевые ощущения иррадиируют в область ягодиц, в 72% – в нижнепоясничную область, у 50% больных отмечается распространение боли по задненаружной поверхности бедра, включая 28% с иррадиацией болей ниже колена и 12% с иррадиацией до стопы. У 14% пациентов боль затрагивает паховую область, у 6% – верхние отделы поясничной области, у 2% – живот [24, 25].
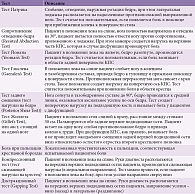
Боли усиливаются при вставании из положения сидя, наклонах, длительном сидении или стоянии. В блокированном КПС нарушается подвижность подвздошной кости относительно крестца. Это проверяется попеременным надавливанием на крестец и подвздошную кость у пациента, лежащего на животе. Характерна болезненность при пальпации КПС с воспроизведением типичного паттерна боли. Отсутствует опускание задней верхней ости при подъеме ноги в положении стоя на стороне блока КПС. Симптомов выпадения не наблюдается, болевые ощущения усиливаются в трех или более провокационных тестах на сжатие или растяжение этого сустава (таблица) [12, 26].
Отношение к применению провокационных тестов в диагностике дисфункции КПС неоднозначно. P. Dreyfuss и соавт. отмечали ненадежность таких критериев, как история болезни и результаты диагностических тестов, для диагностики боли в КПС, подтвержденной положительным ответом на блокаду в качестве эталонного стандарта [27]. По данным C.W. Slipman и соавт., положительная прогностическая ценность ответа на однократную блокаду КПС у 50 больных, отобранных на основе трех и более провокационных тестов, составила 60%. Авторы заключили, что провокационные тесты не должны быть единственным критерием для постановки диагноза [28].
По мнению других исследователей, применение батареи провокационных тестов может быть полезным для выявления боли в КПС. По результатам слепого исследования (n = 48) M. Laslett и соавт., три положительных теста из шести провокационных характеризовались 94%-ной чувствительностью и 78-ной специфичностью [29]. Чуть ниже результаты были получены P. van der Wurff и соавт. (n = 60): чувствительность и специфичность трех положительных из пяти провокационных тестов составили 85 и 79% соответственно. В обоих исследованиях в качестве диагностического стандарта использовалась диагностическая блокада [30]. N.A. Broadhurst и M.J. Bond провели двойное слепое плацебоконтролируемое исследование и продемонстрировали, что тест Патрика, тест заднего смещения и тест сопротивления отведению бедра имели чувствительность в диапазоне от 77 до 87%, при 100%-ной специфичности каждого [31].
В настоящее время для оценки информативности тестов в диагностике заболевания применяется коэффициент отношения правдоподобия (Likelihood Ratios). В систематическом обзоре K.M. Szadek и соавт. пришли к выводу, что три положительных провокационных теста имели значимую диагностическую ценность (отношение шансов 17,16) для подтверждения боли в КПС (в качестве эталонного стандарта использовалась двойная положительная блокада) [32].
Таким образом, нельзя охарактеризовать единичные тесты как достаточно объективные и достоверные [26, 27, 30]. Однако если в результате множественного тестирования три теста из пяти провокационных положительны, можно говорить о достаточной чувствительности и специфичности результатов и высокой вероятности того, что пациенты будут иметь положительный ответ на диагностические блокады КПС [32–34]. Когда все провокационные тесты не дают положительного результата, рекомендуется исключить КПС из предполагаемых причин боли в нижней части спины.
Стандартом для установления диагноза остаются блокады с введением малых объемов местных анестетиков. Подтверждением патологии КПС в развитии боли служит ее исчезновение или существенное уменьшение после блокады сустава растворами местных анестетиков под рентгенологическим или ультразвуковым контролем [34, 35]. Блокады без контроля связаны с высокой частотой ложноположительных ответов, а использование контролируемых блокад повышает вероятность ложноотрицательных результатов, но не влияет на результаты последующего лечения.
Инструментальная диагностика
Радиологическое исследование не имеет диагностической значимости и показано только при наличии «красных флажков».
КТ – быстрое исследование, золотой стандарт для выявления костной патологии. В ретроспективном исследовании с участием 112 пациентов (62 из которых имели подтвержденную блокадами боль в КПС) КТ показала 57,5%-ную чувствительность и 69%-ную специфичность (при использовании диагностических блокад в качестве стандарта) [36].
Радионуклидое сканирование костей также сравнивалось с блокадами анестетиками. C. Slipman и соавт. установили 100%-ную специфичность, но только 13%-ную чувствительность для радионуклидного исследования (участвовали 50 больных, перенесших диагностические блокады КПС) [37]. В то время как J. Maignе и соавт. сообщили о 46,1%-ной чувствительности и 89,5%-ной специфичности в когорте из 32 пациентов [38]. Низкие значения чувствительности не позволяют рекомендовать радионуклидные методы исследования для скрининга боли в КПС.
Сообщается, что магнитно-резонансная томография (МРТ) эффективна в обнаружении спондилоартропатий уже на ранней стадии с чувствительностью, превышающей 90%, но не приносит пользы при диагностике невоспалительных состояний [39].
Дифференциальная диагностика
При возникновении боли в проекции КПС требуется проведение дифференциальной диагностики с целым рядом заболеваний. Специфическими причинами стойкого болевого синдрома могут быть переломы, спондилоартропатии, метастазы, инфекции.
Стрессовый перелом костей таза, спондилолиз, спондилолистез чаще наблюдаются у молодых спортсменов. Для этих состояний характерно усиление боли при разгибании поясницы и ослабление при наклоне вперед, возможна иррадиация в ягодицу или по задней поверхности бедра. Провокационная проба – пациент прогибается назад, стоя на одной ноге, при спондилолизе отмечается усиление боли на стороне поражения. Боль воспроизводится при пальпации позвоночных структур на стороне поражения. Подтверждается нейровизуализацией (лучше КТ).
Дебют спондилоартропатий, как правило, приходится на возраст до 45 лет. Отмечается утренняя скованность более 30 минут, усиление боли во второй половине ночи, миграция ее из одной ягодицы в другую, уменьшение симптомов после разминки. При лабораторном исследовании возможно определение повышенного С-реактивного белка, носительство гена HLA-B27. Рентгенологически – расширение КПС, эрозии, участки склероза и анкилоза, при МРТ – признаки воспаления.
О метастатическом поражении следует задуматься при наличии у пациента онкологического заболевания в анамнезе, отягощенной наследственности, появлении необъяснимой усталости, потери массы тела. Для подтверждения диагноза существенное значение имеют данные нейровизуализации и лабораторных исследований.
На инфекционное поражение указывают стойкие, плохо купируемые боли, лихорадка, лейкоцитоз, повышение скорости оседания эритроцитов, сопутствующая инфекция, инвазивные процедуры в анамнезе, снижение иммунитета, а также соответствующие нейровизуализационные изменения.
В круг дифференциальной диагностики входит также пояснично-крестцовая радикулопатия. Для нее характерны онемение или парестезии в соответствующих дерматомах, парезы в «индикаторных» мышцах, симптомы выпадения и натяжения, а также односторонняя простреливающая боль. При этом боль выражена в конечности больше, чем в спине, усиливается при движении, кашле, иррадиирует до дистальных отделов. На МРТ обнаруживается грыжа диска с компрессией корешка.
От дисфункции КПС следует отличать поражение других скелетно-мышечных структур: фасеточных суставов, грушевидной мышцы, аксиальные дискогенные боли.
Фасеточный синдром развивается чаще после 40 лет. Это боль паравертебральной локализации, односторонняя или двусторонняя, может иррадиировать в ногу, до уровня колена, усиливается при значительном разгибании и уменьшается при сгибании. Возникает после эпизодов длительной неподвижности и уменьшается при движении. Не характерны симптомы натяжения и выпадения (двигательные, чувствительные расстройства, изменение рефлексов, тазовые нарушения). Положительный тест Кемпа – переразгибание позвоночника или сочетание разгибания с ротацией обычно приводит к провокации боли, исходящей из фасеточных суставов. Усиление боли при глубокой пальпации в проекции фасеточных суставов. Подтверждается проведением диагностической блокады под рентгенологическим контролем.
При синдроме грушевидной мышцы боль из ягодичной области распространяется по ходу седалищного нерва, типичны парестезии в стопе. Боль усиливается после сидения и при начале ходьбы. Болезненна абдукция согнутого бедра и ограничена его внутренняя ротация, при которых происходит растяжение и сокращение заинтересованной мышцы соответственно (проба Бонне – Бобровниковой). Объем движений в поясничном отделе позвоночника не изменен. Поднятие прямой ноги ограничено. Поясничные аксиальные дискогенные боли сопровождаются феноменом централизации McКenzie: боль по средней линии, провоцируется сгибанием. Боли ощущаются как глубинные, усиливаются при интенсивном надавливании и перкуссии соответствующего сегмента в положении лежа на животе. Боль усиливается при кашле, чихании, пробе Вальсальвы. При МРТ выявляется грыжа диска с возможными в ней трещинами, изменения субхондральных отделов позвонков по типу Модик 1, 2.
Лечение
Лечение боли, обусловленной дисфункцией КПС, проводят в соответствии с европейскими и североамериканскими руководствами по лечению острых и хронических неспецифических болей в спине [1, 2, 40, 41].
Важно проинформировать пациента о причинах заболевания, эффективных методах лечения и высокой вероятности быстрого разрешения боли. Показана ранняя активизация больных с поддержанием уровня повседневной активности. Следует избегать необоснованной нейровизуализации или других параклинических исследований. Необходимо оценить выраженность боли и неврологического дефицита на начальном этапе терапии, потенциальный успех и риски.
Медикаментозное лечение проводится препаратами с доказанным эффектом и с учетом возможного побочного действия. Оно включает короткий курс нестероидных противовоспалительных средств, трамадол при интенсивных болях, применение местных средств: пластыря с лидокаином, мазей с нестероидными противовоспалительными средствами [42].
По результатам метаанализа 86 исследований (n = 10 160), проведенного R.A. Мооrе и соавт. [43], локальные нестероидные противовоспалительные средства значимо превосходят плацебо по эффективности.
В ряде работ были продемонстрированы возможности применения местной формы ибупрофена при боли в суставах.
В пилотном проспективном рандомизированном исследовании R.L. Tiso и соавт. установили сходную клиническую эффективность местной и пероральной форм ибупрофена при хронической боли в коленных суставах [44].
Эффективность и переносимость крема Долгит® (ибупрофен 5%) при остеоартрозе (76 пациентов в возрасте от 42 лет до 81 года) изучались в российском многоцентровом двухнедельном исследовании [45]. Эффективность оценивалась по снижению интенсивности боли в покое и при движении, а также изменению местного суставного индекса. В конце исследования было отмечено достоверное снижение всех количественных показателей суставного синдрома, при этом уменьшение боли в суставах как значительное расценили 70% пациентов. Нежелательные аллергические кожные реакции наблюдались только у троих пациентов и прошли после отмены терапии, не потребовав специфического лечения.
По данным исследования К. Trnavský, эффективность и безопасность ибупрофена (крем Долгит®) при лечении артроза коленных суставов были статистически и клинически значимыми по сравнению с плацебо [46].
В 2008 г. в Словакии были изучены эффективность и безопасность применения крема Долгит® у 28 пациентов с артрозом коленных суставов. На фоне трехнедельной терапии наблюдалось достоверное уменьшение интенсивности боли, увеличение объема движений в коленном суставе, пациентам стало легче ходить по ступенькам. Из побочных эффектов была отмечена только временная легкая гиперемия кожи в двух случаях [47].
Интервенционные методы лечения включают блокады с введением кортикостероидов и местных анестетиков и радиочастотную деструкцию.
Показания к проведению блокад:
- отсутствие результатов традиционной консервативной терапии;
- побочные эффекты системного лечения;
- желание пациента;
- усиление боли.
Как внутри-, так и внесуставное введение стероидов может обеспечить кратковременное облегчение в подгруппе пациентов с активным воспалением, но длительный эффект остается недоказанным. В систематическом обзоре D. Kennedy и соавт. (2015) оценивали эффективность лечения дисфункции КПС методом блокад под рентгенологическим контролем. Было проанализировано 50 работ, отобрано два рандомизированных плацебоконтролируемых исследования и одно крупное обсервационное. Сделан вывод об эффективности блокад в лечении синдрома КПС (уровень доказательности В) [48].
В других исследованиях была продемонстрирована эффективность как интра-, так и периартикулярных блокад [10]. По результатам обзора L. Manchikanti и соавт. (2013), в лечении дисфункции КПС эффективны внутрисуставные и периартикулярные блокады (уровень С), а также радиочастотная деструкция с охлаждаемым электродом (уровень В) [49].
У пациентов со значительным, но кратковременным облегчением боли с помощью блокад в КПС радиочастотная абляция нижнепоясничных дорзальных ветвей и латеральных ветвей S1–S3 (4) может обеспечить облегчение боли продолжительностью до года. Денервация – это малоинвазивное оперативное вмешательство, позволяющее осуществить деструкцию нервных окончаний с целью быстрого уменьшения болевого синдрома. Радиочастотная денервация основана на принципе термокоагуляции. Метод применяется уже много лет, он зарекомендовал себя как высокоэффективный, имеет широкий спектр показаний, практически лишен осложнений. Высокочастотная невротомия проводится в стерильных условиях под рентгенологическим контролем или КТ. Радиочастотная денервация осуществляется через микропрокол с минимальной травматизацией прилегающих и обрабатываемых тканей.
В научно обоснованном руководстве по применению инвазивных методик лечения болей в спине отмечено, что блокады с глюкокортикоидами могут быть рекомендованы при неэффективности консервативной терапии при дисфункции КПС. Радиочастотная деструкция проводится при неэффективности блокад с глюкокортикостероидами [7].
Если пациенты не отвечают на стартовую терапию, можно задействовать немедикаментозные методы с доказанной эффективностью. При острых болях – мануальную терапию, при подострой и хронической – интенсивную мультидисциплинарную реабилитацию, гимнастику, иглоукалывание, массаж, занятия йогой, когнитивно-поведенческую терапию, коррекцию асимметрии ног с помощью ортопедических стелек.
Полезна гимнастика, особенно если она направлена на укрепление мышц, приводящих бедро, включая упражнения лежа на боку, упражнения на сопротивление и поддержание равновесия.
При неэффективности консервативной терапии и малоинвазивных методов лечения обсуждается возможность операций на КПС с использованием стабилизирующих систем [50–53].
A.I. Isaykin, M.A. Ivanova, A.V. Kavelina, G.Ye. Shevtsova
I.M. Sechenov First Moscow State Medical University
Contact person: Aleksey Ivanovich Isaykin, alexisa68@mail.ru
Dysfunction of the sacroiliac joint (partly – a typical synovial joint, partly – immobile cartilaginous synostosis) underlies up to 30% of nonspecific lumbar pain. A unilateral lumbar pain with no signs of radiculopathy is observed during examination. Pain in the sacroiliac joint may be highly accurately diagnosed by using three or more positive provocation tests, but X-ray controlled diagnostic blockade is a reference standard method to identify painful joints. Treatment is started in accordance with general protocol provided by International guidelines on management of acute and chronic nonspecific back pain. A combination approach including medicines and non-medicated methods should be preferred. Use of local nonsteroidal anti-inflammatory drugs (ibuprofen, Dolgit®) is discussed.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.