Эксенатид – новый препарат для лечения пациентов с сахарным диабетом 2 типа с возможными положительными эффектами на сердечно-сосудистую систему
- Аннотация
- Статья
- Ссылки


Сахарный диабет является постоянно прогрессирующим заболеванием, при котором:
-
дисфункция β-клеток вначале приводит к нарушению глюкозотолерантности, которое у некоторых индивидуумов далее прогрессирует в сахарный диабет 2 типа;
-
дисфункция β-клеток начинается задолго до повышения показателей гликемии и ухудшается после манифестации сахарного диабета.
Механизмы, ответственные за изменения уровней инсулина:
-
нормальная адаптация β-клеток к инсулинорезистентности способствует увеличению секреции инсулина каждой клеткой и увеличению массы
β-клеток; -
нарушенная адаптация β-клеток при сахарном диабете 2 типа развивается в результате снижения секреции инсулина из каждой клетки и уменьшения массы β-клеток
Таким образом, одной из основных задач при лечении сахарного диабета 2 типа является сохранение или замедление утраты функции β-клеток.
Инсулинотерапия всегда считалась и считается до настоящего времени методом выбора терапии у этой группы пациентов, когда диетотерапия, физические упражнения и терапия пероральными сахароснижающими препаратами более не могут поддерживать нормальные показатели сахара в крови. В настоящее время считается, что более раннее назначение инсулина способствует сохранению и замедлению утраты функции и массы
b-клеток. Инсулинотерапию обычно начинают с назначения инсулинов или инсулиновых аналогов длительного действия или с назначения готовых инсулиновых смесей, содержащих как базальный, так и короткодействующий инсулиновые компоненты (6, 7, 8). Однако интенсификация инсулинотерапии часто сопровождается набором веса и увеличением частоты встречаемости гипогликемических состояний, представляющих собой известные барьеры для улучшения гликемического контроля (9, 10). Так, примерно у 60-90% пациентов с сахарным диабетом 2 типа ко времени установления диагноза имеется избыточный вес или ожирение. Большинство вариантов сахароснижающей терапии, за исключением бигуанида, метформина гидрохлорида, приводят к увеличению веса. Таким образом, избыточный вес приводит к увеличению риска развития сердечно-сосудистых заболеваний и одновременно является препятствием для эффективной терапии сахарного диабета.
Эксенатид является первым препаратом из класса миметиков инкретина, который рекомендован для комбинированного назначения с метформином или препаратами сульфонилмочевины, но никогда ранее не рекомендовался в качестве средства замещения инсулинотерапии у пациентов с сахарным диабетом 2 типа, которым показана инсулинотерапия. Важно, что механизм действия эксенатида значительно отличается от механизма действия инсулина. Эксенатид стимулирует секрецию эндогенного инсулина по глюкозозависимому механизму, подавляет секрецию глюкагона, замедляет опорожнение желудка и снижает потребление пищи (11, 12). Исследования с включением (13, 14) пациентов, которые не могут поддерживать удовлетворительные показатели гликемии на терапии пероральными сахароснижающими препаратами, показали, что возможно достигать аналогичных показателей улучшения контроля гликемии при оценке по уровню HbA1c при назначении как эксенатида, так и инсулина. Назначение эксенатида также способствует снижению постпрандиальной гликемии и гликемии натощак, но, в отличие от инсулинотерапии, ассоциируется со снижением веса тела. Однако в настоящее время очень мало данных в поддержку возможного замещения инсулина эксенатидом у пациентов с сахарным диабетом 2 типа
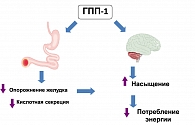
(15, 16, 17). На рисунке 1 (адаптировано из Keffer et al, J Clin Invest, 1998, 101:515-20) представлено два основных эффекта ГПП-1 на желудочно-кишечный тракт и ЦНС.
На основании данных преклинических и клинических исследований, при назначении эксенатида были получены следующие результаты. При исследованиях животных отмечалось снижение веса у крыс, карликовых свиней и макак-резусов. По данным клинических исследований, у пациентов с сахарным диабетом 2 типа отмечалось снижение показателей гликемии и веса, при этом снижение веса было дозозависимым. Влияние терапии эксенатидом на вес пациентов является неоспоримым преимуществом терапии. Возникали вопросы о том, что снижение веса у пациентов может быть обусловлено развитием осложнений со стороны желудочно-кишечного тракта, но впоследствии было показано, что назначение эксенатида приводило к снижению веса вне зависимости от развития побочных эффектов.
Обзор исследований эксенатида по материалам Европейского конгресса по изучению сахарного диабета, который был проведен в Амстердаме
18-21 сентября 2007 года.
В последнее время появилось много новых данных о терапии эксенатидом, часть из которых была описана на последнем Европейском конгрессе по изучению сахарного диабета и которые будут приведены ниже. Okerson T. и коллеги (18) привели данные о влиянии эксенатида на маркеры печеночной функции в течение 3 лет у пациентов с сахарным диабетом 2 типа. Авторы сделали вывод о том, что у пациентов с сахарным диабетом
2 типа, которым проводилась терапия эксенатидом, отмечалось улучшение биохимических показателей печеночной функции с одновременным снижением показателей HbA1c и веса. Авторы предлагают проведение последующих исследований о возможности улучшения течения жирового гепатоза не алкогольного происхождения. Также Gedulin B. и коллеги (19) проводили сравнительное исследование по эффектам ситаглиптина и эксенатида на потребление пищи, вес тела, глюкозозависимую секрецию инсулина и опорожнение желудка у грызунов. Были получены данные о более выраженной in vivo эффективности эксенатида по сравнению с ситаглиптином по эффектам некоторых физиологических параметров, вносящих вклад в улучшение глюкорегуляции. D. Parkes и коллеги (20) впервые получили данные о длительном антигипертензивном эффекте эксенатида на примере модели глюкокортикоид-индуцированного метаболического синдрома без влияния на потребление пищи или вес тела. Высказывались различные предположения о возможных механизмах действия эксенатида, один из которых был предположен Ionut V. (21), и заключался в гормонально независимой гликемии, обусловленной панкреатическим эффектом посредством эффектов на рецепторы ГПП-1 в портальной системе печени. Активация этих портальных рецепторов посредством нейтрального механизма может увеличить клиренс глюкозы вне зависимости от островковых гормонов. Работа MacConell L. и коллег (22) была посвящена оценке фармакокинетики и фармакодинамики эксенатида с механизмом длительного высвобождения препарата после однократного и многократного дозирования. Авторы сделали вывод о том, что фармакокинетика препарата при однократном введении предопределяла фармакокинетику еженедельной дозы. Недельная доза эксенатида при еженедельном введении с поддержанием терапевтических доз препарата в крови хорошо переносилась. Дозозависимые эффекты на постпрандиальные показатели гликемии и вес тела, но не на показатели гликемии натощак, свидетельствуют о дифференцированных взаимосвязях дозы и ответной реакции при оценке фармакологии эксенатида. Эти данные показывают, что эксенатид с пролонгированным механизмом высвобождения (Exenatide LAR) обеспечивает адекватную концентрацию в кровотоке с сохранением основного фармакодинамического действия эксенатида.
По данным ряда клинических исследований, было показано, что монотерапия эксенатидом приводит к снижению веса и когда добавляется к терапии сахароснижающей терапии метформином, препаратами сульфонилмочевины и тиазолидиндионами (24-26). Наибольшее снижение веса отмечалось при дополнительном назначении эксенатида к терапии метформином. Данные двухлетних открытых исследований с продлением времени терапии показали, что снижение веса, достигаемое при терапии эксенатидом, сохраняется, и вес продолжает снижаться, что приводит к улучшению показателей риска со стороны сердечно-сосудистой системы (27).
Побочные эффекты и безопасность терапии эксенатидом
При терапии эксенатидом отмечалась умеренная тошнота (33,2%) и рвота (15%). Частота встречаемости побочных эффектов со стороны желудочно-кишечного тракта в группе терапии эксенатидом была выше по сравнению с группой терапии инсулином аспарт. Средние уровни частоты встречаемости побочных эффектов были аналогичными между группами терапии. Одним из преимуществ эксенатида при терапии пациентов с сахарным диабетом
2 типа является улучшение показателей контроля гликемии без сопутствующего развития гипогликемических состояний. По данным других авторов (28), терапия эксенатидом хорошо переносилась и не было выявлено тяжелых побочных эффектов, за исключением единственного случая развития тяжелой гипогликемии на фоне комбинированной терапии препаратами сульфонилмочевины и метформином. Наиболее часто встречавшимся побочным эффектом также была тошнота (45-51%). Частота тошноты была наибольшей, когда доза эксенатида титровалась от 5 до 10 mг в фазы инициации исследований, начиная от четвертой до восьмой недели при 30-недельных плацебо-контролируемых исследованиях. Частота встречаемости тошноты снижалась у пациентов по мере удлинения времени терапии эксенатидом. Эпизоды гипогликемии в этих исследованиях были обычно от легких до умеренных по своей интенсивности. Не отмечалось повышения частоты встречаемости гипогликемий у пациентов на терапии эксенатидом в сочетании с метформином. Однако частота гипогликемий возрастала, когда одновременно назначали препараты сульфонилмочевины. В одном из трех плацебо-контролируемых исследований III фазы было отмечено, что снижение дозы препаратов сульфонилмочевины снижало частоту гипогликемий у пациентов, находившихся на терапии эксенатидом (26). В дополнение к вышеизложенному, данные аналогичного исследования показали, что исходный уровень HbA1c близкий к 7%, ассоциировался с более высокой частотой встречаемости гипогликемий. Низкие титры антител к эксенатиду и в некоторых случаях высокие титры антител к эксенатиду были выявлены у некоторых пациентов при терапии эксенатидом. Тем не менее, присутствие этих антител не обладало предопределяющим эффектом на показатели гликемического контроля или на частоту встречаемости побочных эффектов (29). Влияние терапии эксенатидом на вес пациентов также является неоспоримым преимуществом терапии. Возникали вопросы о том, что снижение веса у пациентов может быть обусловлено развитием осложнений со стороны желудочно-кишечного тракта, но впоследствии было показано, что назначение эксенатида приводило к снижению веса вне зависимости от развития побочных эффектов.
Терапевтический потенциал при сахарном диабете 2 типа
В рисунке 2 приводятся основные эффекты эксенатида при сахарном диабете 2 типа.
Также инкретины, включая эксенатид, обладают потенциальными положительными эффектами на сердечно-сосудистую систему. Эти эффекты обусловлены рядом важных факторов и приводятся ниже (по данным доклада Holst JJ на заседании EASD 2007 в Амстердаме):
1) рецепторы к ГПП-1 есть в сердце;
2) у мышей с нокаутированным рецептором ГПП-1 нарушена сократимость левого желудочка и отмечается нарушение диастолической функции;
3) антигипертензивные эффекты ГПП-1 были выявлены у крыс Dahl c повышенной солевой чувствительностью;
4) ГПП-1 улучшает кардиальную функцию у собак с сердечной недостаточностью;
5) ГПП-1 защищает миокард крыс от ишемического/реперфузионного повреждения (а.и. является средством профилактики);
6) назначение ГПП-1 пациентам с острым инфарктом миокарда и фракцией выброса левого желудочка (ФВЛЖ) равной 29% после ангиопластики улучшало ФВЛЖ до 39%;
7) ГПП-1 улучшает эндотелиальную дисфункцию у пациентов с СД 2 типа с ишемической болезнью сердца.
Заключение
Внедрение в клиническую практику эксенатида дает клиницистам уникальное средство лечения популяций пациентов с недостаточным контролем гликемии. По современным оценкам только 36% пациентов достигают целевых показателей гликемии и гликированного гемоглобина. Помимо этого, приверженность терапии ограничивается развитием нежелательных побочных эффектов, таких как: увеличение веса и гипогликемии при терапии препаратами сульфонилмочевины и инсулинотерапии, нарушения со стороны желудочно-кишечного тракта при терапии метформином и увеличение веса и периферические отеки при терапии тиазолидиндионами. С учетом этих эффектов, такие свойства эксенатида как влияние на постпрандиальную гипергликемию и показатель гликированного гемоглобина, а также отсутствие гипогликемий с одновременным снижением веса, приобретают большое значение в клинической практике. Можно также отметить, что терапия с дополнительным назначением миметиков инкретина для лечения сахарного диабета 2 типа является клинически оправданной и эффективной и обычно хорошо переносится пациентами. Миметики инкретинов становятся все более заметными в качестве средства эффективного улучшения контроля гликемии. К явным преимуществам такой терапии можно отнести улучшение показателей контроля гликемии, веса, функции b-клеток и снижение риска осложнений, обусловленных сахарным диабетом. Несомненно, что все эти преимущества будут активно изучаться в последующие годы, наряду с возможными отрицательными эффектами и осложнениями терапии.
В заключение хотелось бы сказать несколько слов о новой форме эксенатида продленного действия, которая может вводиться пациентам один раз в неделю. На рисунке 3 представлена схема технологии длительного высвобождения препарата, позволяющая применять его один раз в неделю с сохранением всех положительных свойств препарата, данные об этом уже приводились в этой статье ранее.
Также считаем необходимым привести доводы известного профессора D. Matthews – одного из вдохновителей и главных исследователей UKPDS, которые были представлены в ходе его дебатов на EASD-2007 в Амстердаме по поводу того, смогут ли новые препараты – миметики инкретинов и ингибиторы ДПП-4 – заменить терапию другими препаратами при сахарном диабете 2 типа и согласимся с тем, что на данном этапе дополнительное назначение новых препаратов к проверенным старым препаратам лучше полного их замещения. Приведем доводы профессора D. Matthews без комментариев с нашей стороны:
-
не было проведено долговременных исследований по изучению эффектов препаратов;
-
не было исследований по изучению сердечно-сосудистых клинических исходов такой терапии;
-
снижение веса при терапии – это хороший эффект в краткосрочной перспективе, но как обстоит дело в долгосрочной перспективе у этой группы пациентов – недостаточно известно;
-
сахарный диабет 2 типа – гетерогенное заболевание и в ряде случаев пациентам показаны только препараты сульфонилмочевины.
Также добавим, что в свете новых работ по успешному сочетанию с инсулинотерапией и по возможности замещения инсулина на эксенатид, можно рассматривать достаточно перспективной возможность постепенного замещения инсулина на эксенатид у ряда пациентов с неадекватным контролем сахарного диабета 2 типа, находящихся на терапии пероральными сахароснижающими препаратами (23).
Таким образом, можно сказать, что необходимо проведение исследований по длительному изучению эффективности и безопасности препаратов, и в то же время в последние 10 лет прогресс в изучении сахарного диабета и создание новых, перспективных препаратов дают врачам и пациентам много прекрасных надежд на будущее.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.