Эпидемия ожирения – время активных действий
- Аннотация
- Статья
- Ссылки


Самое печальное, что в настоящее время стремительно растет число детей и подростков, страдающих ожирением. Сегодня в развитых странах до 25% подростков имеют избыточную массу тела, а 15% – страдают ожирением (3, 11). Нельзя не отметить, что в таких странах на долю СД типа 2 в детском и подростковом возрасте приходится 10% и более случаев всех форм СД (1). Избыточный вес в детстве – значимый предиктор ожирения у взрослых: 50% детей, которые имели избыточный вес в 6 лет, становятся взрослыми с ожирением; в подростковом возрасте эта вероятность увеличивается до 80%.
Статистика неутешительна: средняя продолжительность жизни больных ожирением на 8-10 лет меньше, чем у людей с нормальной массой тела (14, 20, 24). Так, увеличение массы тела всего лишь на 0,4 кг увеличивает риск смерти на 2% у лиц в возрасте 50-62 лет.
К сожалению, не только пациенты, но и некоторые врачи не считают ожирение серьезным заболеванием. Ожирение – это хроническое заболевание и фон для развития атеросклероза и его клинических проявлений, артериальной гипертензии, сахарного диабета, заболеваний желудочно-кишечного тракта и опорно-двигательного аппарата, онкологических и ряда других заболеваний (12). Так, вероятность развития артериальной гипертензии (АГ) у лиц с избыточной массой тела на 50% выше, чем у лиц с нормальной массой тела (16). В возрасте старше 18 лет повышение массы тела на 1,0 кг увеличивает риск развития артериальной гипертензии на 5%, а прибавка 8,0-10,9 кг – в 1,6 раз увеличивает риск сердечно-сосудистых заболеваний (19). Высока и частота гипертрофии миокарда левого желудочка, составляющая 29,9% у лиц с ожирением, в отличие от 5% у лиц с нормальной массой тела (9). Среди больных ожирением у 2/3 развивается СД типа 2, около 90% больных СД типа 2 имеют избыточный вес или ожирение (3, 24). Повышенное накопление висцерального жира является основным фактором риска, сопряженным с ожирением патологических состояний. Именно висцеральное ожирение является основным компонентом метаболического синдрома, представляющего собой совокупность гормональных и метаболических нарушений, которые объединяет общий патофизиологический механизм – инсулинорезистентность (ИР). Многочисленные исследования подтвердили, что при одинаковом ИМТ абдоминальное ожирение сопровождается более высоким риском развития сердечно-сосудистых заболеваний, СД типа 2, атеросклероза, чем периферическое ожирение
(3, 14, 24).
Серьезность проблемы ожирения обусловлена и тем, что многие врачи имеют избыточный вес или ожирение, которые обусловлены теми же причинам, что и у их пациентов. Врачи, которые не стремятся к лечению ожирения или потерпели неудачу в его лечении, зачастую и являются теми, кто относится скептически к рекомендациям в отношении необходимости снижения массы тела. Осуществляя лечение заболеваний, причинносвязанных с ожирением (ИБС, АГ, СД, гепатостеатоз и др.), они не всегда настоятельно рекомендуют снижение массы тела. В терапевтическом плане ожирение представляет один из серьезных барьеров не только на пути эффективной профилактики, но и эффективной фармакотерапии большинства хронических заболеваний. Хотя известно, что успешное снижение массы тела позволяет не только уменьшить клинические проявления, но и повысить эффективность терапии этих заболеваний (2, 5, 9). Известно, что снижение массы тела на 5,6 кг уменьшает на 58% риск дальнейшего прогрессирования нарушений углеводного обмена – развития
СД типа 2 у больных с ожирением и нарушением толерантности к глюкозе в пределах 5,0-9,9 кг уменьшает риск развития АГ на 15%, а снижение на 10 кг и более – на 26% (8, 15).
Развитие ожирения обусловлено взаимодействием генетических факторов и факторов внешней среды, включающих переедание, малоподвижный образ жизни, хронические стрессы, недостаток сна (3, 24). Известно более
50 предрасполагающих генов. Ожирение – это хроническое заболевания, результат расстройства энергетического баланса, когда поступление энергии превышает ее расход. В настоящее время одним из ведущих факторов в его патогенезе, несомненно, является избыточное потребление высококалорийной, жирной пищи (рисунок 1).
Основной целью лечения ожирения наряду со снижение массы тела является предотвращение или улучшение течения сопутствующих заболеваний, максимальное снижение риска развития сердечно-сосудистых заболеваний и их осложнений, а также повышение качества жизни пациентов (18, 24). Полноценный успех и долговременные результаты достигаются лишь при проведении комплексной терапии этого хронического заболевания. Рекомендации по модификации образа жизни должны включать индивидуальный расчет диеты, изменение стереотипа питания, повышение физической активности и отказ от вредных привычек. Эффекты изменения образа жизни обычно оценивают через 3 месяца. Согласно современным рекомендациям, минимальное снижение массы тела, позитивно сказывающееся на метаболических расстройствах, составляет 5% от величины исходного веса пациента. Быстрая потеря массы тела, особенно у тучных лиц с сердечно-сосудистыми заболеваниями, может привести к ряду серьезных осложнений, в том числе развитию аритмий (23).
Снижение веса может быть достигнуто при соблюдении низкокалорийной диеты, содержащей не более 25-30% жира от суточной калорийности рациона, в том числе насыщенных жиров – менее 7%, полиненасыщенных – до 10% и мононенасыщенных – менее 20%, холестерина – менее 300 мг, содержание клетчатки должно составлять более
20-25 г/сут. Известно, что питание с высоким содержанием жира вызывает значительное снижение чувствительности органов и тканей к действию инсулина. Насыщенные жирные кислоты, в отличие от моно- и полиненасыщенных кислот, представляют наибольшую опасность в отношении ухудшения чувствительности к инсулину. Рекомендуется употребление соли в умеренных количествах (до 5 г в день), которое положительно сказывается на динамике артериального давления. Помимо рационального питания, снижению массы тела способствует регулярная физическая нагрузка, повышение которой носит индивидуальный характер в зависимости от сопутствующей патологии (4-5 занятий в неделю по 30-45 минут в день при отсутствии клинических признаков ИБС). Повышенная физическая активность может улучшать чувствительность организма к инсулину на 40%. К сожалению, несмотря на доказанную эффективность сочетания низкокалорийного питания и повышенной физической активности, только 20% пациентов, стремящихся снизить массу тела, используют эти лечебные подходы одновременно (3, 17).
Практика показывает, что более чем 90% людей, снизивших массу тела, в течение одного года вновь прибавляют свой вес, а в некоторых случаях масса тела становится даже больше исходной. И лишь 4-5% больных могут достигнуть положительных результатов без дополнительной фармакотерапии (3, 24). Фармакотерапия ожирения проводится, если при модификации образа жизни не удается добиться снижения веса на 5% в течение трех-шести месяцев. Кроме того, если у больного показатель ИМТ≥30 кг/м², или ИМТ≥27 кг/м², но есть факторы сердечно-сосудистого риска, в этом случае, показана медикаментозная терапия. Лечение позволяет не только повысить приверженность пациента к немедикаментозному лечению, но и достигнуть более эффективного снижения массы тела и его поддержания в течение длительного периода (13, 18).
Другой известной проблемой в плане терапевтического подхода к ожирению является то, что тучным людям очень тяжело ограничивать себя в еде (10, 13). Объем желудка у них, как правило, увеличен вследствие постоянного переедания, при этом чувство насыщения они испытывают значительно позднее, чем организм получает необходимый запас энергии.
Кроме того, пациенты, страдающие ожирением, часто заедают стресс, едят «за компанию», испытывая нередко чувство ночного голода, обильно едят в это время.
Современным препаратом для лечения ожирения является препарат Меридиа (сибутрамин), основные фармакологические эффекты которого обусловлены центральным механизмом действия и направлены на модификацию пищевого поведения тучного пациента (2, 4, 17). Фармакологическое действие препарата, являющегося пролекарством, осуществляется за счет активных метаболитов (первичных и вторичных аминов) и состоит в селективном торможении обратного захвата нейромедиаторов серотонина и норадреналина из синоптической щели в ЦНС. Вместе с тем, Меридиа не усиливает секрецию серотонина нейронами ЦНС, поэтому не вызывает лекарственной зависимости, а также не влияет на высвобождение моноаминов. Именно нейромедиатору серотонину отводится основная роль в формировании чувства насыщения (10, 18). Результатом накопления серотонина в межнейрональной щели является усиление и пролонгирование чувства насыщения и, как следствие, постепенное уменьшение объема потребляемой пищи (10, 13). Это один из механизмов действия препарата, способствующий снижению аппетита и формированию правильного пищевого поведения пациента. В целом, как свидетельствуют результаты исследований, 87% пациентов придерживаются сформированного пищевого поведения, выработанного в процессе терапии препаратом Меридиа (4). Наряду с этим, активируя β-3 и β-2 адренорецепторы жировой ткани, препарат стимулирует процессы термогенеза, увеличивает расход энергии организма и тем самым инициирует липолиз (13). Благодаря этому эффекту сибутрамин тормозит снижение скорости метаболических процессов, происходящее на фоне похудения, что имеет большое значение в долгосрочном снижении массы тела и его поддержании (3, 24). Специфический механизм действия позволяет препарату комплексно воздействовать на ведущую причину ожирения, – переедание, в результате снижается количество потребляемой пищи, число дополнительных перекусов, устраняются ночные приемы пищи у тучных пациентов (18). В целом, действуя на обе стороны энергетического обмена, Меридиа способствует не только эффективному снижению массы тела, но и длительному поддержанию достигнутых результатов.
Клиническая эффективность и безопасность препарата Меридиа были продемонстрированы в большом количестве многоцентровых исследований (2, 5, 6). В исследование STORM (Sibutramine Trial on Obesity Reduction and Maintenance), в рамках которого непрерывный прием препарата Меридиа продолжался в течение 2 лет, показан четкий дозозависимый эффект препарата (11). Препарат снизил массу тела более чем на 10% у 70% тучных пациентов, а объем висцерального жира – на 22% от исходной величины, что было доказано при проведении магнитно-резонансной томографии. Следует подчеркнуть, что в отношении снижения массы тела и объема талии, Меридиа был эффективней по сравнению с плацебо соответственно в 3 и 1,9 раза. Показательно и позитивное влияние препарата на нарушения обмена липидов, о чем свидетельствовало повышение на 21% содержания ЛПВП при снижении показателей ЛПНП и триглицеридов (ТГ).
Мета-анализ ряда рандомизированных плацебоконтролируемых исследований, включившим больных с ожирением (ИМТ 30-40 кг/м²) продолжительностью 3-24 месяца, показал, что на фоне приема препарата Меридиа снижение массы тела на 5% и более было отмечено у 19-95% пациентов (7, 8, 15, 17). Снижение массы тела на 10% и более было отмечено
у 19-39% пациентов. В группе плацебо масса тела уменьшилась на 5% и более – у 11-20%, на 10% и более – у 5-7% пациентов. Четко продемонстрировано, что максимальные положительные результаты наблюдаются при длительном курсе терапии. В целом 3 из 5 пациентов, принимавших препарата Меридиа в течение 12 месяцев, достигают потери массы тела более 5% и 3 из 8 – 10% и более. Терапия сибутрамином сопровождается снижением висцеро-абдоминального отложения жира во всех половозрастных группах, о чем свидетельствует уменьшение ОТ (на 8,0-12,51 см) (4, 5, 11).
Следует заметить, что лечение препаратом Меридиа сопровождается позитивными сдвигами в липидном обмене, нарушения которого являются основным маркером МС (11, 18). В исследовании Dujovne C.A. и соавт., продолжавшемся в течение 24 недель и включавшем 332 пациента с избыточной массой тела (ИМТ ≥ 27 кг/м²) и дислипидемией (концентрация ТГ ≥ 250 мг/дл, ЛПВП < 45 мг/дл у женщин, 40 мг/дл у мужчин), наряду с положительной динамикой антропометрических показателей было отмечено значительное снижение уровней ТГ по сравнению с исходным уровнем и группой контроля, наибольших у тех пациентов, которые снизили массу тела более 10% (5). Так, у снизивших массу тела на 5% и 10%, концентрация ТГ уменьшилась на 33,4 и 72,3 мг/дл соответственно. Одновременно возрастала концентрация ЛПВП (на 4,9 мг/дл и 6,7 мг/дл соответственно). В группе плацебо сохранялась атерогенная дислипидемия, о чем свидетельствовало увеличение содержания ТГ (на 31,7 мг/дл) и дальнейшее снижение ЛПВН (на 1,7 мг/дл).
Около 40% тучных больных страдает АГ, поэтому на практике целесообразно знать о наиболее эффективных и безопасных комбинациях сибутрамина с антигипертензивными препаратами. Результаты исследований свидетельствуют,
что у пациентов с ожирением, страдающих АГ, терапия препаратом Меридиа эффективна и безопасна, когда целевые показатели артериального давления (АД) достигаются и поддерживаются приемом как ИАПФ, так и β-адреноблокаторов
(16, 21).
Следует подчеркнуть необходимость длительного поддержания достигнутых результатов после окончания фармакотерапии ожирения. Важным механизмом периферического действия препарата Меридиа является активация скорости метаболических процессов, которая замедляется в процессе снижения массы тела (2, 13). Снижение скорости метаболизма затрудняет дальнейшую эффективную потерю массы тела у пациентов. Так, среди пациентов, ранее получавших лечение препаратом Меридиа, 74% сохранили свой вес на прежнем уровне или в дальнейшем еще снизили массу тела по сравнению с 41% в группе пациентов, принимавших плацебо (1, 4, 11).
Результаты исследования эффективности и переносимости сибутрамина на фоне гипокалорийного питания и увеличения физической активности у больных с МС, проведенного на кафедре эндокринологии и диабетологии МГМСУ, свидетельствуют о высокой эффективности препарата у данной категории больных. В исследование вошли 20 пациентов (13 женщин и 7 мужчин) в возрасте от 18 до 57 лет с ИМТ более 27 кг/м², у которых диагностика МС проводилась согласно рекомендациям комитета экспертов Национальной образовательной программы по холестерину (NCEP АТР III, 2001 г.). Не включались пациенты, имеющие СД, неконтролируемую АГ, булимию, психические и тяжелые соматические заболевания. Как показали данные опроса больных, большинство, включенных в наше исследование, в прошлом имели несколько безуспешных попыток по снижению массы тела (2-3 попытки – 30%, 3 и более – 70% больных). Продолжительность исследования составила 12 недель, в ходе которого у всех пациентов с МС наблюдалось положительная динамика антропометрических показателей.
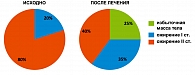
Согласно данным антропометрического исследования на фоне терапии сибутрамином, у всех больных отмечалась положительная динамика показателей антропометрии (массы тела, ИМТ, ОТ, ОТ/ОБ) (рисунок 2). Уменьшение массы тела, наблюдаемое спустя одну неделю от начала лечения, продолжалось в течение всего периода наблюдения.
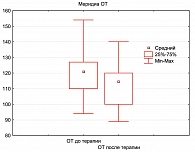
Через 12 недель терапии у всех больных наблюдали снижение масса тела, индивидуальные показатели которого колебались от 2,6 до 15 кг. Среднее снижение массы тела за период лечения составило 12,56% от исходной величины. У большинства больных снижение массы тела достигло клинически значимых величин. К концу исследования 50% пациентов достигли снижения массы тела более 5% от исходной величины. Масса тела у 40% пациентов снизилась на 10% и более от исходной, и только у 10% – менее 5%. Также за период наблюдения ОТ уменьшилась не менее чем на 4 см у 80% больных, у 20% – на 10 см и более по сравнению с исходным показателем (медиана – 6 см) (рисунок 3). Также отмечено уменьшение ОБ.
Среди пациентов, включенных в исследование, у половины сопутствующим заболеванием была контролируемая АГ. В ходе лечения сибутрамином не потребовалось как увеличения суточных доз препаратов, так и схемы гипотензивной терапии, о чем свидетельствовало наблюдение за динамикой АД у больных МС. Кроме того, в течение всего периода лечения, у обследуемых пациентов не отмечалось резких колебаний АД. До лечения медиана и интерквартильный размах показателей систолического АД (САД) и диастолического АД (ДАД) у больных МС составили соответственно 140,0 мм рт. ст. (130,0; 140,0), 132,0 мм рт. ст. (126,0; 134,0). Через 12 недель терапии показатели САД и ДАД достоверно снизились, медиана и интерквартильный размах составили соответственно 132,0 мм рт. ст. (126,0; 134,0) (р=0,026500), 84,0 мм рт. ст. (80,0; 88,0) (р=0,001154). Не было отмечено достоверных изменений частоты сердечных сокращений. Под влиянием препарата снижение массы тела и висцеральной жировой ткани сопровождалось положительной динамикой и ряда других сердечно-сосудистых факторов риска. Так, наблюдались антиатерогенные изменения липидного профиля крови: снизилась концентрация ОХ, ТГ на 16,6% и 17,2% соответственно. Отмечено достоверное снижение содержания ОХ (медиана и интерквартильный размах до лечения 5,9 ммоль/л (4,8; 6,9), через 12 недель – 5,2 ммоль/л (4,1; 6,1) (p=0,003609),
ТГ – 1,83 ммоль/л (1,76; 2,64) до лечения, 1,53 ммоль/л (1,12; 2,13) – через 12 недель; (p = 0,0153). Превышение верхней границы нормального уровня ОХ и ТГ было зарегистрировано соответственно у 35 и 60 % пациентов. До терапии концентрация ЛПВП ниже минимальной границы нормы была выявлена у 30% больных. Через 12 недель терапии обнаруживалось повышение содержания ЛПВП (медиана и интерквартильный размах до лечения – 1,0 ммоль/л (0,9; 1,2), через 12 недель – 1,3 ммоль/л (1,0; 1,4) (p = 0,0433). В соответствии с этим медиана соотношения ТГ/ХС ЛПВП снизилась с 1,59 (1,25; 2,55) исходно до 1,12 (0,80; 1,69) (р=0,0523) через 12 недель терапии сибутрамином. В результате среднее значение атерогенного показателя соотношения ТГ/ХС ЛПВП улучшилось на 35,7%. Максимальное уменьшение степени факторов риска сердечно-сосудистых заболеваний было отмечено у пациентов с МС, которые снизили массу тела более 10%. Исходно у 60% больных имела место бессимптомная гиперурикемия.
Влияние сибутрамина на уровень мочевой кислоты было положительным, хотя не достигло уровня статистической значимости (медиана и интерквартильный размах до лечения – 446,0 (327,4; 535,0), после лечения – 462,0 (403,0; 570,0) (р = 0,121335).
Показатели углеводного обмена также улучшились, о чем свидетельствовало существенное снижение иммунореактивного уровня и инсулина (ИРИ), как базального, так и стимулированного нагрузкой глюкозой (75 г). Так, медиана и интерквартильный размах базального ИРИ до лечения составили 15,0 мкЕД/мл (7,9; 23,3), после лечения – 10,4 мкЕД/мл (6,8; 14,5), различия статистически достоверны, р=0,003609. Медиана и интерквартильный размах стимулированного ИРИ до лечения составили 34,0 мкЕД/мл (16,6; 44,0), после лечения – 25,1 (6,2; 44,0), различия статистически достоверны,
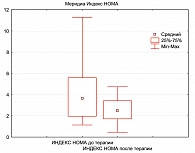
р = 0,04891. Одновременно с этим отмечалось значимое улучшение чувствительности тканей к инсулину. Индекс HOMA IR является одним из информативных показателей, характеризующих степень ИР. Повышение индекса HOMA IR исходно зарегистрировано у 90% больных. Результатом лечения была нормализация чувствительности к инсулину у подавляющего большинства больных МС (85%), о чем свидетельствовала динамика анализируемого показателя (рисунок 4). Так, медиана и интерквартильный размах HOMA IR до лечения составили 3,66 (1,97; 5,59), после лечения – 2,48 (1,72; 3,42), различия статистически достоверны, р = 0,003609.
Анализ данных индивидуального пищевого дневника и мнения пациентов свидетельствует, что регулярный однократный прием сибутрамина позволяет легко и эффективно соблюдать рекомендации врача по низкокалорийному питанию. В практическом плане важно подчеркнуть, что модификация пищевого поведения на фоне терапии сибутрамином, привела к изменению мнения пациентов относительно количества потребляемой пищи. Так, до начала терапии большинство пациентов отмечали, что едят мало и аппетит у них не повышен. В процессе лечения на фоне снижения объема съеденной пищи большинство пациентов переоценили свои пищевые привычки, заметив, что, все-таки до терапии, имея повышенный аппетит, они потребляли большое количество пищи.
Препарат Меридиа в комплексе с диетой и физическими упражнениями предназначен для длительного лечения ожирения. Старт терапии препаратом Меридиа инициируют с начальной дозы 10 мг, принимаемой однократно утром. Он быстро всасывается из желудочно-кишечного тракта не менее чем на 77% (1, 3). Активные метаболиты препарата подвергаются гидроксилированию и конъюгации с образованием неактивных метаболитов, экскретирующихся преимущественно почками. В дальнейшем, если не достигнуто снижение массы тела на 2 кг и более в течение 4-х недель от начала лечения, доза препарата Меридиа увеличивается до 15 мг. Предиктором дальнейшего эффективного снижения массы тела и поддержания достигнутых результатов является потеря массы тела более 2 кг за первый месяц или более 5% от исходной массы за 3 месяца фармакотерапии (11, 18). Наиболее часто встречающиеся нежелательные эффекты (сухость во рту, нарушение сна, головная боль, запоры) обычно выражены незначительно и проходят с течением времени (1, 24). Среди других возможных нежелательных эффектов следует отметить учащение пульса на 4-8 ударов в минуту, незначительное повышение САД в среднем на 1-3 мм рт. ст., ДАД – на 1,8-2,4 мм рт. ст. (4, 11, 15). Увеличение частоты ЧСС опосредовано периферическим эффектом блокады переносчика нейротрансмиттера норадреналина (23). Однако в большинстве случаев возможное повышение АД, обусловленное активностью норадреналина, нивелируется успешным снижением массы тела на фоне терапии препаратом Меридиа. Важно, что риск появления этих побочных явлений не увеличен у пациентов с контролируемой АГ (16, 21).
Врачам необходимо знать о важности контроля АД и ЧСС при назначении и коррекции дозы сибутрамина. В начале первого месяца терапии необходимо контролировать ЧСС, АД каждые 2 недели, а в дальнейшем – один раз в 1-3 месяца. Лечение препаратом Меридиа рекомендуется прекратить в случае, если ЧСС увеличилась на 10 и более ударов в минуту, а показатели САД и ДАД при двух последовательных визитах повысились на 10 мм рт. ст. В целом увеличение ЧСС, показателей АД являются причиной отмены препарата у 5% пациентов (4, 5). Препарат противопоказан при неконтролируемой АГ (≥ 145/90 мм рт. ст.), тяжелой ИБС, нарушениях сердечного ритма, застойной сердечной недостаточности, эпилепсии, печеночной и почечной недостаточности, синдроме тиреотоксикоза, терапии ингибиторами МАО и антидепрессантами, глаукоме (2, 23). Женщины детородного возраста должны использовать адекватные методы контрацепции. Следует воздержаться от приема во время беременности и лактации.
Без комплексного подхода, сочетающего немедикаментозные методы и фармакотерапию, не возможно эффективное лечение ожирения. Основной причиной неудовлетворительных результатов терапии ожирения является, как правило то,
что пациенты не соблюдают рекомендаций врача в отношении коррекции питания и увеличения физических нагрузок. Препарат Меридиа помогает тучным пациентам не только сформировать правильное пищевое поведение, но и изменить образ жизни в целом. Особо следует отметить, что снижение массы тела на фоне терапии сибутрамином сопровождается положительным влиянием на основные ассоциированные с ожирением метаболические нарушения, в том числе расстройства углеводного и липидного обменов. Высокая эффективность и хорошая переносимость препарата Меридиа позволяют рекомендовать его в комплексной долгосрочной терапии МС, обязательно включающей изменение образа жизни и увеличение физической активности.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.