Эторикоксиб: оценка эффективности и безопасности
- Аннотация
- Статья
- Ссылки



В современном мире хроническая боль является одной из наиболее частых причин утраты трудоспособности и социальной дезадаптации. С ней тесно связаны такие патологические состояния, как депрессия, нарушения сна, развитие и прогрессирование заболеваний сердечно-сосудистой системы. Необходимость длительной фармакотерапии боли становится тяжким бременем для государства и общества (1-3).
Для неврологической практики эта проблема имеет особое значение, поскольку хронические болевые синдромы являются одной из наиболее частых причин обращения к специалисту – неврологу. При этом большая часть подобных обращений происходит вследствие дорсопатий – болевых синдромов, связанных с патологией позвоночника и прежде всего с неспецифической болью в нижней части спины (БНЧС) (2-5).
Хотя данная патология носит «функциональный» характер и не является следствием прогрессирующего органического заболевания или травмы, она требует проведения активной комплексной терапии (4, 5). Боль при дорсопатиях может иметь высокую интенсивность и яркую эмоциональную окраску, сопровождаясь серьезными нарушениями функции позвоночника. При острой БНЧС это приводит к временной потери трудоспособности, а в случае хронизации патологии нередко заканчивается инвалидизацией больного. Очень важно, что хроническая БНЧС, как и любой иной хронический болевой синдром, может стать дополнительным фактором, опосредованно угрожающим жизни пожилых пациентов с коморбидной патологией сердечно-сосудистой системы.
Яркой иллюстрацией этого положения стало исследование австралийских ученых K. Zhu и сотр. (2007). В течение 5 лет они наблюдали когорту из 1484 пожилых женщин (старше 70 лет), страдающих БНЧС. Среди этих пациенток 21,7% исходно и 26,9% на момент окончания периода наблюдения испытывали боли в области спины ежедневно. Оказалось, что в данной подгруппе риск гибели от кардиоваскулярных осложнений оказался выше более чем в 2 раза – ОР 2,13 (1,35 – 3,34) в сравнении с пациентками, испытывавшими боли реже, чем 1 раз в день (6).
Эти данные указывают на серьезную проблему – ведь большая часть пожилых пациентов, страдающих от хронических заболеваний опорно-двигательной системы, имеют коморбидную кардиоваскулярную патологию. Исследование распространенности заболеваний сердечно-сосудистой системы у 15000 жителей США в возрасте 65 лет и старше, страдающих остеоартрозом (ОА), показало наличие артериальной гипертензии у 80%, сахарного диабета – у 31,3%, признаков сердечной недостаточности – у 38%, ишемической болезни сердца – у 16,9%, а цереброваскулярных нарушений – у 17,3% (7).
Для лечения БНЧС предложено и активно используется в клинической практике множество разнообразных способов лечения: начиная от выжидательной тактики, использования «простого анальгетика» парацетамола, и заканчивая сложными, дорогостоящими методиками физиотерапевтического воздействия. Однако обилие терапевтических подходов скорее затрудняет, а не облегчает работу в реальной клинической практике. Это связано с отсутствием единой и четкой концепции последовательной терапии БНЧС, а также противоречивым характером информации в отношении клинических достоинств различных препаратов и нефармакологических методов лечения. Поэтому в действительности выбор того или иного способа терапии зачастую имеет эмпирический характер.
В большей степени, чем при какой-либо другой патологии человека, при БНЧС популярны немедикаментозные методы лечения. В этом плане весьма показательны данные J. Chenot и сотр., которые провели опрос 1342 амбулаторных пациентов, страдающих БНЧС. Оказалось, что большинство из них (69%) получало следующие методы немедикаментозной терапии: «прогревание», массаж, мануальная терапия и акупунктура (8).
Определить реальную терапевтическую ценность нефармакологических способов лечения БНЧС не так просто. Имеется явное расхождение между восторженными рекламными материалами, рассказывающими об успешном применении тех или иных методик, которые предоставляют многочисленные коммерческие медицинские фирмы, и весьма сдержанными выводами независимых исследователей. Поэтому столь интересным представляется анализ методических обзоров и мета-анализов, посвященных в большей степени методам немедикаментозного воздействия.
В 2008 году A. Furlan и сотр. представили результаты мета-анализа 13 рандомизированных контролируемых исследований (РКИ), в которых изучалась сравнительная эффективность массажа при БНЧС. По заключению авторов, только 5 РКИ были выполнены на должном методическом уровне, при этом лишь в 2 работах проводилось сравнение с плацебо (ложный массаж). Однако суммарная оценка терапевтического потенциала массажа была позитивной. Этот метод действительно облегчает боль и способствует восстановлению функции позвоночника. Эффективность массажа, по мнению авторов, превосходит многие другие нефармакологические методы при достаточно большой стойкости полученного действия (9).
Не столь оптимистичны выводы в отношении мануальной терапии, как показали W. Assendelft и сотр. (2004). Эта работа представляет собой мета-анализ 39 РКИ эффективности мануальной терапии в сравнении с плацебо (ложная мануальная терапия) и другими методами фармакологического и нефармакологического воздействия. Согласно выводам авторов, мануальная терапия дает незначительное улучшение (в среднем на 10%) лишь в сравнении с плацебо, а в ряде случаев оказалась бесполезной или даже вредной. Она не имеет преимущества в сравнении с другими методами активного лечения (10).
Мета-анализ эффективности терапевтического лазера при БНЧС, проведенный R.Yousefi-Nooraie и сотр. (2007), основан на данных 6 РКИ. По мнению авторов, для этого метода доказано умеренное облегчение боли в сравнении с плацебо (ложная терапия). Однако лазеротерапия не оказывает существенного влияния на функциональные нарушения. Авторы делают вывод, что в сравнении с другими методами активной терапии лазеротерапия не показывает каких-либо преимуществ (11).
Авторы мета-анализа эффективности акупунктуры при БНЧС, J. Yuan и сотр. (2008), располагали для своей работы достаточно обширным материалом – данными 23 исследований (n = 6359). Выводы авторов нельзя назвать оптимистичными. По их заключению, хотя в целом акупунктура имеет благоприятное воздействие на боль и восстановление функции, этот эффект существенно выше только в сравнении с отсутствием лечения. При этом в ходе хорошо организованных исследований было показано, что истинная акупунктура не превосходит по своему действию плацебо (ложную акупунктуру) (12).
Последнее заключение хорошо иллюстрируют результаты масштабного РКИ GERAC, проведенного в Германии. В результате 1132 пациента с хронической БНЧС в течение 6 месяцев получали курсовое лечение истинной акупунктурой, или плацебо (ложная акупунктура – введение традиционных игл в ложные точки). В качестве активного контроля выступило «традиционное» лечение – физиотерапия и анальгетики. Согласно полученным результатам, истинная акупунктура оказалась достоверно эффективнее, чем «традиционное» лечение. Облегчение основных симптомов, как минимум на треть, отмечалось у 47,6% и 27,4% больных соответственно (р < 0,001). При этом ложная акупунктура по своей эффективности практически не отличалась от настоящей, ведь аналогичное улучшение в группе плацебо было достигнуто у 44,2% больных (13).
На основании приведенных данных можно сделать заключение, что четкие данные о существенных достоинствах нефармакологических методов при лечении БНЧС отсутствуют. Конечно, имеется определенная категория пациентов, для которых использование подобных методик оправдано. Однако нам неизвестны критерии, по которым можно было бы рекомендовать тот или иной метод лечения в конкретной клинической ситуации. Кроме того, нефармакологические методы не стандартизированы, а качество их применения во многом определяется опытом и знаниями соответствующего специалиста.
Выбрать медикаментозный метод терапии БНЧС существенно проще. Не вызывает сомнения, что препаратами первой линии при этой патологии должны считаться средства, обладающие непосредственным анальгетическим действием. С этой целью могут быть назначены три основные группы лекарственных препаратов – «простой анальгетик» Ацетаминофен (парацетамол), нестероидные противовоспалительные препараты (НПВП) и опиоидные анальгетики. Наиболее широко для симптоматической терапии БНЧС используются НПВП (1). Эти препараты эффективны, удобны в применении, доступны и в целом хорошо переносятся.
Назначение НПВП для симптоматической терапии БНЧС вполне оправдано с точки зрения патогенеза этого заболевания. Наиболее часто БНЧС возникает на фоне дегенеративных изменений (остеохондроз, спондилез, артроз дугоотростчатых суставов) или патологии мышечно-связочного аппарата (в рамках миофасциального синдрома). В любом случае появление боли тесно связано с процессами местного тканевого повреждения и воспаления. Синтез важнейших медиаторов воспаления и боли – простагландинов, которые вызывают первичную сенситизацию ноцицепторов, определяет активность фермента циклооксигеназы (ЦОГ-2). Этот фермент, в свою очередь, – основная фармакологическая мишень для любых НПВП, как «традиционных» (неселективных, н-НПВП), так и селективных ЦОГ-2 ингибиторов (с-НПВП) (1, 14).
Анальгетическое действие НПВП связано не только с их периферическим действием, обусловленным подавлением синтеза простагландинов, а также иных медиаторов боли и воспаления в области тканевого повреждения и воспаления. Важную роль может играть их влияние на центральные механизмы передачи болевого импульса, ведь стойкое и мощное ноцицептивное возбуждение сенсорных нейронов сопровождается гиперэкспрессией ЦОГ-2 в ткани ЦНС. Этому процессу, ответственному за хронизацию боли (14), придается ключевое значение в появлении феномена «взвинчивания» и «гиперсенсетизации».
Парацетамол, по мнению ряда экспертов, является препаратом первой линии для облегчения умеренно выраженной и слабой боли самого различного генеза, в том числе при БНЧС. Принципиальное достоинство этого препарата – хорошая переносимость и низкий риск лекарственных осложнений при кратковременном и длительном применении терапевтических доз (до 4 г/сут.).
Согласно результатам последнего мета-анализа Cochran (2008), посвященного применению НПВП при БНЧС, нет четких данных по их преимуществу в сравнении с парацетамолом (15). Это заключение представляется небесспорным, поскольку по данным РКИ парацетамол не показал себя эффективным анальгетическим средством при этой патологии. Такой вывод можно сделать на основании работы R. Davies и сотр. (2008), представляющей собой мета-анализ всех доступных РКИ, в которых оценивалось действие парацетамола при БНЧС. Исследований, в которых парацетамол сравнивался с плацебо или отсутствием терапии, авторы обнаружили всего семь. При этом отметили, что все включенные в анализ работы были относительно небольшими (суммарно 676 больных) и не очень высокого, с точки зрения доказательной медицины, качества. Согласно проведенным расчетам, достоверного облегчения боли и улучшения функции позвоночника при использовании парацетамола не отмечается (16).
Проблема определения терапевтического потенциала НПВП и парацетамола при БНЧС, по всей видимости, заключается в недостаточном количестве крупных РКИ, где эти анальгетики непосредственно сравнивались между собой. Тем не менее сопоставить их эффективность можно на основании данных, полученных при лечении остеоартроза (ОА) – столь же частой, как и БНЧС, патологии опорно-двигательной системы.
В последние годы была проведена серия длительных, масштабных и хорошо организованных РКИ – PACES-a, PACES-b, VACT, IPSO, в которых сравнивалась эффективность среднетерапевтических доз различных НПВП с высокими дозами парацетамола (3-4 г/сут.) у больных ОА. Во всех этих работах НПВП показали свое очевидное преимущество, обеспечивая уменьшение боли и улучшение функции на 30-50% больше в сравнении с парацетамолом (17-19).
Большой интерес представляет сравнение эффективности НПВП и опиоидных анальгетиков. Последние имеют мощное анальгетическое действие, поэтому их применение при выраженной боли, связанной с БНЧС, несмотря на очевидные ограничения и сложности, представляется вполне оправданным. В то же время опиоиды воздействуют лишь на проведение и восприятие болевого импульса, но не оказывают влияния на процесс его развития.
Анальгетический потенциал «жестких» опиоидов очень высок. Однако из-за сложной и громоздкой системы контроля над оборотом наркотических средств эти препараты фактически недоступны российским врачам, и говорить о возможности их широкого применения для лечения острой и хронической БНЧС в настоящее время не имеет смысла. В реальной клинической практике могут быть применены лишь «мягкие» опиоиды, такие как трамадол и кодеин (последний в низких дозах в составе некоторых комплексных обезболивающих средств). Однако оценка их эффективности при БНЧС неоднозначна. B. Martell и сотр. (2007) обобщили данные 9 РКИ, в которых лечебное действие опиоидов сравнивалось с другими анальгетиками (в том числе НПВП) или плацебо. На основании проведенного анализа авторы делают вывод, что «мягкие» опиоиды достоверно облегчают БНЧС, однако этот эффект относительно невелик (в сравнении с плацебо). При этом опиоиды в значительно меньшей степени оказывают влияние на улучшение функции позвоночника (20). Результаты нескольких РКИ, в которых изучалась сравнительная эффективность НПВП и «мягких» опиоидов при острой и хронической БНЧС, показали, что первые по своему лечебному потенциалу не уступают или даже превосходят опиоидные анальгетики (21, 22). Мы можем заключить, что в настоящее время НПВП не только наиболее популярный класс средств, используемых для лечения БНЧС, но и единственная группа лекарств, чей обезболивающий потенциал при этой патологии не вызывает сомнения. Подтверждением данного суждения является последний мета-анализ Cochran (2008), в котором проводился анализ эффективности НПВП при острой и хронической БНЧС. Авторы выбрали для своей работы 65 РКИ (всего 11237 больных), из которых 42% были признаны полностью соответствующими требованиям доказательной медицины. Полученный вывод оказался определенный: как при острой, так и хронической БНЧС НПВП однозначно эффективны (15).
Однако НПВП имеют общеизвестный недостаток, который существенно снижает их терапевтические достоинства. Это опасность развития класс-специфических побочных эффектов. В первую очередь, для этих препаратов весьма типично развитие патологии верхних отделов ЖКТ, характеризующихся наличием эрозий, язв и «гастроинтестинальных катастроф» – кровотечения и перфорации (НПВП-гастропатия). Риск появления данных осложнений у лиц, регулярно принимающих НПВП, возрастает по сравнению с популяцией более чем в 4 раза и составляет примерно 0,5-1 эпизод на 100 пациентов в год. Люди, регулярно принимающие НПВП, погибают от подобных осложнений в 2-3 раза чаще в сравнении с пациентами, не принимающими каких-либо НПВП (1, 23, 24).
Класс-специфические осложнения, возникающие на фоне приема НПВП, к сожалению, не ограничиваются только поражением органов пищеварительного тракта. Не меньшее клиническое значение имеет опасность развития осложнений со стороны сердечно-сосудистой системы. Прежде всего речь идет о так называемых кардиоваскулярных катастрофах (инфаркт миокарда, внезапная коронарная смерть, ишемический инсульт), риск которых может повышаться у пациентов, принимающих длительное время НПВП в высоких дозах. Данная патология связывается с прокоагулянтным действием этих препаратов, которая является следствием нарушения равновесия между синтезом тромбоксана А2 (ЦОГ-1 зависимый процесс) и простациклина (ЦОГ-2 зависимый процесс). Хотя все НПВП, в том числе «традиционные», могут оказывать подобное влияние, после скандально знаменитого «кризиса коксибов» проблема кардиоваскулярных осложнений для мировой медицинской общественности в первую очередь связывается с селективными НПВП (1, 25, 26).
В последнее время в нашей стране используются 14 различных НПВП, причем большинство из них представлены не только оригинальным лекарством, но и множеством дженериков. С одной стороны, такое разнообразие представителей одной фармакологической группы, которые значительно различаются как по своим свойствам, так и по цене, является благоприятным фактором, поскольку позволяет проводить индивидуальный подбор препарата с учетом особенностей клинической ситуации, социальных факторов и личностных особенностей пациента. С другой стороны, неизбежная конкурентная борьба между производителями НПВП приводит к активному распространению информации рекламного характера, что затрудняет формирование объективного мнения о реальных достоинствах и недостатках различных представителей этой фармакологической группы. И в первую очередь проблема состоит в недостаточном использовании общепризнанной мировой практики оценки эффективности и безопасности препаратов с использованием доказательств высокого уровня. Несомненно, такая оценка должна иметь систематический характер и основываться на объективных параметрах, а не на мнении отдельных экспертов.
Подобный анализ мы предлагаем провести в отношении эторикоксиба – представителя последней, наиболее совершенной генерации НПВП.
Терапевтический потенциал лекарства определяется его фармакологической природой. Принципиальное значение здесь имеет селективность в отношении ЦОГ-2 , поскольку зависимость между этим показателем и риском развития НПВП-гастропатии носит фактически линейный характер. Поэтому селективные ЦОГ-2 ингибиторы (к ним в нашей стране относят нимесулид, мелоксикам и целекоксиб) вызывают серьезные осложнения со стороны ЖКТ закономерно реже, чем н-НПВП. Напротив, наименее селективные препараты, такие как индометацин и кеторолак, ассоциируются с максимальным риском развития НПВП-гастропатии (1).
Эторикоксиб – самый селективный на сегодняшний день ингибитор ЦОГ-2. По этому параметру он превосходит всех других представителей фармакологической группы НПВП. Соотношение ингибирующей концентрации ЦОГ1/ЦОГ2 для эторикоксиба in vitro составляет 344, что существенно выше в сравнении со всеми «коксибами» (высокоселективными ЦОГ-2 ингибиторами) (27 – 29). Хорошей иллюстрацией высокой селективности эторикоксиба стало исследование J. Schwartz и сотр. Авторы оценили действие диклофенака (75 мг 2 раза в сутки), целекоксиба (200 мг 2 раза в сутки), эторикоксиба (90 мг 1 раз в сутки), а также плацебо на ЦОГ-1 зависимый синтез тромбоксана В2. Согласно результатам исследования, ингибирующая активность изучаемых препаратов и плацебо оказалась 92,2%, 20,2%, 15,5% и 2,4% соответственно (p < 0,01 в сравнении с диклофенаком) (30). Важным достоинством эторикоксиба является удачная фармакодинамика. Его отличает практически 100%-ная биодоступность, которая обеспечивает достижение пиковой концентрации препарата в плазме крови уже через 1-3 ч. после перорального приема. По быстродействию эторикоксиб не уступает любым НПВП, применяемым в ургентных случаях. Но при этом период его полувыведения составляет 22 ч. (эторикоксиб подвергается биотрансформации в печени, 70% метаболитов выводятся через почки, 20% – с калом), и в течение всего этого времени сохраняется подавление активности ЦОГ-2, в частности, в мононуклеарных клетках. Это означает, что стабильный обезболивающий и противовоспалительный эффект после однократного приема эторикоксиба продолжается не менее суток (27 – 29) (таблица 1).
Единственным методом, позволяющим определить реальный лечебный потенциал лекарственного препарата, является хорошо организованное контролируемое исследование. В отношении НПВП следует отдельно рассматривать возможность применения препарата в качестве ургентного обезболивающего средства и как средства для длительного (многомесячного) лечения боли, связанной с хроническими заболеваниями.
Лучшей проверкой анальгетического потенциала любого НПВП является его применение в анестезиологической практике. Именно при хирургической травме можно в полной мере оценить способность НПВП подавлять развитие острой боли, связанной с массивным повреждением ткани. В целом применение НПВП в послеоперационном периоде дает хорошие результаты – существенно снижается выраженность боли, улучшается самочувствие, а также уменьшается необходимость в использовании опиоидных анальгетиках (опиоид-сберегающее действие) (31). Исходя из этого, данные по применению эторикоксиба для послеоперационной анальгезии и сравнение его действия с традиционными НПВП представляет большой интерес.
В работе G. Rasmussen и сотр. (2005) оценивался уровень обезболивания у 228 больных, перенесших эндопротезирование коленного или тазобедренного сустава, на фоне применения в течение 7 дней после операции эторикоксиба 120 мг (1 раз в сутки), напроксена (1100 мг/сут.) и плацебо. Эторикоксиб показал превосходный результат: число больных, у которых через 8 ч. боль была полностью купирована, оказалось в 2 раза больше, чем в группе плацебо. О хорошем или превосходном ответе на анальгетическую терапию сообщили 53%, 60%, и 26% больных соответственно. При этом у пациентов, получавших эторикоксиб, отмечалось достоверное (на 35%) снижение потребности в наркотических обезболивающих препаратах (32).
Эффективность эторикоксиба показана и при полостных операциях. В плацебо-контролируемом исследовании A. Puura и сотр. изучалось действие эторикоксиба 120 мг и эторикоксиба 120 мг + парацетамол 1 г у 75 пациентов, перенесших лапароскопическую холецистэктомию. Препараты и плацебо использовались в режиме предоперационной анальгезии (принимались за 1,5 ч. до операции). Согласно полученным данным, использование обоих режимов активной терапии позволило достоверно снизить потребность в наркотических анальгетиках (33). Эторикоксиб с успехом использовался также для обезболивания при гинекологических операциях и манипуляциях, после хирургических вмешательств на щитовидной железе и в урологии (34-38).
Эторикоксиб весьма эффективен при острых травмах. A. Siddiqui и сотр. (2008) изучали действие эторикоксиба 120 мг (в сравнении с плацебо) у 200 пациентов, перенесших острые травмы и нуждающихся в оперативном вмешательстве. Использование НПВП позволило существенно уменьшить потребность в опиоидных анальгетиках: средняя суточная доза морфина у больных, получивших эторикоксиб, составила 35,1 + 7 мг, а среди получавших плацебо – 44,2 + 8,2 мг (p < 0,001). Соответственно, в первой группе отмечалось достоверно меньше опиоид-ассоциированных побочных эффектов (39).
Ярким подтверждением высокого анальгетического потенциала эторикоксиба стала работа K. Malmstrom и сотр., в ходе которой определялась эффективность этого препарата у лиц с острой болью после удаления 2 или более зубов. Исследуемую группу составил 201 больной, получивший непосредственно после стоматологического вмешательства эторикоксиб 120 мг, напроксен 550 мг, а также комбинированный препарат, содержащий 60 мг кодеина и 600 мг парацетамола, или плацебо. Во всех группах, получавших активную терапию, уменьшение боли было отмечено уже через 30 минут после приема лекарств. Однако спустя 8 ч. отсутствие боли после приема эторикоксиба и напроксена было отмечено у 20,9% и 21,3% пациентов, в то время как при использовании комбинации кодеина и парацетамола – у 11,5% (p < 0,001), а среди получивших плацебо – лишь у 5,4% (p < 0,001) (40).
D. Chang и сотр. провели близкое по дизайну исследование, в ходе которого эторикоксиб 120 мг назначался 100 больным после удаления 3 моляра. Контроль при этом, помимо плацебо (25 больных), составили 100 пациентов, получавших опиоидный препарат оксикодон 10 мг в комбинации с парацетамолом 650 мг. Результаты оказались аналогичны данным, полученным K. Malmstrom: эторикоксиб достоверно превосходил опиоидный препарат как по выраженности, так и по длительности анальгетического эффекта (41).
Недавно были опубликованы результаты мета-анализа 5 хорошо организованных РКИ, в которых оценивалось обезболивающее действие, которое достигается после однократного приема эторикоксиба 120 мг при острой послеоперационной боли. Суммарно в эти исследования было вовлечено 880 больных, получавших активную терапию, и 655 больных на плацебо. Анальгетический потенциал эторикоксиба не вызывал сомнений: уменьшение боли не менее чем на 50% было отмечено в среднем у 64% участников исследования, в то время как среди получавших плацебо – лишь у 10% (p < 0,001). Среди больных, получавших эторикоксиб в течение первых суток наблюдения, достоверно меньшее число потребовало повторного обезболивания или назначения дополнительных анальгетиков (42).
В терапевтической практике главной проверкой эффективности эторикоксиба стало его применение при остром подагрическом артрите. Ведь микрокристаллический синовит при подагре, возникающий вследствие моноцитарно-макрофагальной реакции и сопровождающийся массивным выбросом провоспалительных медиаторов и протеолитических ферментов, проявляется наиболее яркой картиной локального воспаления среди всех неинфекционных заболеваний.
Для купирования острого подагрического артрита используются НПВП с наиболее выраженным противовоспалительным эффектом. Здесь в течение долгого времени золотым стандартом считался индометацин (1). Поэтому в исследовании H. Schumacher и сотр. именно индометацин был выбран в качестве препарата контроля для оценки терапевтического потенциала эторикоксиба. В ходе этой работы 150 больных с острым подагрическим артритом получали эторикоксиб 120 мг/сутки однократно или Индометацин по 50 мг 3 раза в сутки. Выраженность боли определялась в баллах от 0 до 4, причем исходно ее уровень составил в исследуемых группах соответственно в среднем 2,88 и 2,99. На 3 день терапии было достигнуто существенное улучшение: уменьшение боли на 1,66 и 1,76 балла соответственно. Суммарно эффективность эторикоксиба и Индометацина не различалась: к 8-му дню наблюдения артрит был купирован у 89% и 90% больных. Однако если на фоне приема эторикоксиба серьезных осложнений не возникло, то у 3 больных в группе индометацина отмечалось появление опасной патологии ЖКТ (язвы, кровотечение) (43).
Убедительно доказана эффективность эторикоксиба при использовании его в качестве симптоматического обезболивающего средства при ревматических заболеваниях. При таких распространенных нозологических формах, как ревматоидный артрит (РА) и остеоартроз (ОА), эторикоксиб демонстрировал высокий терапевтический потенциал, обеспечивая стойкое уменьшение боли, воспалительной активности и улучшая общее самочувствие больных. Суммарно его лечебное действие при этой патологии не уступает или несколько превышает лечебное действие других НПВП (44, 45).
По мнению ряда экспертов, одним из объективных показателей эффективности того или иного препарата, который позволяет суммировать результаты различных исследований, является частота эпизодов прерывания лечения из-за отсутствия улучшения. Оценке этого параметра для эторикоксиба посвящена работа R. Moore и сотр. (2008), представляющая собой мета-анализ РКИ, в которых этот препарат использовался для лечения ОА и РА. Оказалось, что среди пациентов с ОА, получавших эторикоксиб в дозе 30 и 60 мг, число отмен из-за ее неэффективности к 12-й неделе наблюдения составило 8% и 6%. Для плацебо этот показатель составил 19%, при использовании ибупрофена – 13%, напроксена – 4%, целекоксиба 200 или 400 мг – 8%. При РА был получен аналогичный результат у больных, получавших эторикоксиб в дозе 90 мг/сутки, к 12-й неделе лечение оказалось неэффективным у 18%, а среди получавших 120 мг – у 6% (плацебо – 30%, напроксен – 15%) (46). Таким образом, действие эторикоксиба при ОА и РА как минимум в 2 раза превышает эффект плацебо и не уступает (или превосходит) действию других НПВП.
НПВП играют важнейшую роль в лечении пациентов с анкилозирующим спондилоартритом (АС), особенно центральной формы этого тяжелого заболевания. До настоящего времени эти препараты остаются незаменимым средством борьбы с тяжелыми болями в позвоночнике, столь свойственными этому заболеванию (8). Для оценки эффективности эторикоксиба при болезни Бехтерева van der Heijde и сотр. провели исследование, в ходе которого 387 пациентов с АС в течение 12 мес. принимали эторикоксиб 90 и 120 мг, напроксен – 1000 мг/сутки или плацебо. Согласно полученным результатам, эторикоксиб по всем параметрам оценки (выраженность боли в спине, активность заболевания и динамика функции позвоночника) превосходил плацебо, а также в обеих дозировках оказывал более значимое клиническое действие, чем контрольный препарат (47).
Вероятно, для неврологов наибольшую ценность имеет информация об успешном применении эторикоксиба для лечения БНЧС. Лечебное действие эторикоксиба при этой патологии изучалось как минимум в трех хорошо организованных РКИ.
Работа C. Birbara и сотр. включала 319 больных с БНЧС, которые получали эторикоксиб в дозе 60 и 90 мг, или плацебо. Исследуемый препарат показал достоверное преимущество: к 4-й неделе различие от эффекта плацебо в снижении боли составило для различных дозировок эторикоксиба 12,9 и 10,3 мм по ВАШ (р < 0,001), а к 12-й неделе – 10,5 и 7,5 мм по ВАШ (Р = 0,001). При этом также отмечалось достоверное улучшение функции позвоночника и снижение потребности в дополнительном анальгетике, в роле которого выступал парацетамол (48).
Сходный план исследования, число пациентов (n = 325) и длительность наблюдения имела работа, выполненная R. Pallay и сотр. В этом РКИ эффективность эторикоксиба также не вызывала сомнения: отличие в анальгетическом эффекте от плацебо оказалось наибольшим на 4-й неделе наблюдения, составив 15 мм для 60 мг/сут. и 13 мм для 90 мг/сут. (p = 0,001) (49) (рисунок 1).
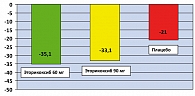
C. Zerbini и сотр. провели сравнение эффективности эторикоксиба 60 мг и Диклофенака 150 мг/сутки. В исследование были включены 446 больных с хронической БНЧС. Через 4 недели снижение выраженности боли на фоне приема эторикоксиба было весьма значительным и в среднем составило 32,9 мм (по ВАШ). Этот результат практически не отличался от эффекта диклофенака (различие на 2,5 мм ВАШ). Оба препарата, помимо анальгетического действия, обеспечили одинаковое и значимое улучшение функции позвоночника и общего самочувствия пациентов (50) (рисунок 2).
Как было отмечено выше, успешное использование НПВП может быть в значительной степени ограничено риском класс-специфических побочных эффектов. Поэтому для любого нового НПВП, появляющегося на фармакологическом рынке, принципиальное значение имеет сравнительная оценка безопасности и переносимости.
Существует несколько основных параметров оценки безопасности НПВП в отношении ЖКТ. Наиболее важным из них является определение риска угрожающих жизни осложнений: кровотечения, перфорации, клинически выраженные язвы. Для оценки этого параметра необходимы масштабные клинические исследования, включающие тысячи пациентов и сроком наблюдения не менее 3 месяцев, или эпидемиологические работы, основанные на ретроспективном анализе многолетней частоты развития подобных осложнений в реальной клинической практике (случай-контроль).
Большое значение придается оценке частоты развития язв желудка и/или двенадцатиперстной кишки (ДПК). Поскольку большинство НПВП-индуцированных язв протекают бессимптомно, эта патология не имеет столь существенного клинического значения, как кровотечения и перфорации. Тем не менее эндоскопические язвы считаются главным «суррогатным маркером» более опасной патологии, а также точным и специфичным показателем негативного воздействия НПВП на ЖКТ. Для выявления эндоскопических язв проводятся специальные клинические исследования, в ходе которых все пациенты до и после курса НПВП проходят эндоскопическое исследование верхних отделов ЖКТ.
Необходимым параметром оценки гастроинтестинальной переносимости НПВП является так называемая НПВП-ассоциированная диспепсия – различные неприятные ощущения со стороны верхних отделов ЖКТ, не связанные с повреждениями слизистой. Хотя диспепсия не угрожает жизни больных непосредственно, это самое частое осложнение (возникает у 20-30% больных) и наиболее частая причина прерывания терапии. Как показывают результаты большого числа РКИ, в которых изучалась безопасность НПВП, из-за появления неприятных ощущений со стороны ЖКТ выбывают из исследования 10-15% пациентов (1).
Эторикоксиб прошел проверку по всем параметрам ЖКТ-безопасности. Риск опасных осложнений был оценен путем мета-анализа данных серии длительных РКИ, законченных к 2003 г. (всего 5441 больной) и посвященных изучению сравнительной безопасности эторикоксиба. Общая частота эпизодов кровотечений, перфораций и клинически выраженных язв на фоне приема эторикоксиба 60-120 мг составила 1,24%. Это было в 2 раза меньше, чем у больных, получавших диклофенак, напроксен, ибупрофен (препараты сравнения), для которых частота опасных осложнений составила 2,48% (р < 0,001) (51).
В двух масштабных 12-недельных РКИ (n = 742 и n = 680) оценивалась частота развития эндоскопических язв у пациентов РА и ОА, принимавших эторикоксиб 120 мг, ибупрофен 2400 мг, напроксен 1000 мг или плацебо. Суммарная частота язв желудка и ДПК на фоне приема эторикоксиба составила 8,1% и 7,4%, что оказалось более чем в 2 раза меньше по сравнению с контрольными НПВП – 17% и 25,3% (р < 0,001), хотя и выше в сравнении с плацебо (1,9% и 1,4%). Дополнительно оценили такой важный показатель негативного влияния НПВП, как потеря крови с калом. Эторикоксиб не отличался по этому параметру от плацебо. В то же время при использовании ибупрофена кишечная кровопотеря увеличивалась более чем в 3 раза (р < 0,001) (52).
Подтверждением относительно низкой частоты развития диспепсии на фоне приема эторикоксиба являются результаты мета-анализа 9 РКИ, в которых изучалась эффективность и безопасность эторикоксиба у больных РА, ОА и БНЧС. Число эпизодов прерывания лечения из-за диспепсии для эторикоксиба составило 1,5 на 100 пациентов/лет. Разница в сравнении с н-НПВП была существенной, ведь для них этот показатель составил 2,7 на 100 пациентов/лет (p = 0,007). При этом потребность в гастропротективных средствах, которые применяются для купирования диспепсии, при использовании эторикоксиба оказалась меньше почти на 30% (53).
Как было отмечено выше, при использовании НПВП не меньшую проблему, чем НПВП-гастропатия, имеет опасность кардиоваскулярных осложнений. Поэтому эторикоксиб, как наиболее селективный ЦОГ-2 ингибитор, активно изучался для определения риска развития патологии со стороны сердечно-сосудистой системы. С этой целью был проведен мета-анализ предрегистрационных исследований (фаза IIb/III), в которых эффективность и безопасность этого препарата сравнивались с плацебо и н-НПВП у пациентов, страдающих ОА, РА, АС и БНЧС (n = 6500). Среди пациентов, принимавших участие в исследованиях, было отмечено 64 эпизода кардиоваскулярных катастроф. Согласно проведенным расчетам, достоверного отличия в отношении риска развития этой патологии между эторикоксибом и плацебо не было (ОР 1,11, 0,32-3,81). Он вызывал кардиоваскулярные осложнения несколько чаще, чем напроксен (ОР 1,70; 0,91-3,18), но реже, чем ибупрофен и диклофенак (ОР 0,83; 0,26-2,64) (37).
С целью получения наиболее полных данных о сравнительной безопасности эторикоксиба – как в отношении ЖКТ, так и сердечно-сосудистых осложнений, была проведена исследовательская программа MEDAL (Multinational Etoricoxib and Diclofenac Arthritis Long-term). В настоящее время это наиболее крупное и продолжительное исследование НПВП в мировой практике. Суммарно в программу MEDAL были включены 34701 пациент ОА и РА, которые в течение 1,5 лет непрерывно принимали эторикоксиб 60 или 90 мг или диклофенак 150 мг/сут.
План этого исследования отображал реальную клиническую практику. Поэтому у больных с серьезными факторами риска НПВП-гастропатии допускалось назначение ингибиторов протонной помпы, а при наличии кардиоваскулярного риска – низких доз аспирина.
Полученные результаты вновь подтвердили хороший терапевтический потенциал эторикоксиба. По своей эффективности он не уступал препарату сравнения – прерывание терапии из-за отсутствия положительной динамики было отмечено у 9,0% и 9,8% соответственно.
Суммарная частота осложнений со стороны ЖКТ при использовании эторикоксиба была существенно меньше в сравнении с диклофенаком – 1,0% и 1,4% соответственно (р < 0,001). Число отмен терапии из-за ЖКТ осложнений также было значительно ниже при использовании эторикоксиба и достигало (в зависимости от дозы и диагноза) 8,6%, в то время как в контрольной группе составило до 11,2% (р < 0,001). В то же время частота ЖКТ кровотечений и перфорации оказалась очень близкой – 0,3 и 0,32 на 100 пациентов/лет. По всей видимости, это было связано с применением гастропротектора (55).
Важной особенностью программы MEDAL явилось то, что существенная часть включенных в нее больных имела кардиоваскулярные факторы риска. При среднем возрасте 63,2 года около 41% в каждой группе составляли лица старше 65 лет, по 38% имели 2 и более стандартных фактора риска сердечно-сосудистых осложнений. В 2 группах примерно у 47% больных исходно была диагностирована артериальная гипертензия.
Развитие или дестабилизация артериальной гипертензии чаще отмечалась у пациентов, получавших эторикоксиб: отмены терапии, связанные с этой патологией, составили 2,2-2,5 и 0,7-1,6 эпизодов на 100 пациентов/лет. Тем не менее, частота кардиоваскулярных осложнений на фоне приема эторикоксиба и диклофенака оказалась фактически одинаковой – 1,24 и 1,3 на 100 пациентов/лет (суммарно 320 и 323 эпизода). Не различалось и число летальных исходов, связанных с кардиоваскулярными осложнениями – по 43 (0,26%) в каждой группе (56).
На основании результатов программы MEDAL можно сделать заключение, что эторикоксиб вновь доказал свою эффективность и хорошую гастроинтестинальную переносимость. При этом длительный непрерывный прием этого препарата не сопровождался значимым повышением частоты кардиоваскулярных катастроф, в сравнении с традиционным НПВП. Этот результат представляется особенно ценным с учетом того, что около половины больных имели факторы риска осложнений со стороны сердечно-сосудистой системы.
Интересно отметить, что в ходе программы MEDAL была отмечена низкая частота осложнений со стороны печени при использовании эторикоксиба. Число гепатотоксических реакций на фоне приема этого препарата оказалось примерно в 10 раз меньше, чем при использовании диклофенака.
Еще одним достоинством эторикоксиба является достаточно низкая частота реакций гиперчувствительности. В ряде исследований была показана хорошая переносимость этого препарата у больных, у которых ранее на фоне приема неселективных НПВП возникали кожные аллергические реакции, а также у лиц, страдающих аспирин-индуцированным респираторным заболеванием (57-59).
Таким образом, эторикоксиб является мощным и универсальным анальгетиком, который может применяться как для купирования острой боли, так и для длительной симптоматической терапии у пациентов с хронической патологией суставов и позвоночника (таблица 2). Эторикоксиб весьма удобен в использовании – его принимают 1 раз в день. Кроме того, широкий диапазон терапевтических дозировок – от 30 до 120 мг/сут., позволяет подобрать индивидуальную дозу препарата для конкретной клинической ситуации. В нашей стране эторикоксиб доступен под торговым названием Аркоксия (в дозировке 60, 90 и 120 мг), при этом официально зарегистрированными показаниями для его назначения являются ревматоидный артрит, остеоартроз, болезнь Бехтерева и острый подагрический артрит.
Следует помнить, что длительное использование высоких доз эторикоксиба (как и других НПВП) ассоциируется с определенным повышением риска развития кардиоваскулярных осложнений. Поэтому требуется особое внимание при назначении этого препарата больным с клинически выраженной коморбидной патологией сердечно-сосудистой системы, прежде всего лицам с ишемической болезнью сердца и некомпенсированной адекватной терапией артериальной гипертензией. При этом необходимо четко указать на тот факт, что риск кардиоваскулярных катастроф при длительном применении эторикоксиба не превышает аналогичный риск, связанный с использованием других НПВП (в частности, диклофенака).
Четко доказано, что эторикоксиб существенно безопаснее традиционных НПВП в отношении развития опасных осложнений со стороны ЖКТ, что делает возможным его использование у пациентов, имеющих соответствующие факторы риска. Используя эторикоксиб, в значительно меньшей степени, чем при назначении иных НПВП, приходится опасаться развития реакций гиперчувствительности (как кожных, так и бронхолегочных), а также гепатотоксических осложнений.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.