Ингибитор рецепторов интерлейкина 6 левилимаб в терапии ревматоидного артрита
- Аннотация
- Статья
- Ссылки
- English
Новым представителем этой группы препаратов является левилимаб – моноклональное антитело IgG1 к ИЛ-6Р, которое связывает как растворимые, так и мембранные рецепторы.
Эффективность и безопасность левилимаба были продемонстрированы в исследовании фазы II AURORA и исследовании фазы III SOLAR.
В статье представлены результаты указанных исследований, а также основные положения резолюции регионального экспертного совета ревматологов Москвы и Московской области на тему «Место нового ингибитора ИЛ-6Р левилимаба в терапии пациентов с ревматоидным артритом», заседание которого состоялось 18 декабря 2021 г. в Москве. Совет экспертов подтвердил, что левилимаб рекомендуется для широкого применения у пациентов с активным ревматоидным артритом при недостаточной эффективности или непереносимости традиционных синтетических базисных противовоспалительных препаратов.
Новым представителем этой группы препаратов является левилимаб – моноклональное антитело IgG1 к ИЛ-6Р, которое связывает как растворимые, так и мембранные рецепторы.
Эффективность и безопасность левилимаба были продемонстрированы в исследовании фазы II AURORA и исследовании фазы III SOLAR.
В статье представлены результаты указанных исследований, а также основные положения резолюции регионального экспертного совета ревматологов Москвы и Московской области на тему «Место нового ингибитора ИЛ-6Р левилимаба в терапии пациентов с ревматоидным артритом», заседание которого состоялось 18 декабря 2021 г. в Москве. Совет экспертов подтвердил, что левилимаб рекомендуется для широкого применения у пациентов с активным ревматоидным артритом при недостаточной эффективности или непереносимости традиционных синтетических базисных противовоспалительных препаратов.
Ревматоидный артрит (РА) – одно из распространенных и наиболее социально значимых иммуновоспалительных ревматических заболеваний [1]. В соответствии с современными рекомендациями при ведении больных РА необходимо придерживаться принципов лечения до достижения цели [2, 3], что обусловливает назначение современных генно-инженерных биологических препаратов (ГИБП) или таргетных синтетических базисных противовоспалительных препаратов (тсБПВП), таких как ингибиторы янус-киназ (JAK), подавляющему большинству пациентов, недостаточно отвечающих на терапию метотрексатом (МТ). При РА потребность в ГИБП или тсБПВП достигает 28–81% в зависимости от популяции [4–6]. Примерно 20% пациентов с резистентным РА для достижения как минимум низкой активности болезни требуется последовательное назначение трех ГИБП и более [7].
В настоящее время в российской клинической практике для лечения тяжелых вариантов РА используются четыре группы ГИБП:
- ингибиторы фактора некроза опухоли α (ФНО-α) – инфликсимаб, этанерцепт, адалимумаб, цертолизумаба пэгол, голимумаб;
- ингибиторы интерлейкина 6 (ИЛ-6) – олокизумаб, а также его рецепторов (ИЛ-6Р) – тоцилизумаб, сарилумаб, левилимаб;
- анти-В-клеточные препараты – ритуксимаб;
- анти-Т-клеточные препараты, в частности ингибитор костимуляции Т-лимфоцитов, – абатацепт.
Наиболее активно развивающейся группой ГИБП для лечения РА являются ингибиторы ИЛ-6 [8]. Это связано с плейотропными эффектами этого важнейшего провоспалительного цитокина, который стимулирует ряд процессов, играющих важную роль в патогенезе РА [9–11]:
- пролиферацию, дифференцировку, выживаемость, функциональную активность лимфоцитов, синовиоцитов, эндотелиоцитов, остеокластов, что индуцирует экссудативное и пролиферативное воспаление, неоангиогенез, выработку аутоантител, развитие остеопороза;
- индукцию синтеза других провоспалительных цитокинов;
- синтез клетками печени острофазовых белков, включая С-реактивный белок и сывороточный амилоид А;
- синтез гепатоцитами гепсидина, гормоноподобного пептида, пептида, регулирующего метаболизм железа в организме, что приводит к анемии хронического воспаления.
Таким образом, ИЛ-6 глобально воздействует на организм, регулируя процессы воспаления на разных уровнях.
Кроме того, ИЛ-6 влияет на циркадные ритмы организма, в частности на выработку кортизола [12, 13], что может определять такие типичные симптомы РА, как утренняя скованность, нарушение сна, утомляемость.
Ответ клеток разных тканей на ИЛ-6 осуществляется через активацию JAK/STAT-сигнального пути [14]. Для активации этого сигнального пути ИЛ-6 должен связаться со своим рецепторным аппаратом. Специальный рецептор ИЛ-6 (ИЛ-6Р) связывает ИЛ-6 с наномолярной аффинностью. Однако для передачи сигнала комплекс «ИЛ-6/ИЛ-6Р» должен связаться с гликопротеином 130 (gp130, CD130) – трансмембранным белком, состоящим из пяти доменов гликопротеина фибронектина III и одного иммуноглобулиноподобного домена. Тем самым индуцируется димеризация gp130 и инициируется внутриклеточная передача сигнала от ИЛ-6 через сигнальный путь JAK/STAT [15].
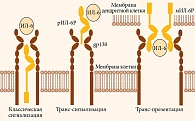
Рецептор ИЛ-6 экспрессируется на поверхности ограниченного числа клеток – на гепатоцитах и некоторых типах иммунных клеток, тогда как gp130 – повсеместно, что соответствует различным функциям ИЛ-6. Данный рецептор оказывает биологическое воздействие с помощью трех различных режимов передачи сигнала (рисунок). При классической сигнализации ИЛ-6 взаимодействует с мембранным ИЛ-6Р (мИЛ-6Р), экспрессированным в клетках, которые также экспрессируют gp130. При другом режиме передачи сигнала ИЛ-6 связывает растворимый ИЛ-6Р (рИЛ-6Р), который высвобождается после расщепления металлопротеазой ADAM17, а также образуется путем альтернативного сплайсинга мРНК [16]. Комплекс «ИЛ-6/рИЛ-6Р» связывается с gp130, образуя димер, который инициирует внутриклеточную передачу сигнала. Данный процесс получил называние «транс-сигнализация» [15]. Относительно недавно был идентифицирован еще один способ передачи сигналов ИЛ-6 – транс-презентация [17]. Этот режим специфичен для дендритных клеток, на мембране которых экспрессируется мИЛ-6Р. Образующийся на поверхности дендритных клеток комплекс «ИЛ-6/мИЛ-6Р» связывается с gp130, экспрессируемым на Т-клетках, для примирования патогенных клеток Th17 [16, 17], вырабатывающих важнейший провоспалительный цитокин – интерлейкин 17. Эти альтернативные способы передачи сигнала ИЛ-6 обусловливают множество вариантов его воздействия на разные клеточные процессы [16].
Ингибиция ИЛ-6Р была первым методом влияния на биологические эффекты ИЛ-6 [8, 18]. Выбор в качестве мишени ИЛ-6Р, а не ИЛ-6 объяснялся тем, что концентрация рецепторов характеризуется меньшей индивидуальной вариабельностью, чем концентрации ИЛ-6, что могло значительно упростить выбор дозы и схемы лечения [8, 16].
Зарегистрированные в России ингибиторы ИЛ-6Р – тоцилизумаб, сарилумаб, левилимаб – имеют сходную структуру. Они представляют собой моноклональные антитела класса G1 (IgG1) к ИЛ-6Р, связывающие как мИЛ-6Р, так и рИЛ-6Р, что обеспечивает воздействие на все режимы активации сигнального пути ИЛ-6/ИЛ-6Р/JAK/STAT.
Ингибиция ИЛ-6Р имеет свои особенности по сравнению с другими мишенями при РА – ФНО-α для его ингибиторов, CD20 на В-лимфоцитах для ритуксимаба, СD80/СD86 на Т-лимфоцитах для абатацепта. Вероятно, из-за более комплексного влияния ИЛ-6 на формирование воспаления и других проявлений РА ингибиторы ИЛ-6Р оказались эффективными независимо от метода их назначения – в комбинации с метотрексатом или в виде монотерапии. Уже в первых рандомизированных клинических исследованиях (РКИ) тоцилизумаба, наиболее давно применяющегося препарата из этой группы, отмечалась его высокая эффективность как в комбинации с метотрексатом, так и без него [19]. В исследовании ADACTA тоцилизумаб в виде монотерапии был эффективнее ингибитора ФНО-α адалимумаба [20]. В исследовании AMBITION было продемонстрировано превосходство монотерапии тоцилизумабом над монотерапией метотрексатом у больных, ранее не получавших метотрексат [21, 22]. В исследованиях сарилумаба MOBILITY [23], TARGET [24], MONARCH [25] были получены аналогичные результаты. Они подтвердили возможность применения препарата в виде монотерапии [26–28]. Именно поэтому в международных и российских клинических рекомендациях [2, 3] постулируется целесообразность назначения именно ингибиторов ИЛ-6Р при невозможности назначения МТ и других стандартных синтетических базисных препаратов (другими вариантами могут быть ингибиторы ИЛ-6 и JAK). Однако предпочтительно комбинированное применение ингибиторов ИЛ-6Р с МТ.
Наиболее новым препаратом из группы ИЛ-6Р, зарегистрированным для лечения РА в Российской Федерации, является левилимаб1 (ЛВЛ). По данному показанию он разрешен для применения в 2021 г.
Левилимаб представляет собой моноклональное антитело IgG1 к ИЛ-6Р, которое связывает как растворимые, так и мембранные рецепторы.
Препарат выпускается в виде раствора для подкожного введения 180 мг/мл – 0,9 мл (162 мг) в предварительно наполненном шприце. Режим применения – 162 мг/нед. При развитии нежелательных явлений (изменение лабораторных показателей) его можно вводить один раз в две недели [29].
Левилимаб достаточно хорошо изучен при РА в предрегистрационных исследованиях. Его эффективность была продемонстрирована в РКИ фазы II AURORA [30] и фазы III SOLAR [31] (таблица).
AURORA – многоцентровое РКИ, проведенное в 19 центрах в Российской Федерации и Республике Беларусь. В него были включены 105 лиц с активным РА, недостаточно ответивших на терапию МТ. Некоторые больные до участия в исследовании применяли другие ГИБП, а именно инфликсимаб, этанерцепт, абатацепт. Пациенты были рандомизированы на три группы: группа плацебо, группа ЛВЛ в дозе 162 мг один раз в неделю, группа ЛВЛ в дозе 162 мг один раз в две недели. Через 12 недель изначально получавшие плацебо переводились на ЛВЛ. В двойном слепом периоде к 12-й неделе частота достижения ответа по критериям ACR 20 (American College of Rheumatology) в группах ЛВЛ составила 77,1 и 57,1% соответственно, в группе плацебо – 17,1% (p < 0,01 в обоих случаях). К 52-й неделе в группах ЛВЛ частота достижения ремиссии по критериям ACR/EULAR (Еuropean League Against Rheumatism) составила 28,6%.
Исследование фазы III SOLAR также проводилось в Российской Федерации и Республике Беларусь в 19 и двух центрах соответственно. В исследовании приняли участие 154 пациента с активным РА, недостаточно ответивших на терапию МТ в стабильной дозе 15–25 мг/нед в течение четырех недель и более. Опыт применения ГИБП имел место у пяти пациентов. Большинство больных также получали глюкокортикоиды. Участники исследования были рандомизированы в группу ЛВЛ в дозе 162 мг/нед (n = 102) или группу плацебо (n = 52), которые применялись в дополнение к МТ. Через 12 недель ответ по ACR 20 был достигнут у 70 (68,6%) пациентов в группе ЛВЛ и 20 (38,5%) пациентов в группе плацебо. Низкая активность РА на 24-й неделе исследования отмечена у 53 (52,0%) получавших ЛВЛ и 3 (5,8%) применявших плацебо. Через 24 недели частота достижения ремиссии по DAS 28 с оценкой скорости оседания эритроцитов в группе ЛВЛ составила 42,2%, в группе плацебо – 1,9%, то есть один пациент.
Таким образом, в РКИ фаз II и III продемонстрировано существенное превосходство ЛВЛ над плацебо у больных РА с недостаточным эффектом на фоне МТ, среди которых также были недостаточно ответившие на ГИБП.
Показатели безопасности ЛВЛ соответствовали таковым других ингибиторов ИЛ-6Р и в целом по группе ГИБП. Среди нежелательных явлений отмечалось повышение уровня холестерина, триглицеридов, активности аланинаминотрансферазы (АЛТ) и аспартатаминотрансферазы (АСТ). Однако такие случаи были редки. Фиксировались также единичные случаи положительного интерферонового теста на Mycobacterium tuberculosis и снижения абсолютного числа нейтрофилов и лимфоцитов.
Эффективность ЛВЛ была продемонстрирована в РКИ CORONA при синдроме высвобождения цитокинов вследствие COVID-19 [32].
Необходимо отметить, что 18 декабря 2021 г. в Москве состоялся региональный экспертный совет ревматологов Москвы и Московской области, посвященный месту нового ингибитора ИЛ-6Р левилимаба в терапии пациентов с РА. В работе экспертного совета приняли участие ведущие специалисты-ревматологи Д.Е. Каратеев, А.И. Загребнева, Е.В. Жиляев, Е.Л. Лучихина, Т.В. Мезенова, Е.Н. Симонова, Л.В. Теплова, К.А. Лыткина, Е.А. Шикина, Н.М. Бабадаева и многие другие.
На основании всесторонней оценки имеющихся данных была принята резолюция, которая содержит основные выводы и рекомендации по применению левилимаба при РА.
- В рамках дискуссии участников регионального совета экспертов были сформулированы следующие основные положения:
- среди ГИБП, зарегистрированных для лечения РА, ингибиторы ИЛ-6Р являются одними из наиболее изученных и длительно используемых в реальной практике;
- с учетом роли ИЛ-6 в патогенезе РА ингибиторы ИЛ-6Р как класс имеют ряд преимуществ перед другими ГИБП;
- при недостаточной эффективности или непереносимости синтетических БПВП, в том числе при их сочетанном приеме с глюкокортикоидами, левилимаб, являясь оригинальным ингибитором ИЛ-6Р с выраженной противовоспалительной активностью, позволяет добиться низкой активности болезни или клинической ремиссии у значительной части пациентов, а также предотвратить нарушение функции суставов.
Обобщив результаты клинических исследований и последующего обсуждения, эксперты сделали заключение.
- Имеющиеся данные проведенных многоцентровых рандомизированных двойных слепых плацебо-контролируемых клинических исследований фаз II и III (BCD-089-2/AURORA, BCD-089-3/SOLAR) позволяют констатировать следующее:
- препарат левилимаб в комбинации с метотрексатом демонстрирует несомненную клиническую эффективность у пациентов, не давших адекватного ответа на лечение метотрексатом, выражающуюся в снижении активности заболевания, повышении функциональных возможностей и улучшении качества жизни;
- препарат левилимаб демонстрирует лечебные эффекты и профиль безопасности, характерные для класса препаратов – блокаторов рецептора ИЛ-6;
- препарат левилимаб может быть рекомендован для лечения пациентов с РА, не достигших целевой активности заболевания на фоне лечения традиционными синтетическими базисными противовоспалительными препаратами.
- На основании известных класс-специфических эффектов и данных клинических исследований препарата левилимаб совет экспертов дает следующие рекомендации по его применению:
a) препарат можно рассматривать как предпочтительный у пациентов с выраженными общими симптомами воспаления: высокие уровни С-реактивного белка, высокий тромбоцитоз, анемия, потеря массы тела, а также у пациентов с АА-амилоидозом;
b) при оценке эффективности препарата предпочтение следует отдавать индексам активности заболевания, не включающим оценку скорости оседания эритроцитов и уровня С-реактивного белка (например, CDAI);
c) при контроле безопасности следует тщательно мониторировать те же показатели и с той же частотой, что и при использовании других препаратов класса ингибиторов рецептора ИЛ-6 (тоцилизумаба, сарилумаба):
i) клинический анализ крови, клинический анализ мочи, креатинина, глюкозы, АЛТ, АСТ должен проводиться не менее одного раза в три месяца;
ii) липидный спектр крови определяется перед началом лечения и через три месяца;
iii) признаки латентной и манифестной туберкулезной инфекции – один раз в шесть месяцев.
- Необходим последующий анализ данных практического применения препарата левилимаб у больных РА для уточнения профиля безопасности, относительных показаний и противопоказаний для применения, удержания на терапии.
С учетом перечисленного выше левилимаб рекомендуется для широкого применения у пациентов с активным РА при недостаточной эффективности или непереносимости традиционных синтетических базисных противовоспалительных препаратов.
D.E. Karateev, MD, PhD, Prof., E.L. Luchikhina, PhD
Moscow Regional Research and Clinical Institute
Contact person: Dmitry E. Karateev, dekar@inbox.ru
The inhibitors of the biological effects of interleukin 6 (IL-6) are the most actively developing group of biologics for the treatment of rheumatoid arthritis (RA) due to pleiotropic effects of this most important pro-inflammatory cytokine, which stimulates a number of processes that play an important role in the pathogenesis of RA. IL-6 receptor (IL-6R) is of great importance in the implementation of these biological effects. Activation of IL-6R occurs with the participation of the glycoprotein gp130 in three variants: classical, and in trans-signaling and trans-presentation modes.
The most recent representative of this group is levilimab, an IgG1 monoclonal antibody to IL-6R that binds both soluble and membrane forms of the receptor.
The efficacy and safety of levilimab has been demonstrated in the Phase II AURORA and Phase III SOLAR trials.
The paper presents the main statements of the resolution of the regional expert council of rheumatologists of Moscow and the Moscow Region on the topic: ‘The place of a new IL-6R inhibitor levilimab in the treatment of patients with rheumatoid arthritis’, which took place on December 18, 2021 in Moscow. The panel of experts confirmed that levilimab is recommended for widespread use in patients with active RA who fail or are intolerant to traditional synthetic DMARDs.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.