Когнитивные расстройства без деменции: классификация, основные причины и лечение
- Аннотация
- Статья
- Ссылки
- English


![Таблица 3. Классификация когнитивных нарушений по степени тяжести [5]](/upload/resize_cache/iblock/97f/195_350_1/pronoran3.jpg)

Около 90% площади коры головного мозга человека участвует в познавательной деятельности. Поэтому большинство неврологических заболеваний с заинтересованностью головного мозга сопровождаются теми или иными когнитивными расстройствами. Обычно они сочетаются с изменениями в эмоционально-поведенческой сфере, будучи объединенными общим патоморфологическим и патофизиологическим субстратом. Практикующему неврологу необходимо оценивать наличие и особенности когнитивных и других нервно-психических нарушений и учитывать эту информацию при синдромальной, топической и нозологической диагностике заболевания нервной системы.
Нарушения когнитивных функций имеют не меньшее значение для клиницистов других врачебных специальностей. Органом-мишенью многих соматических заболеваний, в частности широко распространенных в пожилом возрасте заболеваний сердечно-сосудистой системы, является головной мозг. Оценка состояния головного мозга в таком случае исключительно важна для оценки эффективности контроля основного заболевания и выбора терапевтической тактики.
Наличие когнитивных нарушений крайне негативно влияет на качество жизни пациента и его ближайших родственников, затрудняет лечение сопутствующих заболеваний и проведение реабилитационных мероприятий. Поэтому очень важным представляются своевременная диагностика и максимально раннее начало терапии имеющихся когнитивных расстройств.
Определение и классификация когнитивных нарушений
Согласно последнему пересмотру международных рекомендаций по диагностике психических расстройств (Diagnostic and statistical manual of mental diseases – DSM-V), к когнитивным расстройствам относится снижение по сравнению с преморбидным уровнем одной или нескольких высших мозговых функций, обеспечивающих процессы восприятия, сохранения, преобразования и передачи информации (табл. 1) [1].
Важно не только установить когнитивное снижение и провести его качественный анализ, но и количественно оценить выраженность имеющихся расстройств. Известно, что некоторые лекарственные препараты, эффективные при выраженных когнитивных расстройствах (деменциях), в значительно меньшей степени влияют на когнитивные нарушения, не достигающие степени деменции. Вероятно, это связано с различными нейрохимическими изменениями, которые отмечаются на ранних и более поздних этапах патологического процесса [2–4].
Деменция (или, согласно DSM-V, выраженное нейрокогнитивное расстройство) характеризуется значительной выраженностью нарушений высших мозговых функций, которые препятствуют нормальному функционированию пациента. При деменциях из-за выраженных когнитивных расстройств пациент хотя бы частично лишен независимости и нуждается в посторонней помощи в самых обычных жизненных ситуациях (например, при ориентировании на местности, совершении покупок в магазине) (табл. 2) [1].
В лечении пациентов с выраженными когнитивными расстройствами приоритет следует отдавать препаратам с симптоматическим эффектом, которые позволяют уменьшить выраженность расстройств и тем самым повысить качество жизни пациентов и их родственников.
Диагноз недементных когнитивных нарушений устанавливается в тех случаях, когда, несмотря на имеющийся интеллектуальный дефект, пациент сохраняет самостоятельность в повседневной жизни. При этом пациент может ощущать некоторые трудности при умственной работе, что отражается в жалобах. Однако пациент преодолевает эти трудности, не прибегая к помощи со стороны (табл. 2) [1]. В лечении пациентов с недементными когнитивными расстройствами следует не только использовать симптоматическую терапию, но и проводить мероприятия по профилактике деменции.
Согласно классификации академика Н.Н. Яхно, недементные когнитивные расстройства разделяются на легкие и умеренные (табл. 3) [5]. При этом пациенты с умеренными нарушениями могут испытывать затруднения в наиболее сложных и непривычных для пациента видах деятельности. В то же время пациенты с легкими нарушениями полностью независимы и самостоятельны во всех видах активности, в том числе и самой сложной.
Последние годы возрастает внимание неврологов, психиатров и представителей других нейронаук к еще более ранней стадии когнитивной недостаточности – так называемым субъективным когнитивным нарушениям. Формулировка «субъективные когнитивные нарушения» (субъективные нарушения памяти, жалобы когнитивного характера) в настоящее время широко используется как в научной литературе, так и в повседневной клинической практике в качестве самостоятельного диагноза. Этот диагноз выставляется, если имеются жалобы когнитивного характера, в то время как результаты объективных когнитивных тестов остаются в пределах возрастной нормы.
Больные могут высказывать жалобы на повышенную забывчивость, снижение концентрации внимания, повышенную утомляемость при умственной работе, иногда – трудности подбора нужного слова в разговоре. Указанные жалобы представляют собой весьма актуальную для пациента проблему, которая может послужить самостоятельным или главным поводом для обращения к врачу. В то же время применение стандартных когнитивных тестов не выявляет каких-либо существенных отклонений от принятых нормативов. Пациенты с субъективными когнитивными расстройствами полностью сохраняют независимость в повседневной жизни. Когнитивные трудности также незаметны со стороны: родственники, сослуживцы и другие лица всегда оценивают когнитивные способности пациента как вполне сохранные.
В настоящее время известны следующие международные диагностические критерии (2014) синдрома субъективных когнитивных нарушений [6]:
-
жалобы пациента на стойкое ухудшение по сравнению с прошлым умственной работоспособности, возникшее без видимой причины;
-
отсутствие каких-либо отклонений от возрастной нормы по данным когнитивных тестов, используемых для диагностики болезни Альцгеймера и других дементирующих заболеваний;
-
когнитивные жалобы не связаны с каким-либо установленным диагнозом неврологического, психиатрического заболевания или интоксикацией.
Диссоциация между жалобами пациентов, результатами тестирования и повседневным функционированием пациентов ставит закономерные вопросы об истинной природе жалоб. Эти вопросы пока далеки от своего разрешения и активно изучаются. На современном этапе научных знаний складывается впечатление, что пациенты с субъективными когнитивными нарушениями представляют собой весьма гетерогенную группу, в которую входят как пациенты с наиболее ранними стадиями дементирующего процесса, так и пациенты с расстройствами тревожно-депрессивного и ипохондрического спектра.
В некоторых случаях преимущественно субъективный характер нарушений объясняется методологическими трудностями объективизации когнитивного статуса. В настоящее время отсутствуют общепринятые рекомендации по использованию конкретных методик для диагностики деменции или недементных когнитивных нарушений. Поэтому на практике используются тесты различной степени чувствительности, специфичности и воспроизводимости. Использование тестов с низкой чувствительностью будет приводить к недостаточной диагностике легких и умеренных когнитивных нарушений и к избыточной диагностике так называемых субъективных нарушений.
Диагноз «субъективные когнитивные нарушения» часто получают пациенты с высоким преморбидным интеллектуальным уровнем. Сниженные в результате церебрального заболевания когнитивные функции по сравнению с индивидуальной нормой длительное время формально будут находиться в пределах среднестатистического норматива. Следовательно, когнитивное снижение может длительное время оставаться формально неподтвержденным, иначе говоря, «субъективным».
Жалобы когнитивного характера могут быть обусловлены тревожно-депрессивными расстройствами в отсутствие органического церебрального заболевания. Так, пациентов с высоким уровнем тревоги будет чрезмерно беспокоить незначительная ситуационно обусловленная забывчивость. В этом случае причиной обращения к врачу становятся такие широко распространенные, в том числе среди здоровых лиц, жалобы, как «не помню, зачем пришел в комнату», «не помню, что куда положил», «не узнал знакомого человека или не вспомнил его фамилию» и др.
Однако наибольший исследовательский интерес в гетерогенной группе пациентов с субъективными когнитивными нарушениями вызывают пациенты со снижением толерантности к умственным нагрузкам, поскольку указанный патологический феномен может действительно быть наиболее ранним клиническим проявлением дементирующего процесса. Как известно, на самых начальных стадиях нейродегенеративного или цереброваскулярного заболевания клиническая симптоматика может отсутствовать, несмотря на наличие органического поражения мозга, иногда значительного. Это объясняется так называемым церебральным резервом, то есть компенсаторными возможностями головного мозга. Наличие таких возможностей будет приводить к ложноотрицательному результату тестирования. В то же время в повседневной жизни пациент может испытывать затруднения в особых условиях, когда церебральный резерв истощается и не может преодолеть возникающие трудности, например в состоянии утомления или эмоционального стресса. В настоящее время в мире весьма активно ведутся разработки методологии «интеллектуальный тредмилл». Она позволит оценить степень толерантности к повышенным умственным нагрузкам, которая может снижаться до развития клинически очерченных когнитивных расстройств.
Международные исследования свидетельствуют, что риск развития дементирующих заболеваний среди пациентов с субъективными когнитивными нарушениями достоверно выше, чем в среднем в популяции [6]. Поэтому даже изолированные жалобы, не подтвержденные когнитивными тестами, не должны оставаться без внимания лечащих врачей. Они не могут служить основанием для какого-либо определенного клинического диагноза, но их наличие является показанием для активной профилактики, в первую очередь немедикаментозной (умственная и физическая активность, оптимизация питания и образа жизни).
Диагностика умеренных когнитивных нарушений
Как следует из приведенных выше критериев (табл. 2), диагностика синдрома умеренных нейрокогнитивных нарушений базируется, во-первых, на жалобах пациентов и/или их родственников, во-вторых, на объективных результатах тестирования. При этом следует учитывать, что жалобы когнитивного характера далеко не всегда прямолинейны. Обычно на снижение памяти или повышенную забывчивость жалуются пациенты с так называемым амнестическим типом синдрома умеренных нейрокогнитивных нарушений, у которых в когнитивном статусе преобладают прогрессирующие мнестические расстройства. У таких пациентов в будущем чаще всего устанавливается болезнь Альцгеймера. Однако, по данным анализа специализированного амбулаторного приема пациентов с когнитивными нарушениями, самой частой причиной синдрома умеренных когнитивных нарушений является цереброваскулярная патология. Так, опыт первой российской клиники нарушений памяти свидетельствует, что дисциркуляторная энцефалопатия или последствия острых нарушений мозгового кровообращения обусловливают 68% умеренных когнитивных нарушений [7].
Сосудистые когнитивные нарушения в большинстве случаев относятся к так называемому подкорково-лобному типу. При этом память на текущие события и события жизни практически не страдает, а в когнитивном статусе преобладают снижение концентрации внимания и темпа познавательной деятельности (брадифрения), нарушение управляющих лобных функций (планирование и контроль). Характерной особенностью является также частое сочетание когнитивных и эмоционально-поведенческих нарушений: депрессии, апатии или аффективной лабильности. Следует подчеркнуть, что эмоционально-поведенческие расстройства при хронической сосудистой мозговой недостаточности носят органический характер и вызываются тем же поражением головного мозга (дисфункция фронто-стриарных связей), что и когнитивные нарушения. Коморбидность сосудистой депрессии и сосудистых когнитивных нарушений составляет не менее 80% [8–11].
Пациенты с сосудистыми когнитивными расстройствами редко жалуются на забывчивость, так как память у них относительно сохранна. В структуре жалоб доминируют так называемые субъективные неврологические симптомы: головная боль, несистемное головокружение, шум и тяжесть в голове, повышенная утомляемость, нарушения сна. Указанные симптомы достаточно типичны для начальных стадий дисциркуляторной энцефалопатии и в недалеком прошлом рассматривались как важный признак хронического ишемического поражения головного мозга. В настоящее время очевидно, что головная боль, головокружение и другие неприятные ощущения в голове не могут быть непосредственным результатом церебральной ишемии. Патогенез субъективных неврологических симптомов более сложен и связан в первую очередь с имеющимися когнитивными, эмоциональными и двигательными расстройствами. Так, головная боль чаще всего имеет характер головной боли напряжения, которая, как известно, практически всегда обусловлена тревогой и/или депрессией. Эмоциональную причину также имеют нарушения сна. Повышенная утомляемость может как быть признаком депрессии (табл. 4), так и отражать снижение умственной работоспособности. В последнем случае данная жалоба есть субъективный эквивалент когнитивных расстройств. Головокружение при хронической недостаточности мозгового кровообращения обычно носит несистемный характер и описывается как чувство неустойчивости при ходьбе. За этим ощущением, как правило, стоят реальные нарушения равновесия вследствие поражения фронто-стриарных и фронто-церебеллярных связей.
Субъективные неврологические симптомы почти всегда присутствуют на начальных стадиях хронической сосудистой мозговой недостаточности. Они не могут быть основанием для диагноза, но должны заставить врача заподозрить хроническое цереброваскулярное заболевание. Для подтверждения диагноза необходима тщательная оценка когнитивного и эмоционального статуса с помощью объективных методик. На стадии умеренных (недементных) когнитивных расстройств следует использовать наиболее чувствительные методики, например Монреальскую шкалу оценки когнитивных функций [12].
Патогенетическая и симптоматическая терапия недементных когнитивных нарушений
На сегодняшний день окончательно не выработан единый общепризнанный протокол ведения пациентов с когнитивными нарушениями, не достигающими выраженности деменции. Многие международные исследования не смогли продемонстрировать, что фармакотерапия такими препаратами, как ингибиторы ацетилхолинэстеразы, пирацетам, нестероидные противовоспалительные средства, предотвращает или снижает риск развития деменции [2–4]. В то же время в тех же работах была показана способность некоторых из указанных выше лекарственных препаратов уменьшать выраженность симптоматики у пациентов с синдромом умеренных когнитивных нарушений.
Эмпирически в повседневной клинической практике в настоящее время широко используются вазотропные и нейрометаболические лекарственные средства, дофаминергический и норадренергический препарат пирибедил (Проноран) и блокаторы NMDA-рецепторов.
Результаты ряда крупных исследований и опыт практического применения свидетельствуют о клинической эффективности препарата пирибедил (Проноран). Проноран имеет комплексный механизм действия: он стимулирует постсинаптические D2/D3-рецепторы к дофамину и блокирует пресинаптические альфа-адренорецепторы. При этом блокада пресинаптических адренорецепторов ведет к увеличению церебральной норадренергической активности. Таким образом, на фоне применения данного лекарственного средства увеличивается активность двух церебральных нейротрансмиттерных систем: дофаминергической и норадренергической. Обе эти системы непосредственно вовлечены в познавательную деятельность. При этом считается, что дофаминергическая стимуляция префронтальной коры опосредованно через мезокортикальный дофаминергический путь играет важную роль в процессах внимания и обеспечивает интеллектуальную гибкость, то есть способность менять парадигму поведения. Норадренергическая активация важна для процессов запоминания и воспроизведения информации, поскольку обеспечивает оптимальный для мнестической деятельности уровень концентрации внимания и мотивации. С возрастом снижаются синтез и активность как дофамина, так и норадреналина. Поэтому коррекция указанных нейротрансмиттерных нарушений на фоне применения Пронорана способствует уменьшению выраженности ассоциированных с возрастом нарушений внимания и памяти. Кроме того, благодаря адреноблокирующему и дофаминергическому действию Проноран оказывает также благоприятный вазотропный эффект, что создает дополнительные преимущества при когнитивных нарушениях сосудистой этиологии [13–16].
В клинической практике Проноран используется для лечения легких и умеренных когнитивных нарушений, не достигающих выраженности деменции, у пациентов старше 50 лет. Препарат может назначаться как при сосудистых когнитивных нарушениях, так и на начальных стадиях нейродегенеративного процесса. По данному показанию было выполнено большое число клинических исследований, в том числе с использованием двойного слепого метода. Так, во Франции в 1980-е гг. проведено 14 клинических исследований, в которых принимало участие более 7 тыс. пациентов с недементными когнитивными нарушениями. Было показано, что Проноран способствует достоверному улучшению показателей памяти, концентрации внимания и интеллектуальной гибкости, то есть способности изменять парадигму поведения в зависимости от внешних условий [17, 18]. В 2001 г. клиническая эффективность Пронорана была вновь продемонстрирована в работе D. Nagaradja и S. Jayashree. Авторы использовали Проноран при синдроме умеренных когнитивных нарушений в соответствии с современными диагностическими критериями. Было показано, что на фоне исследуемого препарата отмечается более чем двукратное увеличение частоты когнитивного улучшения по краткой шкале оценки психического статуса по сравнению с плацебо, что имело статистически и клинически значимый характер [19].
В настоящее время российские специалисты также имеют значительный опыт использования Пронорана у пациентов с когнитивными нарушениями, не достигающими выраженности деменции. Так, в рамках исследования ПРОМЕТЕЙ Проноран получали 574 пациента из 33 городов 30 регионов России, из них 336 женщин и 207 мужчин, в возрасте от 60 до 89 лет (средний возраст 69,5 ± 5,5 года) с легкими или умеренными когнитивными расстройствами. Для лечения отбирались пациенты с жалобами когнитивного характера, которые набирали 25–27 баллов по краткой шкале оценки психического статуса или выполняли с ошибками тест рисования часов, но не соответствовали диагностическим критериям деменции. На фоне терапии было зафиксировано статистически значимое улучшение когнитивных функций, которое отмечалось уже на шестой неделе лечения и в дальнейшем возрастало вплоть до окончания 12-недельного наблюдения. При этом одна часть пациентов получала монотерапию Пронораном, а другая часть – Проноран в комбинации с вазотропными и/или нейрометаболическими препаратами. Достоверной разницы между указанными группами пациентов показано не было, то есть комбинация Пронорана с вазотропной и нейрометаболической терапией не имела преимуществ перед монотерапией исследуемым препаратом [20, 21].
В рамках наиболее крупного российского несравнительного исследования терапию Пронораном получали более 2 тыс. пациентов в возрасте от 50 до 94 лет (средний возраст 64,9 ± 8,3 года) с диагнозом «дисциркуляторная энцефалопатия первой или второй стадии» и с легкими или умеренными когнитивными нарушениями. Все пациенты принимали Проноран в течение трех месяцев. По мнению лечащих врачей, в 2/3 случаев отмечалось значительное или умеренное улучшение когнитивных и других неврологических функций [22].
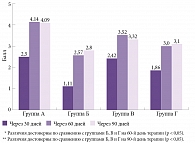
По некоторым данным, величина терапевтического эффекта дофамин- и норадренергической терапии в отношении недементных когнитивных расстройств может быть больше, чем у других активно используемых в клинической практике вазотропных и нейрометаболических препаратов. В исследовании ФУЭТЕ наблюдались 189 пациентов, из них 139 женщин и 57 мужчин, в возрасте от 42 до 82 лет (средний возраст 63,6 ± 8,5 года) с когнитивными расстройствами, не достигающими выраженности деменции, на фоне артериальной гипертензии и церебрального атеросклероза. Лечение пациентов проводилось различными препаратами, при этом представители терапевтических групп не отличались по возрасту, уровню образования и клиническим особенностям основного заболевания. На фоне проводимой терапии отмечался регресс как субъективных, так и объективных когнитивных расстройств во всех сравниваемых терапевтических группах. При этом выраженность субъективного улучшения и объективная динамика когнитивных тестов на фоне применения Пронорана после двух месяцев терапии были достоверно больше по сравнению с вазотропной и нейрометаболической терапией (рис. 1) [23].
Регресс когнитивных расстройств, по данным специальных тестов, является главным критерием эффективности проводимой терапии. Однако, как уже отмечалось выше, многие пациенты с умеренными когнитивными нарушениями, в первую очередь сосудистой природы, предъявляют также жалобы на головную боль, несистемное головокружение, шум, тяжесть или иные неприятные ощущения в голове, повышенную утомляемость и нарушения сна. Эти жалобы имеют одну природу и связаны как с когнитивной недостаточностью, так и с изменениями в эмоциональном статусе пациентов на начальной стадии хронической сосудистой мозговой недостаточности. Они существенно снижают качество жизни пациентов и часто являются основной причиной обращения к неврологу. Поэтому динамика субъективных неврологических симптомов у пациентов с синдромом умеренных нейрокогнитивных нарушений сосудистой этиологии на фоне проводимой терапии крайне важна для оценки значимости клинического эффекта и степени влияния терапии на повседневную жизнь пациентов. Регресс субъективных неврологических симптомов в наибольшей степени способствует приверженности терапии.
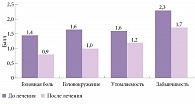
В исследовании Н.Н. Яхно и соавт. (2006) 29 пациентов с диагнозом «умеренные когнитивные нарушения» на фоне дисциркуляторной энцефалопатии первой-второй стадии получали Проноран в течение трех месяцев [24]. При этом не использовались какие-либо другие вазотропные или нейрометаболические препараты. На фоне лечения Пронораном достоверно уменьшались частота и выраженность головной боли, головокружения, утомляемости и субъективного ощущения забывчивости (рис. 2). Об ослаблении субъективных неврологических симптомов на фоне применения Пронорана сообщали и другие авторы [17, 18]. Таким образом, дофамин- и норадренергическая терапия способствует значительному улучшению самочувствия пациентов, а следовательно, повышает качество жизни и приверженность проводимым лечебным мероприятиям.
Можно резюмировать, что к настоящему времени Проноран зарекомендовал себя как эффективное лекарственное средство, улучшающее когнитивные способности и самочувствие у пациентов с начальными стадиями органических церебральных заболеваний без деменции. В отличие от болезни Паркинсона, при которой используются существенно большие дозы, при недементных когнитивных нарушениях Проноран назначается в дозе 50 мг/сут один раз в день. Рекомендуемая длительность терапии – не менее трех месяцев.
V.V. Zakharov
Sechenov First Moscow State Medical University
Contact person: Vladimir Vladimirovich Zakharov, zakharovenator@gmail.com
Here, there are outlined classification, diagnostic criteria, opportunities of pathogenetic and symptomatic therapy of cognitive impairment no dementia. Opportunities of using dopaminergic and noradrenergic drug piribedil (Pronoran) in treatment of mild and moderate cognitive impairments without developing dementia are discussed in more detail.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.