Опыт комбинированного применения топического препарата, содержащего трифаротен, и перорального доксициклина у пациентов с акне тяжелой степени тяжести
- Аннотация
- Статья
- Ссылки
- English
Акне – это хроническое воспалительное заболевание, которое занимает восьмое место по распространенности в мире и встречается как среди подростков, так и среди взрослых всех демографических групп [1]. Примерно у 50% пациентов с элементами акне на коже лица они присутствуют и на коже туловища [1]. Акне может осложняться формированием рубцов и очень часто имеет психоэмоциональные последствия, включая заниженную самооценку, социальную дезадаптацию, при этом считается, что такие последствия преимущественно обусловлены локализацией высыпаний на эстетически значимых участках кожи, таких как лицо [2]. Однако недавние исследования показали, что акне на лице и туловище оказывают более негативное влияние на качество жизни, чем только акне на лице. Кроме того, влияние на качество жизни ухудшается с увеличением тяжести акне на туловище из-за застенчивости по поводу внешнего вида и нежелания участвовать в деятельности, при которой могут быть видны высыпания на туловище [3].
Акне – это мультифакторное заболевание, при котором ключевое значение имеют четыре фактора: аномальная фолликулярная кератинизация, повышенная выработка кожного сала, колонизация Cutibacterium acnes (C. acnes), воспаление [4]. На тяжесть акне оказывают влияние экспозом-факторы, такие как употребление продуктов с высоким гликемическим индексом, употребление молочных продуктов, прием некоторых лекарственных препаратов и БАДов, а также факторы окружающей среды [5]. Дополнительный вклад вносят генетические факторы и нарушения в качественном составе микробиоты кожи [6].
Методы медикаментозной терапии акне включают топические и системные препараты, при этом ретиноиды играют ключевую роль в лечении пациентов вне зависимости от фенотипа и степени тяжести. Топические ретиноиды включают такие молекулы, как третиноин, адапален, тазаротен и трифаротен. Терапевтические эффекты ретиноидов реализуются через RAR-рецепторы (рецепторы ретиноевой кислоты) благодаря их противовоспалительному действию. После нанесения на кожу ретиноид проникает в сально-волосяной фолликул и попадает в место образования микрокомедона, после чего транспортируется в эпителиальные клетки, связываясь с RAR в их ядрах. Это вызывает активацию генов, изменяющих процессы кератинизации фолликулов, пролиферацию клеток и оказывающих влияние на воспаление, что имеет решающее значение в патогенезе акне, способствует ускорению терапии акне и предотвращению появления новых элементов [7, 8].
Элементы акне традиционно делят на «воспалительные» и «невоспалительные», однако воспаление существует при любой их форме. Медиаторы и рецепторы воспаления, в том числе ряд цитокинов, дефензинов, пептидаз и других молекул, играют роль в патогенезе акне. На непораженной коже и ранних поражениях при акне обнаружена активация Е-селектина, молекул сосудистой адгезии-1, интерлейкина (ИЛ) 1 и интегрина. Кроме того, в области комедонов была показана активация ИЛ-1, а в непораженной коже – повышение иммунореактивности дефензина-2, Т-клеток и макрофагов [9]. Именно топические ретиноиды действуют при невоспалительной форме акне, а также подавляют экспрессию toll-подобных рецепторов (TLR)-2 и ИЛ-10, оказывая таким образом противовоспалительный эффект [10]. Кроме того, недавний транскриптомный анализ изменений в очагах акне, разрешившихся спонтанно, и очагах акне, разрешившихся с помощью лечения ретиноидом трифаротеном, показал, что трифаротен модулирует уникальный набор из 67 генов, которые не были обнаружены в спонтанно разрешающихся поражениях [11]. Гены, на которые воздействует трифаротен, в первую очередь участвуют в клеточной миграции, воспалении и организации внеклеточного матрикса, а также в численности уникальной популяции SPP1+ пролиферативных макрофагов, недавно обнаруженных в фиброзной ткани [11].
В соответствии с актуальными клиническими рекомендациями ретиноиды назначаются в качестве первой линии лечения акне (топические при легкой и средней степени тяжести, системные – при тяжелой степени тяжести), поскольку они влияют на множество аспектов патофизиологии акне. С момента одобрения первого топического ретиноида (третиноина) Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) в 1971 г. молекулы ретиноидов претерпели химические модификации, которые привели к клиническим улучшениям эффективности и безопасности [12]. Трифаротен является ретиноидом четвертого поколения и разработан специально для обеспечения высокой селективности в отношении RAR-γ.
Трифаротен для местного применения (крем Аклиф, 50 мкг/г или 0,005%; Галдерма) – первая новая молекула ретиноида, одобренная в США, за более чем 20 лет – показан к применению один раз в день при вульгарных акне [13–15]. Трифаротен 50 мкг/г впервые получил одобрение в США в октябре 2019 г., затем в Канаде в ноябре 2019 г., в Европе в декабре 2019 г. и в РФ в сентябре 2022 г. (крем Аклиф, регистрация в ЕАЭС). Трифаротен является мощным селективным агонистом рецепторов ретиноевой кислоты, преимущественно RAR-γ [16].
Фармакокинетическое исследование (n = 19) показало, что трифаротен имеет незначительную системную абсорбцию после 29 дней местного применения в дозах от 1,5 до 2 г в день на кожу лица, груди, плеч и спины, что позволяет наносить препарат на большие поверхности [13, 17]. Трифаротен не снижал системное воздействие пероральных контрацептивов у 24 здоровых добровольцев, участвовавших в исследовании лекарственного взаимодействия [17]. Кроме того, исследование с участием 60 здоровых взрослых не выявило влияния на электрофизиологию сердца через 14 дней приема трифаротена в сверхтерапевтической дозе (12 г трифаротена 100 мкг/г) [18, 19].
В РФ крем Аклиф с трифаротеном 50 мкг/г показан для лечения акне средней и тяжелой степени тяжести при наличии многочисленных комедонов, папул и пустул с локализацией патологического процесса на коже лица и/или туловища у пациентов 12 лет и старше [20].
Актуальными в плане определения профиля пациентов для назначения трифаротена являются исследования с изучением эффективности комбинированных схем терапии, включая системные антибиотики, в т.ч. у пациентов с тяжелыми формами акне. Так, в международном многоцентровом рандомизированном контролируемом исследовании DUAL J.Q. DelRosso и соавт. (2022) [19] изучали комбинированное лечение пациентов с тяжелыми акне с помощью крема трифаротен 50 мкг/г и перорального доксициклина в дозе 120 мг, который, согласно дополнительно проведенному исследованию, был биоэквивалентен пероральному доксициклину в дозе 100 мг [21]. Пациенты в возрасте 12 лет и старше с тяжелыми акне на лице (по шкале Глобальной оценки исследователя IGA* = 4 балла), определяемыми как 20 и более воспалительных поражений, 30–120 невоспалительных поражений и до четырех узлов, были рандомизированы 2 : 1 в группы терапии с использованием крема с трифаротеном (Т) плюс доксициклин (Д) в дозе 120 мг (n = 133 пациентов, Т + Д) или крема с плацебо (п) (основа крема с трифаротеном) плюс плацебо доксициклина (n = 69 пациентов, Тп + Дп) в течение 12 недель. Абсолютное общее количество поражений изменилось на -69,1% в группе Т + Д и -48,1% в группе Тп + Дп (р < 0,0001). Сообщалось также о значительном уменьшении как воспалительных, так и невоспалительных поражений при применении комбинации Т + Д. Выраженный клинический эффект (достижение IGA = 0/1 балл, что означает «чистая или почти чистая кожа») был отмечен у 31,7% пациентов в группе Т + Д в сравнении с 15,8% в группе Тп + Дп (р = 0,01). Безопасность и переносимость были сопоставимы в группах исследования, при этом нежелательные явления наблюдались у 13,5% пациентов, получавших лечение Т + Д, и у 15,9% пациентов, получавших лечение Тп + Дп [19]. Эти данные подтверждают целесообразность применения системных антибиотиков и топического трифаротена у пациентов с тяжелыми формами акне.
Далее представлены собственные клинические наблюдения применения крема Аклиф, содержащего трифаротен 50 мкг/г, один раз в сутки, вечером и перорального доксициклина в дозе 100 мг два раза в сутки (курс две-три недели). Представлены данные наблюдения пациентов в течение 8–12 недель от начала лечения, в то же время следует отметить, что все пациенты продолжили терапию трифаротеном.
Клинический пример 1
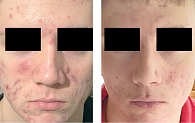
Пациент К., 18 лет, с диагнозом «акне тяжелой степени тяжести (IGA = 4 балла), рубцы постакне». Болеет акне более четырех лет. Неоднократно получал лечение системными и топическими антибиотиками с временным эффектом. Локальный статус: процесс носит островоспалительный характер, представлен множественными пустулами, папулами, единичными узлами, рубцами. Пациенту было назначено лечение: доксициклин 100 мг два раза в день 14 дней, крем трифаротен один раз в день – восемь недель (период наблюдения) с последующим продолжением применения топического препарата, а также специализированная дерматокосметика (очищение и увлажнение кожи). После восьми недель наблюдений в анкете удовлетворенности терапией пациент сообщил, что в целом удовлетворен лечением. Из побочных эффектов пациент отметил сухость кожи лица (1 балл по 4-балльной шкале). Через восемь недель лечения общее количество высыпаний на лице уменьшилось на 90% для воспалительных поражений и на 60% для невоспалительных поражений (IGA = 2 балла) (рис. 1).
Клинический пример 2
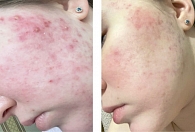
Пациентка Р., 16 лет. Болеет акне около трех лет. Получала лечение топическими препаратами с временным положительным эффектом. Локальный статус: процесс носит островоспалительный характер, представлен множественными пустулами, папулами, поствоспалительными пятнами, единичными атрофическими рубцами на коже лица (тяжелая степень, IGA = 4 балла). Пациентке было назначено лечение: доксициклин 100 мг два раза в день 14 дней, крем трифаротен один раз в день восемь недель (период наблюдения) с последующим продолжением применения топического препарата, а также специализированная дерматокосметика (очищение и увлажнение кожи). В анкете (восемь недель лечения) пациентка указала, что удовлетворена лечением. Хотя в течение первых двух недель лечения наблюдалась легкая эритема, шелушение и сухость кожи лица, результаты опросника удовлетворенности показали, что побочные эффекты ее беспокоили в умеренной степени (2 балла по 4-балльной шкале). Через восемь недель лечения общее количество высыпаний на лице уменьшилось на 90% для воспалительных поражений и на 70% для невоспалительных поражений (IGA = 1 балл) (рис. 2).
Клинический пример 3
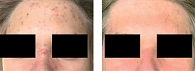
Пациент Г., 17 лет. Болеет акне в течение 2,5 лет. Периодически использовал дерматокосметические средства. Локальный статус: процесс носит островоспалительный характер, представлен множественными пустулами, папулами, единичными узлами, поствоспалительными пятнами на коже лица (тяжелая степень, IGA = 4 балла). Пациентке было назначено лечение: доксициклин 100 мг два раза в день 14 дней, крем трифаротен один раз в день восемь недель (период наблюдения) с последующим продолжением применения топического препарата, а также специализированная дерматокосметика (очищение и увлажнение кожи). В анкете (восемь недель лечения) пациент указал, что удовлетворен лечением. На вопрос, беспокоят ли его побочные эффекты, отметил эритему и сухость кожи лица (2 балла по 4-балльной шкале). Через восемь недель лечения общее количество высыпаний на лице уменьшилось на 100% для воспалительных поражений и на 80% для невоспалительных поражений (IGA = 0–1 балл) (рис. 3).
Клинический пример 4
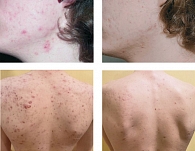
Пациент И., 22 лет, с диагнозом «акне тяжелой степени тяжести, рубцы постакне». Болеет акне в течение пяти лет. Неоднократно получал лечение антибиотиками, системным ретиноидом с временным эффектом. Локальный статус: процесс носит островоспалительный характер, локализуется на коже лица, груди, спины, представлен множественными пустулами, папулами, единичными узлами, рубцами (тяжелая степень, IGA – 4 балла на лице, PGA* – 4 балла на туловище). Пациенту было назначено лечение: доксициклин 100 мг два раза в день в течение 21 дня, крем трифаротен один раз в день в течение 12 недель (период наблюдения) с последующим продолжением применения топического препарата, а также специализированная дерматокосметика (очищение и увлажнение). В сроки 6, 7, 8, 9 и 10 недель пациенту были проведены процедуры IPL-терапии (область спины). После 12 недель наблюдений в анкете удовлетворенности терапией пациент сообщил, что полностью удовлетворен лечением. На вопрос, беспокоят ли его побочные эффекты, отметил сухость кожи лица в период с первой по пятую неделю терапии (2 балла по 4-балльной шкале). Через 12 недель лечения общее количество высыпаний уменьшилось на 90% для воспалительных поражений и на 50% для невоспалительных поражений (IGA = 0–1 балл, PGA = 1 балл) (рис. 4).
Обсуждение и заключение
Трифаротен — топический ретиноид последнего поколения [11], является мощным агонистом RAR (рецепторов ретиноевой кислоты), специфически связываясь с гамма-подтипом RAR (RAR-γ), который является преобладающим (90%) типом рецепторов в коже в ядрах кератиноцитов [1, 3]. Трифаротен обладает 20-кратной селективностью в отношении RAR-γ по сравнению с RAR-α и RAR-β, тогда как третиноин, тазаротен и адапален менее специфичны. Трифаротен регулирует экспрессию как известных генов, модулируемых ретиноидами, так и экспрессию новых генов, позитивно влияя на патологические процессы при акне. Так, в исследовании J. Aubert и соавт. (2018) [13] было показано, что трифаротен как ретиноид воздействует на гены, регулирующие эпидермальную дифференцировку клеток, пролиферацию и кератинизацию. В исследовании B. Dreno и соавт. (2021) [11] было показано, что трифаротен дополнительно регулирует 67 уникальных генов, участвующих в образовании воспалительных клеточных инфильтратов и реорганизации внеклеточного матрикса. Трифаротен также положительно влияет на численность (возвращает к нормальному уровню) уникальной популяции профибротических макрофагов (SPP1+), которые активируются при акне [11].
В широкомасштабных международных многоцентровых исследованиях было доказано, что трифаротен эффективен при акне средней степени тяжести с локализацией на коже лица и туловища и имеет хороший профиль безопасности как при применении в течение 12 недель, так и при длительном применении (52 недели) [14–16]. Кроме того, в международном исследовании DUAL было показано, что трифаротен эффективен в сочетании с пероральным доксициклином при применении у пациентов с акне тяжелой степени тяжести [19]. Это также подтверждается результатами описанных выше клинических наблюдений.
* IGA (Investigator’s Global Assessment) – шкала общей оценки исследователем, для оценки и мониторинга акне с локализацией на коже лица (от 0 – «чистая кожа» до 4 баллов – тяжелая степень).
*PGA (Physician’s Global Assessment) – шкала общей оценки врачом, для оценки и мониторинга акне с локализацией на коже туловища (от 0 – «чистая кожа» до 4 баллов – тяжелая степень).
В целом трифаротен является методом медикаментозного лечения вульгарных акне с доказанной эффективностью и подходит для монотерапии акне средней степени тяжести с множественными высыпаниями (папулами, пустулами, комедонами), а также в сочетании с пероральным доксициклином при тяжелых формах акне с единичными узлами.
L.S. Kruglova, PhD, Prof., N.V. Gryazeva, PhD
Central State Medical Academy of Department of Presidential Affairs, Moscow
Contact person: Natalia V. Gryazeva, tynrik@yandex.ru
The article presents the results of large international clinical studies that have proven clinical efficacy and good safety profile of both monotherapy with a topical medicine containing trifarotene in patients with moderate acne and its combination with oral doxycycline in patients with severe acne. Trifarotene as was shown to demonstrate a high selectivity for retinoic acid receptors RAR-γ, which are predominant in the skin, that ensures clinically important efficacy. In addition, the article presents the results of our own clinical observations.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.