Первая линия терапии распространенного гормонозависимого HER2- рака молочной железы. Интенсификация лечения
- Аннотация
- Статья
- Ссылки
- English
Введение
Рак молочной железы является одной из самых распространенных опухолей в мире [1]. В России в 2016 г. с впервые установленным диагнозом рака молочной железы поставлено на учет 68 547 пациентов [2]. Грубые показатели заболеваемости и смертности составили 87,09 и 28,27 на 100 тыс. женского населения соответственно, прирост заболеваемости за десять лет – 33,08% [2]. Ежегодно в Иркутской области рак молочной железы диагностируется более чем у 1200 женщин, около 10% из них на момент первичной диагностики имеют отдаленные метастазы [3, 4].
Несмотря на расширение знаний о молекулярно-генетических характеристиках рака молочной железы и развитие таргетной терапии, пятилетняя выживаемость пациенток с метастатическими формами рака остается около 27% [5]. После радикального лечения у 30% больных со стадией N- и до 70% со стадией N+ отмечаются рецидив и прогрессирование заболевания [6]. С появлением отдаленных метастазов цель лечения меняется с выздоровления на увеличение выживаемости при сохранении удовлетворительного качества жизни [7].
Выбор терапии зависит от ряда молекулярно-генетических маркеров. До назначения лечения все больные должны пройти исследования рецепторов к стероидным гормонам – эстрогенам (РЭ) и прогестерону (РП), HER2, Ki-67, а в ряде случаев исследование мутаций в генах BRCA1 и BRCA2 [7, 8].
Установлено, что в 33% случаев злокачественная опухоль молочной железы гиперэкспрессирует рецепторы HER2, в 71% – РЭ и/или РП. В 19% случаев опухоль может быть отнесена к трижды негативному раку с отсутствием экспрессии рецепторов гормонов и HER2 [9]. В первой линии при рецептор-негативном раке назначают химиотерапию, при гормонозависимой опухоли в отсутствие признаков висцерального криза – гормонотерапию [7, 8]. К гормонозависимым опухолям относятся новообразования с позитивной экспрессией РЭ и/или РП в более чем 1% клеток опухоли. Медиана продолжительности ответа на первую линию гормонотерапии составляет от 11 до 16 месяцев [10, 11]. Ингибиторы циклинзависимых киназ (CDK4/6), включенные в схему лечения, способны повышать его эффективность [12].
Клинический случай
Пациентка З. 1972 года рождения обратилась в Иркутский областной онкологический диспансер в апреле 2014 г. В ходе обследования был диагностирован рак молочной железы T2N0M0, стадия IIА. При исследовании трукат-биоптата первичной опухоли обнаружена рецептор-позитивная опухоль с отрицательным статусом HER2 1+. Индекс пролиферации Ki-67 7%.
2 июня 2014 г. выполнены радикальная кожесберегающая мастэктомия слева, одномоментная реконструкция левой молочной железы с эндопротезированием.
Результаты гистологического исследования операционного материала: левая молочная железа с подмышечной клетчаткой, в центральном секторе, в толще, опухолевый узел молочно-белого цвета 2,5 × 1,5 см, при микроскопии в опухоли структуры инвазивной карциномы неспецифицируемого типа, в клетчатке три лимфатических узла 1–1,5 см обычного строения pT2N0G2.
В рамках комплексного лечения с 23 июня по 6 октября 2014 г. проведено шесть курсов химиотерапии по схеме АС (доксорубицин 60 мг/м2, циклофосфан 600 мг/м2).
20 ноября 2014 г. выполнена операция – второй этап реконструкции левой молочной железы, эксплантация грудного экспандера, эндопротезирование имплантата ARION.
С ноября 2014 г. назначена адъювантная эндокринотерапия тамоксифеном 20 мг/сут ежедневно на протяжении пяти лет.
21 апреля 2016 г. проведены лапаротомия, ампутация матки с придатками по поводу миомы матки и гиперплазии эндометрия, удаление яичников выполнено с учетом возраста, гормонотерапии рака молочной железы и профилактики возможного рака яичников. Исследования BRCA-статуса не проводилось.
С мая 2017 г. появились сухой кашель, боли в грудной клетке, требовавшие регулярного приема анальгетиков. В июне 2017 г. пациентка обратила внимание на увеличение лимфатического узла в левой надключичной области. В июле 2017 г. обратилась к онкологу. При обследовании, по данным мультиспиральной компьютерной томографии (МСКТ), выявлено прогрессирование заболевания: метастазы в плевре, легких и лимфатических узлах. Метастазирование в костную систему исключено на основании результатов остеогаммасцинтиграфии. Сопутствующей патологии не выявлено.
24 июля 2017 г. выполнена эксцизионная биопсия надключичного лимфатического узла слева.
При гистологическом исследовании в лимфоузле надключичной области слева размером до 1 см обнаружен метастаз аденокарциномы с солидно-железистыми структурами. Проведено иммуногистохимическое исследование на парафиновых срезах с антителами GCDPF-15, Mammaglobin, РЭ, РП. В клетках метастатической карциномы – позитивные реакции с вышеперечисленными маркерами. Реакция с HER2/neu негативная. Заключение: метастатическая рецептор-позитивная карцинома молочной железы.
Тамоксифен в адъювантном режиме отменен в связи с генерализацией процесса. В общем и биохимическом анализах крови клинически значимых отклонений не выявлено. Результаты электрокардиограммы в пределах нормы, корригированный интервал QT, рассчитанный по формуле Фридерика (QTcF), – 350 мсек.
8 сентября 2017 г. начато лечение в рамках клинического исследования IIIb фазы по оценке эффективности и безопасности комбинации в расширенной популяции пациентов CLEE011A2404 (NCT02941926): рибоциклиб (LEE011) в дозе 600 мг перорально ежедневно с 1-го по 21-й день цикла совместно с летрозолом 2,5 мг перорально ежедневно непрерывно длительно.
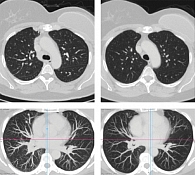
Через восемь недель терапии нормализовалось общее состояние, исчезли перечисленные выше жалобы. По данным МСКТ, в динамике (по состоянию на 28 ноября 2017 г., спустя два месяца терапии) достигнута частичная регрессия опухоли. При исследовании 20 февраля 2018 г. (через пять месяцев терапии) диагностирована полная регрессия опухоли, сохранявшаяся в сентябре 2018 г. (рисунок).
Из нежелательных явлений зарегистрированы кратковременная кожная сыпь, степень СТС АЕ 1, тошнота на первой неделе приема рибоциклиба, степень СТС АЕ 1. Нейтропения до 3-й степени СТС АЕ 1 продолжительностью менее семи дней отмечалась после первых двух циклов приема рибоциклиба и не потребовала снижения дозы.
Обсуждение
После проведенного в 2014 г. комплексного лечения в августе 2017 г. у пациентки диагностирован диссеминированный гормонозависимый рак молочной железы на фоне адъювантной терапии тамоксифеном. Больная находилась в состоянии постменопаузы после ампутации матки с придатками по поводу миомы матки и гиперплазии эндометрия. Удаление яичников выполнено с учетом возраста, гормоночувствительности рака молочной железы и профилактики возможного рака яичников. Исследование BRCA-статуса в тот период не проводилось. В такой ситуации назначается гормонотерапия. Возможными опциями могут быть высокие дозы фулвестранта 500 мг каждые четыре недели или ингибиторов ароматазы (анастрозол, летрозол, экземестан) в монорежиме [7, 8]. Данная терапия высокоэффективна, но у одних пациентов существует первичная резистентность, у других неминуемо развивается приобретенная. Медиана продолжительности ответа колеблется от 13,8 до 16,6 месяца [13].
Согласно данным клинического исследования FALCON, в отличие от анастрозола фулвестрант эффективен в отсутствие висцеральных метастазов.
При использовании новой группы препаратов ингибиторов CDK4/6 в терапии первой и последующих линий при гормонопозитивном HER2-негативном диссеминированном раке молочной железы были получены обнадеживающие результаты [12, 14–16]. В исследованиях MONALEESA2 и PALOMA2 при добавлении ингибитора CDK4/6 к ингибитору ароматазы увеличилась выживаемость без прогрессирования (ВБП) в первой линии. Так, на фоне применения комбинации рибоциклиба и летрозола ВБП увеличилась с 16 до 25,3 месяца по сравнению с монотерапией летрозолом. При этом комбинация «рибоциклиб + летрозол» существенно увеличила медиану ВБП как у пациентов с предшествующей нео(адъювантной) эндокринотерапией (19,3 месяца), так и без нее (на момент среза данных медиана ВБП не была достигнута) [17]. Двухлетняя ВБП в группе рибоциклиба и летрозола составила 54,7%, в группе плацебо – 35,9% [18]. Аналогичные результаты получены при использовании другого ингибитора CDK4/6 – палбоциклиба в комбинации с летрозолом [19]. В более позднем исследовании рибоциклиба в комбинации с тамоксифеном или нестероидным ингибитором ароматазы и гозерелином у женщин в пременопаузе в качестве первой линии терапии при гормонопозитивном HER2-негативном раке (MONALEESA 7) были подтверждены ранее полученные данные [20].
Еще один ингибитор CDK4/6 абемациклиб в комбинации с летрозолом или анастрозолом также значительно увеличивает ВБП [21]. Но в настоящее время абемациклиб не зарегистрирован в России.
Доказана эффективность комбинаций CDK4/6-ингибиторов с фулвестрантом [22–24].
Назначенная нами комбинация рибоциклиба и летрозола оказалась высокоэффективной и привела к обратному развитию клинической симптоматики (кашель, боли в грудной клетке), отмене сопутствующей обезболивающей терапии и полной регрессии опухоли, по данным МСКТ с контрастированием, в соответствии с критериями RECIST 1.1, через 16 недель от начала терапии.
К наиболее частым нежелательным явлениям при терапии рибоциклибом относятся нейтропения и повышение уровней трансаминаз [17, 18, 25, 26]. Удлинение интервала QTcF – явление достаточно редкое: по данным клинического исследования MONALESSA-2 – 3,3% случаев. В рассматриваемой ситуации из негативных явлений зарегистрированы кожная сыпь, степень СТС АЕ 1, тошнота на первой неделе приема рибоциклиба, степень СТС АЕ 1. Нейтропения до 3-й степени СТС АЕ 1 продолжительностью менее семи дней отмечалась после первых двух циклов приема комбинации рибоциклиба и летрозола. Клинически значимых изменений на электрокардиограмме и удлинения интервала QTcF не зарегистрировано. В целом переносимость комбинации была хорошей. Снижения доз препаратов или модификации режима приема не требовалось.
Заключение
Препараты группы ингибиторов CDK4/6 значительно повышают эффективность первой линии терапии гормонопозитивного HER2-негативного распространенного рака молочной железы. Комбинация рибоциклиба и летрозола, зарегистрированная в России, характеризуется высокой эффективностью и хорошей переносимостью.
Приведенный клинический случай демонстрирует новый потенциал лечения распространенного рака молочной железы с возможностью достижения полной ремиссии.
D.M. Ponomarenko
Irkutsk State Medical Academy of Postgraduate Education
Contact person: Dmitry Mikhaylovich Ponomarenko, ponomarenkodm@gmail.com
The article discusses the application of a combination of letrozole and ribociklib in first-line treatment of metastatic hormone-dependent HER2-breast cancer.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.