Первичный и вторичный лекарственный буллезный пемфигоид у пациентов с меланомой: семиотика высыпаний, характеристика зуда, патоморфологических и лабораторных параметров
- Аннотация
- Статья
- Ссылки
- English
Цель исследования – сравнительная характеристика клинических (зуд, сыпь), дерматоскопических, лабораторных (эозинофилы, антитела к BP180 и BP220), патоморфологических и конфокально-микроскопических особенностей буллезного пемфигоида у пациентов, получающих противоопухолевую терапию.
Материал и методы. Обследованы два пациента с буллезным пемфигоидом, получающих лечение по поводу меланомы. Детально описаны и сопоставлены случаи первичного и вторичного лекарственного буллезного пемфигоида. Показаны особенности первичного лекарственного БП (более молодой возраст дебюта, ремиссия меланомы, клиническая картина невоспалительного БП с более слабым зудом, высыпания в виде папул с точечной или звездчатой эрозией в центре, выявление антител BP180 и BP230, содержание эозинофилов в крови в норме, в биоптате снижено, более благоприятное течение после отмены спровоцировавшего препарата) и вторичного (в данном случае паранеопластического) лекарственного БП (более пожилой возраст дебюта, прогрессирование меланомы, клинически классические симптомы БП с более интенсивным зудом, папулами с гладкой поверхностью, выявление антител к BP180 в крови, повышение уровня эозинофилов в крови, умеренное содержание в инфильтрате, персистенция БП после отмены спровоцировавшего препарата).
Заключение. Подчеркивается возможная роль иммунотерапевтических препаратов в провокации или индукции БП. Таргетные противоопухолевые препараты маловероятно являются значимым провоцирующим или индуцирующим БП фактором, хотя можно ожидать их влияния на течение паранеопластического буллезного пемфигоида.
Цель исследования – сравнительная характеристика клинических (зуд, сыпь), дерматоскопических, лабораторных (эозинофилы, антитела к BP180 и BP220), патоморфологических и конфокально-микроскопических особенностей буллезного пемфигоида у пациентов, получающих противоопухолевую терапию.
Материал и методы. Обследованы два пациента с буллезным пемфигоидом, получающих лечение по поводу меланомы. Детально описаны и сопоставлены случаи первичного и вторичного лекарственного буллезного пемфигоида. Показаны особенности первичного лекарственного БП (более молодой возраст дебюта, ремиссия меланомы, клиническая картина невоспалительного БП с более слабым зудом, высыпания в виде папул с точечной или звездчатой эрозией в центре, выявление антител BP180 и BP230, содержание эозинофилов в крови в норме, в биоптате снижено, более благоприятное течение после отмены спровоцировавшего препарата) и вторичного (в данном случае паранеопластического) лекарственного БП (более пожилой возраст дебюта, прогрессирование меланомы, клинически классические симптомы БП с более интенсивным зудом, папулами с гладкой поверхностью, выявление антител к BP180 в крови, повышение уровня эозинофилов в крови, умеренное содержание в инфильтрате, персистенция БП после отмены спровоцировавшего препарата).
Заключение. Подчеркивается возможная роль иммунотерапевтических препаратов в провокации или индукции БП. Таргетные противоопухолевые препараты маловероятно являются значимым провоцирующим или индуцирующим БП фактором, хотя можно ожидать их влияния на течение паранеопластического буллезного пемфигоида.

Введение
Меланома является основной причиной смерти пациентов в структуре всех злокачественных новообразований кожи [1]. У большинства пациентов с локальными стадиями заболевания предпочтение отдается хирургическому иссечению опухоли, однако хирургический подход не является оптимальным при распространенном процессе. Не так давно для лечения метастатической меланомы (ММ) использовались только химиотерапевтические препараты, не обладающие достаточной эффективностью, но последние достижения в изучении патогенеза меланомы, а также внедрение иммунотерапии, таргетных терапевтических препаратов и комбинированных схем лечения произвели революцию в лечении ММ, продемонстрировав многообещающие результаты с точки зрения эффективности и безопасности [2].
Одним из относительно новых методов терапии является применение ингибиторов иммунных контрольных точек (ИКТ) – нового класса препаратов, появление которого радикально изменило концепцию терапии онкологических больных. Однако, несмотря на общий благоприятный профиль безопасности, их применение ассоциировано с развитием специфических токсических реакций, которые потенциально могут повлиять на лечение. Так называемые иммуноопосредованные нежелательные явления (ИНЯ) в основном соответствуют иммунным реакциям, которые могут затрагивать практически все системы органов [3].
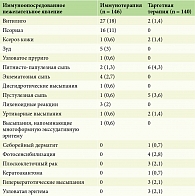
По данным ретроспективного когортного исследования G. Gullo и соавт., включавшего 286 пациентов с метастатической меланомой III или IV стадии, которые получали комбинированную терапию iBRAF + iMEK или иммунотерапию ИКТ, были получены эпидемиологические данные по спектру и частоте встречаемости дерматологических иммуноопосредованных нежелательных явлений (табл. 1) [4]. Следует отметить, что в данное исследование не были включены такие нежелательные явления, как синдром Стивенса – Джонсона / токсический эпидермальный некролиз и буллезный пемфигоид, ввиду их относительно редкой частоты встречаемости.
Дерматологические иммуноопосредованные нежелательные явления являются наиболее распространенными формами токсичности и поражают до 50% пациентов, проходящих иммунотерапию. У пациентов, получающих лечение ИКТ, часто развиваются кожные реакции, но довольно редко они достигают степени тяжести ≥ 3 по CTCAE (общие терминологические критерии для оценки нежелательных явлений) версии 5.0. Кожная токсичность часто является самым ранним проявлением ИНЯ и возникает в среднем через пять недель от начала применения анти-PD-1, через три-четыре недели при применении анти-CTLA-4 и через две недели при использовании комбинации ипилимумаба и ниволумаба. Кожная токсичность, возникающая при комбинированной блокаде рецепторов PD-1/CTLA-4, как правило, протекает более тяжело и начинается раньше [5].
Среди буллезных дерматозов, ассоциированных с приемом анти-PD-1/PD-L1 препаратов, наиболее частым является буллезный пемфигоид (БП). В патогенезе БП принимают участие аутоантитела, нацеленные на два структурных белка дермо-эпидермального соединения: BP-1 (BPAG1 или антиген BP230) и BPAG2 (или антиген BP180) [6]. Частота развития БП как ИНЯ, развивающегося у пациентов со злокачественными новообразованиями, получающих терапию ингибиторами контрольных точек, варьирует от 0,3 до 3,8% в различных исследованиях [7]. Развитие БП в основном ассоциировано с применением с анти-PD-1/PD-L1 препаратов, реже встречается при терапии анти-CTLA-4. В сравнении с другими ИНЯ, высыпания при буллезном пемфигоиде имеют более позднее начало, в среднем первые признаки развиваются только через 14 недель после начала лечения и проявляются продромальной небуллезной фазой зуда, за которой следует развитие генерализованных или локализованных напряженных пузырей с серозным или геморрагическим содержимым. Пузыри при БП обычно располагаются на коже сгибательных поверхностей, например в подмышечных впадинах, слизистая оболочка полости рта вовлекается в 10–30% случаев [5, 8].
R. Mari и соавт. описали случай БП, развившегося у пациента через четыре года после начала терапии ниволумабом и сохраняющегося даже после отмены ИКТ, что подчеркивает тот факт, что иммуноопосредованные нежелательные явления могут иметь отсроченный характер и, более того, могут длительно сохраняться, несмотря на отмену ИКТ [9].
Как следует из результатов национального итальянского многоцентрового ретроспективного обсервационного исследования, проведенного M. Merli и соавт., ассоциированный с приемом ИКТ буллезный пемфигоид у мужчин развивается чаще, чем у женщин (74%). Наиболее распространенными первичными опухолями у обследованных пациентов были меланома кожи (42%) и немелкоклеточный рак легких (25%). Терапия анти-PD-1 препаратами чаще ассоциировалась с БП, как наиболее часто встречающимся буллезным дерматозом, ассоциированным с терапией ИКТ, поскольку в 45% случаев (169 из 373) пациенты находились на терапии ниволумабом, а в 40% (148 из 373) – на терапии пембролизумабом. Средний промежуток времени между началом приема ИКТ и развитием БП в данном исследовании составил 26 недель [10]. В исследование также были включены пациенты с другими иммуноопосредованными буллезными нежелательными явлениями.
Иммунотерапия была полностью отменена у 49% пациентов (182 из 373) по причине развития ИКТ-индуцированного БП, а в качестве лечения чаще всего использовались системные кортикостероиды (62%) и антибиотики тетрациклинового ряда (38%). Что касается исхода опухоли, то среди пациентов с БП (n = 218) 32% находились в стабильном состоянии, у 23% был достигнут полный ответ, в 22% случаев наблюдался частичный ответ на терапию ИКТ, у 23% наблюдалось прогрессирование опухоли. После отмены ИКТ с медианным интервалом в девять недель проявления БП возобновились у 25 пациентов [10].
Кроме того, по-видимому, существует взаимосвязь между клиническим течением буллезного пемфигоида и злокачественных новообразований, в частности меланомы, вне зависимости от терапии ИКТ. В литературе описаны случаи острого начала БП с одновременным обнаружением метастатического процесса. Так, после иссечения меланомы в начальной стадии, а затем пораженного лимфатического узла, J.M. Marks и соавт. отметили параллельное улучшение клинического течения БП у женщины 61 года. После резекции лимфатического узла пациентке удалось снизить дозу преднизолона с требуемых для лечения БП 60 мг в сутки до 2,5–5 мг в сутки [11].
K.T. Amber и соавт. также описали случай быстрого разрешения клинических проявлений БП после иссечения меланомы кожи [12].
J. Siegel и соавт. провели ретроспективный анализ девяти случаев индуцированного иммунотерапией БП и во всех девяти случаях наблюдали либо первоначальный положительный ответ опухоли на терапию, либо стабильное течение заболевания, хотя в шести случаях в конечном итоге наблюдали прогрессирование опухоли. При последующем наблюдении за пациентами пять из девяти пациентов были живы, а четверо умерли в результате осложнений, связанных с распространенной злокачественной опухолью [13].
Хотя появляется все больше свидетельств того, что развитие кожной токсичности на фоне иммунотерапии может быть связано с улучшением ответа опухоли на проводимую терапию и выживаемость, для подтверждения этой гипотезы необходимы дальнейшие исследования [14].
В когортном исследовании с участием 2955 пациентов, находящихся на терапии ИКТ, J.T. Said и соавт. оценивали факторы риска развития БП. Авторами было обнаружено, что возраст 70 лет и старше и наличие злокачественных новообразований кожи были связаны с повышенным риском развития БП, ассоциированного с иммунотерапией. Согласно одновариантной модели логистического регрессионного анализа Firth, возраст 70 лет и старше (p = 0,01), мужской пол (p = 0,05) и наличие меланомы (p < 0,01) или немеланомного рака кожи (НМРК) (p < 0,01) были ассоциированы с повышенным риском развития индуцированного иммунотерапией БП. В ходе анализа методом вложенной выборки было выявлено, что фактором риска развития БП на фоне иммунотерапии (p = 0,01) был первоначальный полный или частичный ответ на противоопухолевую терапию по сравнению со стабильным течением или прогрессированием опухоли [7].
Хотя механизм развития БП при лечении ИКТ у пациентов с вышеупомянутыми факторами риска все еще неясен, потенциальными триггерами могут являться, во-первых, повышенные уровни аутоантител к BP180 у пациентов с меланомой. Во-вторых, существует вариант человеческого лейкоцитарного антигена, ассоциированный как с меланомой, так и с БП HLA-DQB1*0301. Иммунная активация, вызванная ингибиторами контрольных точек, может усугубить этот базовый риск. На генетическом уровне полиморфизм человеческого лейкоцитарного антигена (HLA) может обусловливать предрасположенность как к БП, так и к меланоме. Высокая экспрессия HLA-DQB1*0301 была обнаружена у лиц европеоидной расы с меланомой кожи, а также она является независимым предиктором рецидивов и метастазирования. Кроме того, HLA-DQB1*0301 тесно взаимодействует с BP180 и является наиболее изученным HLA-аллелем, ассоциированным с БП [7, 12, 14].
A.C. Bateman и соавт. было выявлено увеличение частоты генотипа HLA-DQB1*0303 среди пациентов с меланомой кожи по сравнению с контрольной группой (19,2 против 5,8%) в популяции Великобритании. Также было обнаружено, что HLA-DQB1*0301 ассоциировался с более распространенными первичными опухолями и, следовательно, с худшим прогнозом. Эти данные свидетельствуют о том, что локус HLA DQB1 и, в частности, аллели HLA DQB1*0303 и *0301 могут играть важную роль в определении риска развития и прогноза меланомы кожи [14].
В исследовании T. Krenacs и соавт. сообщалось об экспрессии эндодомена BP180 (коллагена XVII типа) при меланоме и ее отсутствии в доброкачественных меланоцитарных новообразованиях. Коллаген XVII типа представляет собой гемидесмосомальный трансмембранный белок недифференцированных кератиноцитов массой 180 кДа, который взаимодействует с ламинином 332 (ранее именуемым ламинином 5) базальной мембраны. Являясь мишенью для антител при БП, коллаген XVII типа также известен как BP180/BPAG2. Наличие эндодомена коллагена XVII типа было статистически связано с инвазивным фенотипом меланомы. Эти результаты позволяют предположить, что накопление эндодомена коллагена XVII типа в меланоцитарных опухолях связано с их злокачественной трансформацией [15].
Кроме того, в популяционном исследовании K. Kridin и соавт. c участием 3924 пациентов с БП было обнаружено, что наличие меланомы в анамнезе на 50% повышает риск развития БП. Риск развития БП был выше среди мужчин и лиц старше 80 и сохранялся даже после поправки на многочисленные искажающие факторы, включая терапию анти-PD-1/PDL-1. Что касается риска развития меланомы у пациентов с БП, то он также был несколько повышен, но не достиг уровня статистической значимости. Согласно этому исследованию, наличие меланомы в анамнезе ассоциировано с 50% увеличением риска развития БП. Практикующие врачи, ведущие пациентов с обоими заболеваниями, должны быть осведомлены об этой связи [16]. Кроме того, необходимо помнить, что у пациентов старше 60 лет повышается риск развития аутоиммунных буллезных дерматозов в целом и БП в частности. Также у пациентов с онкологическим процессом заболеванием в анамнезе нужно учитывать возможность развития паранеопластических процессов, к которым также относится БП. Взаимосвязь механизмов развития потенциального паранеопластического процесса и ИНЯ до конца не ясна и требует дальнейшего изучения.
Высыпания при БП могут либо изначально быть представлены преимущественно пузырями, либо пузыри могут прогрессивно изменяться в течение нескольких недель и месяцев. В исследовании M. Liu и соавт., включавшем 60 пациентов с ИКТ-индуцированным БП со средним возрастом 71 год (диапазон от 30 до 85 лет), среди которых преобладали мужчины (78,3%), наиболее частыми клиническими проявлениями были напряженные пузыри (93,3%), зуд (55,0%) и уртикарные высыпания (31,7%) [17].
Если у пациента, проходящего иммунотерапию, развивается зудящая сыпь, которая не разрешается при использовании топических стероидов, то следует заподозрить наличие буллезного пемфигоида. В таких случаях рекомендуется провести биопсию кожи. Биопсию следует проводить в непосредственной близости от очага поражения, в пределах 1 см от пузыря. Биоптат должен быть взят из видимо здорового участка кожи [18, 19]. По данным некоторых авторов, взятие для патоморфологического исследования самого пузыря и интактной кожи в отдаленных участках кожного покрова связано с более высокой частотой ложноотрицательных результатов при проведении прямой реакции иммунофлуоресценции (ПИФ). C. Sladden и соавт. при проведении ретроспективного анализа 1423 биоптатов обнаружили, что 50% биоптатов, взятых с небуллезных высыпаний при БП, были положительными при проведении ПИФ, но только 22% биоптатов, полученных из кожи вблизи очагов поражения, давали положительный результат. Эти данные указывают на то, что биоптаты, полученные из небуллезных высыпаний (в непосредственной близости от пузыря, в пределах 1 см), с большей вероятностью дадут положительный результат при ПИФ. Это открытие имеет большое клиническое значение, поскольку схемы лечения при ПИФ-положительных и ПИФ-отрицательных буллезных дерматозах различаются [20].
Имеются лишь единичные описания случаев развития БП, ассоциированного с таргетной терапией. Так, H. Eriksson и соавт. описали три случая развития высыпаний, напоминающих таковые при БП, у пациентов, находящихся на терапии таргетными препаратами. На примере клинического случая авторы предполагают, что высыпания, напоминающие БП, обычно быстро разрешаются после отмены таргетного препарата (в данном случае вемурафениба). При БП, ассоциированном с приемом ИКТ, кожная токсичность часто сохраняется в течение нескольких месяцев после прекращения лечения [21]. Однако в двух случаях из трех были соблюдены не все критерии для постановки диагноза БП, поскольку исследования методом прямой и непрямой РИФ не проводились [21].
R. Satta и соавт. описали случай развития пемфигоидоподобных высыпаний у 82-летнего пациента с метастатической меланомой, находящегося на терапии дабрафенибом, через шесть месяцев после старта терапии. Термин «пемфигоидоподобная сыпь/реакция» вместо «буллезный пемфигоид» применяется авторами по следующим причинам: развитие нежелательной реакции после начала таргетной терапии, улучшение после снижения дозы дабрафениба и специфическая патоморфологическая картина буллезного пемфигоида в сочетании с отрицательными результатами иммунофлуоресцентного анализа [22].
Потенциальная роль таргетной терапии в развитии БП все еще не определена, однако известно, что эти препараты могут модулировать иммунный ответ из-за повышения уровня антигенов, цитокинов и увеличения инфильтрации CD4+- и CD8+- лимфоцитов, характерных для меланомы. БП считается аутоиммунным заболеванием, однако в процесс могут быть вовлечены аутореактивные Т-клетки/регуляторные клетки. Экспрессия BP180 выявляется вдоль базальной мембраны и на клетках меланомы [23]. В целом данный факт указывает на схожие пути патогенеза БП как изолированного заболевания, паранеопластического процесса, а также в рамках развития ИНЯ.
Ввиду высоких показателей эффективности иммунотерапии и таргетной терапии при метастатической меланоме, вполне вероятно, что данные виды терапевтического воздействия получат более масштабное распространение среди различных групп пациентов. Таким образом, осведомленность практикующих врачей о такой тяжелой иммуноопосредованной токсичности, как буллезный пемфигоид, может помочь в ранней диагностике и, следовательно, предупреждении прогрессирования высыпаний. В этой статье мы описаны и сопоставлены два случая первичного и вторичного лекарственного буллезного пемфигоида, ассоциированного с терапией ИКТ.
Клинический случай 1
Пациентка Т., 62 года. В 1998 г. была иссечена меланома кожи передней грудной стенки, с тех пор находится под наблюдением. В ноябре 2020 г. самостоятельно обнаружила уплотнение в правой надключичной области. Узел был иссечен, гистологически верифицирован метастаз меланомы, обнаружена мутация BRAF v600E. В НМИЦ онкологии им. Блохина был назначен ниволумаб, лечение проводилось с января 2021 по март 2022 г.: 22 инфузии ниволумаба (3 мг/кг в/в кап. 1 раз в 14 дней) с последующей отменой в связи с отсутствием метастатических очагов по результатам ПЭТ-КТ. Терапию перенесла хорошо, с единичным эпизодом зудящих высыпаний легкой степени тяжести, полностью разрешившихся на фоне терапии наружными глюкокортикостероидными препаратами.
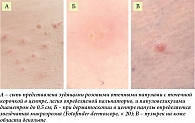
Спустя шесть месяцев после завершения терапии ниволумабом, в октябре 2022 г., пациентка обратилась к дерматологу с жалобами на зудящие высыпания на коже лица, туловища, верхних и нижних конечностей. При осмотре наблюдалась распространенная сыпь воспалительного характера, представленная немногочисленными зудящими бледно-розовыми уртикароподобными папулами диаметром до 0,5 см, в центре подавляющего большинства которых имелись точечные серозные корочки со звездчатыми очертаниями при дерматоскопии либо везикулы до 1 мм в диаметре. Элементы сыпи не сливались и не были сгруппированы, располагались на чистой коже, преимущественно на коже живота, груди, поясницы, единичные очаги отмечались на коже межлопаточной области (рис. 1).
Было проведено гистологическое исследование уртикарного элемента с везикулой в центре, расположенного на коже живота. Выявлен ортогиперкератоз, акантоз, спонгиоз, отек сосочкового слоя дермы, выраженная периваскулярная лимфоцитарная инфильтрация. Заключение: картина спонгиотического дерматита.
Назначена системная противозудная терапия (цетиризина дигидрохлорид, 10 мг в сутки), наружная терапия глюкокортикостероидными препаратами (мазь клобетазола пропионата один раз в день с последующим постепенным переходом на крем локоид два раза в сутки), на фоне чего отмечалось практически полное исчезновение элементов. Однако после короткого периода почти полной ремиссии пациентка отметила приступообразное появление аналогичных элементов. В последующем аналогичные приступообразные рецидивы повторялись после непродолжительных периодов почти полной ремиссии.
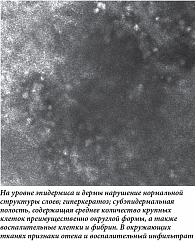
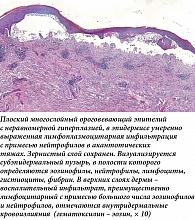
В декабре 2022 г. в момент очередного обострения отметила появление на коже груди единичного пузыря около 5 мм с напряженной толстой покрышкой, узким бледно-розовым эритематозным венчиком в основании. С целью уточнения диагноза и получения дополнительных данных о морфологии была выполнена конфокальная микроскопия in vivo (рис. 2). Проведено патоморфологическое исследование пузыря (рис. 3) и иммуногистохимическое исследование видимо непораженной кожи вблизи пузыря. Заключение: патоморфологические изменения более всего соответствуют буллезному пемфигоиду. Иммуногистохимическое исследование: иммуноморфологическая картина может наблюдаться при буллезном пемфигоиде с лечебным патоморфозом. Проведено исследование сыворотки крови методом непрямой иммунофлуоресценции, антител к десмоглеинам первого и третьего типов не обнаружено, выявлены антитела к белкам BP180 (116,08 RU/мл) и BP230 (102,40 RU/мл).
Поставлен диагноз «буллезный пемфигоид, легкая степень тяжести по CTCAE v 5.0». Продолжена наружная терапия глюкокортикостероидными препаратами и системная терапия антигистаминными препаратами. В течение следующих нескольких месяцев отмечено постепенное нарастание степени тяжести эпизодов обострений и некоторое увеличение количества пузырей (до трех – пяти штук), в связи с чем после получения результатов общего и биохимического анализов крови (все показатели в пределах нормы) был назначен дапсон в дозе 50 мг/сут с повышением дозы через неделю до 100 мг/сут. Спустя месяц прием препарата был отменен в связи с развитием полного клинического эффекта и изменениями в лабораторных анализах, которые нормализовались спустя неделю после отмены лечения. В течение последующих 12 месяцев пузыри отсутствовали, сохранялось периодическое появление единичных уртикароподобных элементов плоских папул.
Клинический случай 2
Пациент С., 87 лет, обратился с жалобами на зуд и высыпания на коже туловища и конечностей, возникшие в период лечения по поводу меланомы.
Из анамнеза известно, что в июле 2022 г. отметил быстрый рост новообразования на коже передней поверхности грудной клетки слева с изъязвлением, а также обнаружил появление опухолевого образования в толще мягких тканей левой подмышечной области. Проведено цитологическое исследование (мазок-отпечаток) образования на коже грудной клетки: картина соответствует пигментной меланоме. По результатам тонкоигольной аспирационной пункционной биопсии цитологическая картина образования левой подмышечной области соответствует метастазу пигментной меланомы в лимфоузел. При ПЭТ-КТ (от 18.08.2022 г.) обнаружено гиперметаболическое образование на коже передней поверхности грудной клетки слева, метастатическое поражение подмышечных лимфоузлов слева, умеренное повышение метаболической активности в надключичном лимфоузле слева, вероятно, метастатического генеза.
Проведено широкое иссечение опухоли кожи передней грудной стенки и подмышечная лимфодиссекция слева. При патоморфологическом исследовании верифицирована эпителиоидноклеточная пигментная меланома кожи (уровень инвазии по Кларку IV, толщина по Бреслоу 5,2 мм) с фокусами лимфоваскулярной инвазии (by1), изъязвлением эпидермиса, pT4bN3b. Выявлена мутация BRAF V600E.
С октября по декабрь 2022 г. проведено четыре курса терапии препаратом ниволумаб по 240 мг внутривенно один раз в 14 дней. В связи с мутационным статусом опухоли, прогрессированием заболевания на фоне иммунотерапии пациент был переведен на таргетную терапию дабрафенибом в дозе 150 мг/сут и траметинибом в дозе 2 мг/сут с 16.12.2022 г.
В январе 2023 г. в связи с эпизодами судорог в мышцах рук и ног, развитием общей слабости и головокружения терапия была приостановлена на один месяц. С 09.02.2023 по 27.02.2023 г. возобновление таргетной терапии дабрафенибом в дозе 150 мг/сут и траметинибом в дозе 2 мг/сут. 28.02.23 г. повторный приступ судорог в мышцах и слабость, в связи с чем пациент самостоятельно отменил прием препаратов, побочные эффекты разрешились. С 10.03.2023 г. отмена траметиниба, монотерапия дабрафенибом с постепенным увеличением суточной дозы до 300 мг/сут.
Вскоре после отмены траметиниба, в марте 2023 г., отметил появление пузырей на коже передних поверхностей бедер, в связи с чем терапия дабрафенибом была прервана. При ПЭТ-КТ от 29.04.2023 г. в сравнении с ПЭТ-КТ от 01.12.2022 г.: значительное уменьшение размеров, количества и уровня метаболической активности большинства очагов в костях скелета, печени, лимфоузлов (мезентериальных, внутригрудных, надключичного слева, подмышечных слева), регресс участков тяжистого уплотнения в легких с обеих сторон, повышение уровня метаболической активности очага в S7 печени, крестце и левой подвздошной кости – контроль в динамике, появление участков утолщения на коже с низким уровнем метаболической активности.
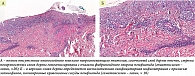
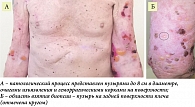
При обращении к дерматовенерологу 04.05.2023 г. жалобы на образование пузырей на коже туловища и конечностей, которые постепенно эрозировались и сопровождались выраженным болевым синдромом. При осмотре кожный патологический процесс носит распространенный симметричный островоспалительный характер, локализуется на коже туловища и конечностей, представлен эритемой, на фоне которой располагаются пузыри округлой формы с плотной покрышкой и серозно-геморрагическим содержимым, с дальнейшим образованием эрозий с серозно-геморрагическими корками на поверхности (рис. 4 А). Одновременно на коже правой надушной области выявлен метастаз меланомы, возникший, со слов пациента, незадолго до осмотра, и увеличивающийся в размере. Рекомендована консультация онколога.
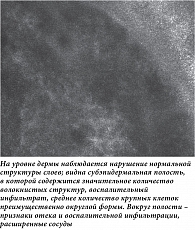
Для верификации диагноза произведена биопсия пузыря с сохранением дна, покрышки и содержимого с задней поверхности плеча (рис. 4 Б). Проведено патоморфологическое исследование (рис. 5). Обнаруженные признаки коррелировали с изменениями, выявленными при конфокальной лазерной сканирующей микроскопии (рис. 6). Проведено исследование сыворотки крови методом непрямой иммунофлуоресценции, антител к десмоглеинам первого и третьего типов не обнаружено, выявлены антитела к белкам BP180 (> 200,0 RU/мл), содержание антител к BP230 было диагностически не значимым (9,13 RU/мл при норме < 20 RU/мл).
Пациенту рекомендована приостановка противоопухолевой терапии, назначен преднизолон в дозе 40 мг в сутки семь дней, наружно – мазь клобетазола пропионата один раз в день, обработка пузырей местными антисептиками, с полным регрессом высыпаний и последующим переводом на системную терапию дапсоном в дозе 50 мг/сут с последующим повышением через неделю до 100 мг/сут. Был возобновлен прием таргетных препаратов, на фоне чего в последующем отмечалось появление небольшого количества пузырей, купированное наружным применением клобетазола пропионата и дапсона 100 мг/сут.
Обсуждение
В последние годы ингибиторы иммунных контрольных точек и таргетные препараты произвели революцию в лечении метастатической меланомы и в настоящее время одобрены или проходят клинические исследования при других злокачественных новообразованиях. Было показано, что ипилимумаб, ниволумаб и пембролизумаб увеличивают общую выживаемость, а комбинация ипилимумаба с ниволумабом может помочь в достижении уровня ответа опухоли на терапию до 60% у пациентов с метастатической меланомой [24]. Однако применение иммунотерапии и таргетной терапии в некоторых случаях сопровождается развитием различных специфических кожных токсических реакций, а также дерматозов, степень тяжести которых может варьировать от легкой до угрожающей жизни. В числе дерматозов, провоцированных иммунотерапевтическими препаратами, описан и буллезный пемфигоид. Его развитие приводит к снижению качества жизни пациентов и в некоторых случаях – к прекращению противоопухолевой терапии.
Манифестация БП более характерна для пациентов, получающих терапию ИКТ, нежели таргетную терапию. Развитие ИКТ-индуцированного БП, как правило, имеет отсроченный характер, в среднем первые проявления нежелательного явления манифестируют через четыре месяца после начала терапии ИКТ, а в некоторых случаях развиваются через полтора года терапии или даже после отмены ИКТ. Продромальные явления могут включать генерализованный зуд, за которым следует образование пятен или уртикароподобных папул, а затем напряженных пузырей на коже конечностей и туловища, заполненных серозной или геморрагической жидкостью. Вероятность вовлечения слизистой оболочки полости рта при ИКТ-индуцированном БП составляет, по разным данным, до 40%, в отличие от БП, не ассоциированного с приемом лекарственных средства, при котором слизистая оболочка вовлекается в патологический процесс только у 19% пациентов [25]. Вместе с тем необходимо учитывать возможность развития БП в рамках паранеопластического процесса, который может проявляться именно в виде одного из вариантов аутоиммунного буллезного дерматоза, в том числе БП. В литературе описано довольно много случаев паранеопластического БП при различных видах опухолей. Одной из особенностей развития такого паранеопластического дерматоза является взаимосвязь с активностью опухоли, таким образом активность аутоиммунного процесса может служить косвенным маркером прогрессирования или регресса опухоли [26]. Ряд исследователей при описании сложных случаев сочетания опухолей и паранеоплазий придерживаются концепции так называемого паранеопластического аутоиммунного мультиорганного синдрома (PAMS), в которой оценка патологических реакций и подход к лечению основаны на комплексном анализе аутоиммунных реакций [27]. В случае развития ИКТ-индуцированного БП для дифференциальной диагностики и понимания генеза БП и, следовательно, его эффективной терапии большое значение имеют анамнестические данные, иммунологическое обследование, а также анализ взаимосвязи с проводимой терапией опухоли. Понимание закономерностей развития аутоиммунных реакций, возникающих как следствие онкологического процесса или как следствие проводимой терапии опухоли, может не только помочь в выборе правильного подхода к лечению, но и в определении прогноза течения опухолевого процесса.
Несмотря на обширные исследования, специфические антигены при лекарственно-индуцированном БП так и не были выявлены. Поэтому считается, что аутоантигены, вовлеченные в патологический процесс, могут совпадать с антигенами при идиопатическом БП. Результаты исследований прямой и непрямой иммунофлуоресценции, как правило, схожи при лекарственно-индуцированном и идиопатическом БП. Типичные признаки, наблюдаемые при патоморфологическом исследовании биоптатов с очагов поражения лекарственно-индуцированного БП, включают наличие внутриэпидермальных пузырьков, некротизированных кератиноцитов и выраженного эозинофильного инфильтрата, иногда с образованием тромбов. Однако при идиопатическом БП обычно отсутствуют внутриэпидермальные везикулы, некротизированные кератиноциты и тромбы, а эозинофильный инфильтрат обычно выражен слабее. Выраженная эозинофилия в сыворотке крови часто наблюдается в случаях лекарственно-индуцированного БП [28, 29].
В то же время следует подчеркнуть, что буллезный пемфигоид, развивающийся на фоне противоопухолевой терапии, может иметь двоякую природу, которую иллюстрируют описанные случаи. Так, представлены наблюдения БП у женщины относительно молодого возраста с ремиссией меланомы, без других факторов риска развития БП, и БП у пациента пожилого возраста с прогрессирующей меланомой, находящегося в группе риска развития паранеопластического БП, который потенциально был запущен иммунотерапией. Это наблюдение позволило различить первичный лекарственный буллезный пемфигоид (истинно лекарственно-индуцированный БП, у пациентов без факторов риска развития БП, обусловленный иммунотерапией и вторичный лекарственный буллезный пемфигоид (БП у пациентов с высоким риском развития БП, у которых иммунотерапия послужила лишь дополнительным пусковым фактором). Сопоставление клинико-лабораторных особенностей данных форм заболевания обнаружило отличия по клиническим и лабораторным характеристикам (табл. 2).
Также обращает внимание тот факт, что провокация БП на фоне таргетной терапии отмечается крайне редко, что соотносится и с представленным наблюдением. В описанном случае буллезный пемфигоид дебютировал уже после редукции таргетной терапии в виде отмены траметиниба и перехода на монотерапию дабрафенибом (что делает маловероятной провоцирующую роль таргетных препаратов), спустя пять месяцев от начала иммунотерапии (что соответствует срокам развития БП, вызванного иммунотерапией, согласно данным литературы, и указывает на возможную провоцирующую роль иммунотерапии), и совпал с появлением нового метастаза меланомы на коже волосистой части головы (что свидетельствует в пользу паранеопластического генеза БП). Однако затем в описанном случае наблюдалось негативное влияние на течение уже имеющегося вторичного (паранеопластического) лекарственного БП. Возможно, негативное влияние связано с усилением выделения антигенов опухолью на фоне противоопухолевой терапии.
Заключение
Буллезный пемфигоид, ассоциированный с применением новейших представителей противоопухолевых препаратов, – довольно редкое явление, поражающее, по разным данным, до 3,8% пациентов, находящихся на терапии ИКТ. По сравнению с другими дерматологическими иммуноопосредованными нежелательными явлениями БП имеет более позднее начало, кроме того, БП может возникнуть даже после прекращения противоопухолевой терапии. Своевременное распознавание признаков БП, ассоциированного с противоопухолевыми препаратами, необходимо для оптимизации лечения и улучшения результатов ответа опухоли на терапию. Дифференциация первичного и вторичного лекарственного БП позволит оптимизировать тактику ведения пациента, обеспечить индивидуальный подход и прогнозировать последующее течение заболевания кожи.
Дополнительная информация
Пациенты добровольно подписали форму информированного согласия на публикацию персональной медицинской информации в обезличенной форме, а также на передачу электронной копии подписанной формы информированного согласия сотрудникам редакции журнала.
Источник финансирования
Авторы заявляют об отсутствии внешнего финансирования при проведении исследования и подготовке публикации.
Конфликт интересов
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с проведенным исследованием и публикацией настоящей статьи.
A.V. Michenko, PhD, E.A. Shatokhina, PhD, Prof., L.S. Kruglova, PhD, Prof., A.N. Lvov, PhD, Prof., A.S. Allenova, PhD, A.G. Tsaregorodtseva, A.Yu. Syryseva, O.G. Pyagay, N.V. Danilova, PhD, L.P. Veshkina
Central State Medical Academy of Department of Presidential Affairs, Moscow
Medical Scientific and Educational Institute of Lomonosov Moscow State University, Moscow
International Institute of Psychosomatic Health, Moscow
Institute of Plastic Surgery and Cosmetology, Moscow
I.M. Sechenov First Moscow State Medical University
Skin and Venereological Dispensary No 9, St. Petersburg
Moscow City Oncological Hospital No 62
Contact person: Anna Valentinovna Michenko, amichenko@mail.ru
Bullous pemphigoid (BP) is a chronic bullous disease characterized by the formation of blisters on the skin and mucous membranes. The association of PD and concomitant diseases, in particular internal malignancies, has been studied with conflicting results. However, in the literature there is a clear relationship between the development of PD as an adverse immune-mediated phenomenon observed in patients treated with immune checkpoint inhibitors.
Aim. This work was a comparative description of clinical (itching, rash), dermatoscopic, laboratory (eosinophils, antibodies to BP180 and BP220), pathomorphological and confocal microscopic features of bullous pemphigoid in patients receiving antitumor therapy.
Material and methods. Two patients with bullous pemphigoid receiving treatment for melanoma are presented. Primary and secondary drug-induced bullous pemphigoid are identified, described in detail and compared. The features of primary drug-induced PD are shown (younger age of onset, remission of melanoma, clinical picture of non-inflammatory PD with milder itching, rashes in the form of papules with punctate or stellate erosion in the center, detection of antibodies BP180 and BP230, normal content of eosinophils in the blood, reduced eosinophils in the biopsy specimen, more favorable course after discontinuation of the triggering drug) and drug-induced (paraneoplastic in our case) PD (older age of onset, progression of melanoma, clinically classic symptoms of PD with more intense itching, papules with a smooth surface, detection of antibodies to BP180 in the blood, increased levels of eosinophils in the blood, moderate eosinophil content in the infiltrate , persistence of PD after discontinuation of the triggering drug).
Conclusion. It is emphasized that the most likely trigger of PD was immunotherapeutic drugs. Targeted antitumor therapy was unlikely to be a significant provoking or inducing factor for PD, although one can expect their influence on the course of paraneoplastic bullous pemphigoid, possibly due to increased release of antigens by the tumor during antitumor therapy.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.