Прогностические факторы достижения целевых значений гликемического контроля у пациентов с сахарным диабетом 2 типа, получавших инсулин гларгин (результаты исследования реальной клинической практики SERENITY)
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. В исследование было включено 5395 пациентов, соответствовавших критериям включения/исключения: 1792 мужчины (средний возраст – 57,5 ± 9,5 года) и 3603 женщины (средний возраст – 61,0 ± 9,3 года).
Первичная конечная точка – клинические и неклинические факторы, связанные с достижением индивидуальных целевых значений HbA1c через 12 месяцев.
Результаты. Выявлена связь между достижением целевого уровня HbA1c и такими параметрами, как возраст больных, индекс массы тела (31,4 ± 5,2 vs 32,2 ± 5,4 кг/м2), исходные уровни HbA1c, глюкозы плазмы натощак (ГПН), постпрандиальной гликемии (ППГ) (p < 0,001). Доля пациентов, достигших индивидуальных целевых значений HbA1c через три, шесть и 12 месяцев после включения в исследование, была выше, чем доля пациентов, достигших HbA1c менее 7,0 и 6,5%.
Общее число нежелательных явлений составило 1,06%. На суммарную частоту эпизодов симптоматической гипогликемии приходилось 0,61%. Ни один из таких эпизодов не был связан с введением инсулина гларгин. Другие нежелательные реакции также не были связаны с инсулинотерапией.
Выводы. Наиболее значимыми прогностическими факторами достижения индивидуальных целевых значений HbA1c являются более низкие исходные значения HbA1c, ГПН и ППГ, более низкая масса тела и участие в образовательных программах, посвященных сахарному диабету.
У большинства пациентов перевод/добавление инсулина гларгин к предшествующей сахароснижающей терапии способствует улучшению гликемического контроля при низкой частоте эпизодов гипогликемии и отсутствии увеличения массы тела.
Материал и методы. В исследование было включено 5395 пациентов, соответствовавших критериям включения/исключения: 1792 мужчины (средний возраст – 57,5 ± 9,5 года) и 3603 женщины (средний возраст – 61,0 ± 9,3 года).
Первичная конечная точка – клинические и неклинические факторы, связанные с достижением индивидуальных целевых значений HbA1c через 12 месяцев.
Результаты. Выявлена связь между достижением целевого уровня HbA1c и такими параметрами, как возраст больных, индекс массы тела (31,4 ± 5,2 vs 32,2 ± 5,4 кг/м2), исходные уровни HbA1c, глюкозы плазмы натощак (ГПН), постпрандиальной гликемии (ППГ) (p < 0,001). Доля пациентов, достигших индивидуальных целевых значений HbA1c через три, шесть и 12 месяцев после включения в исследование, была выше, чем доля пациентов, достигших HbA1c менее 7,0 и 6,5%.
Общее число нежелательных явлений составило 1,06%. На суммарную частоту эпизодов симптоматической гипогликемии приходилось 0,61%. Ни один из таких эпизодов не был связан с введением инсулина гларгин. Другие нежелательные реакции также не были связаны с инсулинотерапией.
Выводы. Наиболее значимыми прогностическими факторами достижения индивидуальных целевых значений HbA1c являются более низкие исходные значения HbA1c, ГПН и ППГ, более низкая масса тела и участие в образовательных программах, посвященных сахарному диабету.
У большинства пациентов перевод/добавление инсулина гларгин к предшествующей сахароснижающей терапии способствует улучшению гликемического контроля при низкой частоте эпизодов гипогликемии и отсутствии увеличения массы тела.



Введение
Сахарный диабет (СД) 2 типа – хроническое заболевание, характеризующееся гипергликемией вследствие множественных патогенетических дефектов, основными из которых считаются дисфункция бета-клеток поджелудочной железы и инсулинорезистентность [1]. В большинстве случаев терапию начинают с модификации образа жизни и приема пероральных сахароснижающих препаратов (ПССП) или агонистов рецепторов глюкагоноподобного пептида 1. Однако со временем в связи с прогрессирующим снижением функции бета-клеток для достижения и поддержания индивидуального целевого уровня гликированного гемоглобина (HbA1c) пациентам с СД 2 типа требуется назначение инсулина.
Эффективность и безопасность инсулина гларгин были изучены в многочисленных рандомизированных клинических исследованиях (РКИ) и метаанализах. Их результаты подтвердили, что инсулин гларгин при сопоставимой с НПХ-инсулином эффективности обладает лучшим профилем безопасности, в частности в отношении частоты гипогликемий [2–4]. Вместе с тем, несмотря на жесткость протоколов РКИ, доля пациентов, достигших стандартного целевого значения HbA1c (< 7%) при инициации инсулинотерапии, составляла практически 60%, в реальной клинической практике она была значительно ниже. При недостижении целевых значений HbA1c после инициации того или иного режима инсулинотерапии пациентов, как правило, переводят на другой инсулин или на другой режим его введения. Установлено, что перевод пациентов, не достигших целевого уровня HbA1c на терапии ПССП и НПХ-инсулином, на терапию инсулином гларгин [5] или инсулином детемир [6] приводило к улучшению гликемического контроля.
Согласно рекомендациям экспертов Американской диабетической ассоциации/Европейской ассоциации по изучению диабета, переходить с монотерапии на более сложные схемы лечения, включающие применение инсулина, следует при невозможности достичь целевых значений гликемического контроля в течение шести месяцев терапии. Эксперты Российской диабетической ассоциации указывают на то, что своевременная интенсификация сахароснижающей терапии, в том числе инсулином, способствует значительному улучшению гликемического контроля у пациентов с СД 2 типа.
Прогностические факторы достижения стандартного целевого уровня HbA1c у пациентов при инициации базальной инсулинотерапии определялись при проведении субанализов результатов РКИ и ретроспективных наблюдательных исследований [7–13]. Однако отсутствуют данные о прогностических факторах достижения не стандартного, а индивидуального уровня HbA1c не только после инициации, но и после перевода пациентов на инсулин гларгин.
Нами было проведено многоцентровое наблюдательное проспективное исследование SERENITY. Протокол исследования (версия № 2 от 03.12.2014) одобрен 12 декабря 2014 г. Независимым междисциплинарным комитетом по этической экспертизе клинических исследований.
Целью исследования стало определение в условиях реальной клинической практики прогностических факторов, ассоциированных с достижением индивидуальных целевых значений гликемического контроля у пациентов с СД 2 типа, получавших инсулин гларгин.
Материал и методы
Исследование проводилось в 498 центрах Российской Федерации с декабря 2014 г. по июль 2016 г.
Для участия в исследовании были выбраны активно практикующие эндокринологи амбулаторных отделений из семи крупнейших федеральных округов. Во избежание систематической ошибки при отборе каждый врач должен был последовательно включить в исследование 10–11 пациентов, соответствующих критериям включения/исключения.
Критерии включения:
- мужчины и женщины c СД 2 типа старше 18 лет, в том числе пациенты старше 60 лет;
- решение о необходимости назначения инсулина гларгин в качестве дополнения к ПССП или в качестве коррекции проводившейся ранее инсулинотерапии;
- HbA1c более 7 и менее 10%;
- подписанное информированное согласие на участие в исследовании.
Критерии исключения:
- СД 1 типа;
- беременность или период лактации;
- гиперчувствительность к инсулину гларгин в анамнезе;
- любые клинически значимые тяжелые заболевания внутренних органов или системные заболевания, которые могут затруднить интерпретацию результатов;
- невозможность или нежелание пациентов должным образом проводить самоконтроль/титровать дозу инсулина.
Все терапевтические и диагностические процедуры были проведены в соответствии со стандартной клинической практикой [14].
Процедуры, выходящие за рамки стандартной клинической практики, не проводились, за исключением сбора данных в соответствии с индивидуальной регистрационной картой.
Для каждого пациента продолжительность исследования составляла 12 месяцев.
Дизайн исследования предусматривал пять визитов: первый визит – скрининг/включение в исследование, второй – пятый – наблюдение через три, шесть, девять и 12 месяцев соответственно.
После включения в исследование все пациенты получали инсулин гларгин 100 ЕД/мл (Лантус СолоСтар) в качестве дополнения к ПССП или коррекции проводившейся ранее инсулинотерапии.
Решение о стартовой дозе и дальнейшем алгоритме титрации принималось врачом в соответствии с существующими рекомендациями [15] и клинической практикой.
В качестве первичных конечных точек/исходов исследования были выбраны клинические и неклинические параметры, которые могли оказать влияние на достижение или недостижение целевых значений HbA1c через 12 месяцев от начала терапии инсулином гларгин. К таковым относятся:
- антропометрические характеристики (возраст, пол, масса тела);
- параметры гликемического контроля (исходное значение HbA1c, глюкозы плазмы натощак (ГПН) и постпрандиальной гликемии (ППГ));
- данные анамнеза (длительность СД, наличие поздних осложнений, предшествующая сахароснижающая терапия);
- доза инсулина гларгин исходно и через 12 месяцев;
- участие в образовательных программах для пациентов с сахарным диабетом;
- социально-экономический профиль пациентов (образование, трудоустроенность).
Вторичные конечные точки/исходы исследования – динамика уровня HbA1c, ГПН и ППГ, дозы инсулина гларгин, массы тела, частота гипогликемий и нежелательных/серьезных побочных эффектов через три, шесть и 12 месяцев, проведение титрации дозы препарата пациентом.
Под симптоматической гипогликемией понимали состояние, сопровождавшееся типичными симптомами и подтвержденное измерением глюкозы плазмы ≤ 3,9 ммоль/л, или купирование симптоматики после перорального приема углеводов/инъекции глюкагона при невозможности измерить уровень гликемии. Под тяжелой симптоматической гипогликемией подразумевали событие, сопровождавшееся типичными симптомами и подтвержденное (при возможности измерения) уровнем глюкозы плазмы < 2,0 ммоль/л, потребовавшее помощи другого лица для купирования симптомов (пероральный прием углеводов, инъекция глюкагона или внутривенное введение раствора глюкозы), с купированием неврологической симптоматики после перорального приема углеводов, инъекции глюкагона или внутривенного введения раствора глюкозы. Под ночной гипогликемией – событие, развившееся во время сна (после отхода ко сну и до пробуждения). Сбор информации о гипогликемических событиях проводился на основании анализа дневников самоконтроля/данных глюкометров пациентов.
Вся информация отражалась в разработанной в соответствии с целями и задачами исследования индивидуальной регистрационной карте пациента.
Факторы оценивали преимущественно по долям. Максимально высокая ожидаемая доля составляла 50%. Для анализа использовали следующую формулу [16]:
n = Z2 × P × (1 - P) : d2,
где n – размер выборки;
Z – статистика для доверительного интервала;
P – ожидаемая доля;
d – точность.
Для стандартного 95%-ного доверительного интервала (ДИ) значение Z составило 1,96. Ширина ДИ была в два раза больше точности – 2d.
Исследуемые группы разделили по длительности заболевания (три подгруппы) и исходному значению HbA1c (три подгруппы).
Размер выборки (554 пациента) обеспечивал мощность 90% для оценки доли 50 ± 10% при двустороннем уровне значимости 0,05 в одной исследуемой группе. Таким образом, общее число пациентов достигло 4986 (554 пациента × 9 исследуемых подгрупп). При учете 10%-ного выбывания общее число пациентов составило 5484 (округлено до 5500).
Статистический анализ проводили с помощью программного обеспечения SAS 9.3. Анализ нормально распределенных переменных – параметрических методов (ANOVA, t-критерий Стьюдента), в других случаях – непараметрических методов (критерии Вилкоксона и Манна – Уитни).
Для сравнения качественных переменных использовали хи-квадрат Пирсона и точный двусторонний критерий Фишера. Количественные параметры, соответствовавшие нормальному распределению, описаны как среднее значение и стандартное отклонение (M ± SD), параметры, не соответствовавшие нормальному распределению, – как медиана, 25%-ный и 75%-ный квартили (Me [25%; 75%]). Качественные параметры представлены как процент от абсолютного значения. Различия считали статистически значимыми при р < 0,05.
Результаты
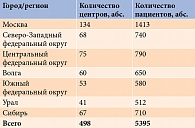
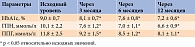
В исследование были включены 5395 пациентов из различных регионов Российской Федерации (табл. 1).
Из исследования выбыли 74 (1,4%) пациента: потеря связи с пациентом – 50/5395 (0,93%), отказ пациента от продолжения участия в исследовании – 14/5395 (0,26%), невозможность продолжения участия из-за логистических соображений – 7/5395 (0,13%), изменение терапии – 2/5395 (0,04%), развитие ночной гипогликемии – 1/5395 (0,02%).
Средний возраст пациентов, включенных в исследование, составил 59,8 ± 9,5 года, длительность СД – 7,8 [4,7; 12,1] года, индекс массы тела (ИМТ) – 31,9 ± 5,3 кг/м2 (табл. 2).
ПССП получали 3563 (66%) пациента, ПССП в комбинации с базальным инсулином – 1057 (20%). Остальные 14% больных находились на базис-болюсной инсулинотерапии или терапии смешанными инсулинами, иногда в комбинации с ПССП (см. табл. 2).
Пациентов трудоспособного и пенсионного возраста было большинство – 43,6 и 43,6% соответственно. Меньшую долю составляли нетрудоспособные – 12%, студенты – 0,1% и безработные – 0,6%.
О незаконченном среднем образовании сообщили 74 (1,4%) участника исследования. Среднее или среднее специальное образование получили 2897 (53,7%) пациентов, высшее образование – 2424 (44,9%) пациента.
Низкий уровень дохода имел место у 1187 (22,0%) пациентов, средний – у 3988 (73,9%), высокий – у 218 (4,0%) больных. В отношении 0,1% пациентов данные отсутствовали.
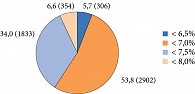
Индивидуальное целевое значение HbA1c для каждого пациента определяли исходя из алгоритмов, разработанных экспертами Российской ассоциации эндокринологов [14]. Распределение участников исследования в зависимости от индивидуальных целевых значений HbA1c представлено на рис. 1.
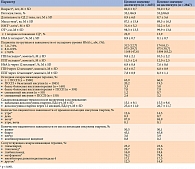
Оценка прогностических факторов. Через 12 месяцев около половины (46,3%) пациентов достигли целевых значений HbA1c. Эти пациенты исходно были незначительно старше, имели более низкую массу тела и меньшую окружность талии (ОТ). Необходимо отметить, что у пациентов данной группы исходно были статистически значимо более низкие средние значения уровней HbA1c, ГПН, ППГ (табл. 3), хотя с клинической точки зрения эта разница не представляется существенной. Кроме того, и по завершении исследования у них были зарегистрированы значительно более низкие уровни HbA1c, ГПН, ППГ (p < 0,001) (см. табл. 3), чем у пациентов, не достигших целей лечения. Необходимо отметить, что в обеих группах на фоне лечения отмечено улучшение гликемического контроля.
Исходный уровень HbA1c был одним из основных прогностических факторов достижения рекомендованной цели лечения: в группе с исходным уровнем HbA1c 7,0–7,9% доля пациентов, достигших целевого значения HbA1c, составила 64,4%, в то время как в группах с исходным уровнем HbA1c 8,0–8,9% и HbA1c ≥ 9,0% – 52,6 и 39,3% соответственно (p < 0,001). Наличие/отсутствие поздних осложнений сахарного диабета также ассоциировалось с достижением цели лечения. В то же время связь достижения целевых значений гликемии с длительностью заболевания и предшествующей сахароснижающей терапией не прослеживалась (см. табл. 3).
В отношении сахароснижающей терапии значимые различия между группами в стартовой и конечной дозах инсулина гларгин, области инъекций инсулина, сопутствующих препаратах отсутствовали. Однако в группе, достигшей рекомендованных целей лечения, доля пациентов, вводивших инсулин гларгин перед сном, была выше (см. табл. 3).
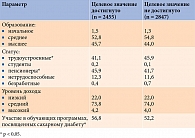
Анализ социально-экономического положения пациентов показал, что среди достигших целей лечения было меньше трудоустроенных и больше неработающих пенсионеров, при этом в обеих группах уровень дохода был сопоставимым.
Кроме того, среди достигших индивидуальных целевых значений HbA1c было больше пациентов, участвовавших в разных обучающих программах, посвященных сахарному диабету, – 56,8 vs 52,2% (р < 0,05) (табл. 4).
Анализ эффективности. После перевода пациентов на инсулин гларгин средний уровень HbA1с снизился с 9,3 ± 0,7 до 8,1 ± 0,7% к третьему месяцу, до 7,6 ± 0,8% к шестому и до 7,2 ± 0,6% к 12-му месяцу (см. рис. 1), что было ассоциировано со снижением как ГПН, так и ППГ (p < 0,05 для всех параметров относительно исходных значений) (табл. 5). При этом улучшение гликемического контроля отмечено у всех пациентов независимо от исходной сахароснижающей терапии.
Необходимо еще раз подчеркнуть, что снижение уровней HbA1c, ГПН и ППГ на фоне терапии инсулином гларгин отмечено в обеих группах пациентов, как достигших, так и не достигших рекомендованных целей лечения. Однако значения всех параметров углеводного обмена через 12 месяцев были статистически значимо ниже в первой группе (см. табл. 3).
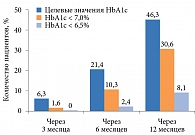
С клинической точки зрения большую значимость имеет не столько снижение уровня HbA1c, сколько достижение целевых значений. Так, доли пациентов, достигших индивидуальных целевых значений HbA1c через три, шесть и 12 месяцев, составили 6,3, 21,4 и 46,3% соответственно. Уровня HbA1c < 7% через три, шесть и 12 месяцев лечения достигли 1,6, 10,3 и 30,6% пациентов соответственно. Количество пациентов, достигших уровня HbA1c < 6,5%, было еще меньше. Через три месяца терапии ни один из пациентов не достиг этого значения, через шесть и 12 месяцев – 2,3 и 8,1% соответственно (рис. 2). Это означает, что достижение индивидуальных целевых значений значительно отличается от достижения стандартных значений HbA1c и в большей степени определяет эффективность гликемического контроля. Вместе с тем более половины пациентов не достигли рекомендованных целей терапии через один год после модификации лечения.
Самостоятельно титровали дозу инсулина гларгин 93,6% пациентов, что свидетельствует о достаточно простом и понятном алгоритме титрации. Через 12 месяцев отмечено статистически значимое повышение дозы инсулина гларгин относительно исходной у 89,1% пациентов. У 7,1% больных таковая не изменилась, у 3,8% – зарегистрировано ее снижение. Через 12 месяцев статистически значимых различий в средних суточных дозах инсулина гларгин между группой пациентов, достигших целевых значений HbA1c, и группой пациентов, которые не достигли целей лечения, не отмечено (см. табл. 3).
Достижение целей лечения было ассоциировано с введением инсулина гларгин перед сном.
Необходимо подчеркнуть, что средняя суточная доза инсулина гларгин через 12 месяцев была значительно ниже средних доз, вводимых аналогичной выборке пациентов с СД 2 типа в клинических исследованиях длительностью шесть месяцев.
Динамика массы тела. После перевода пациентов на инсулин гларгин к 12-му месяцу терапии в общей когорте пациентов отмечено незначительное снижение массы тела с 88,1 ± 16,0 до 87,7 ± 15,2 кг (р < 0,05) и уменьшение ОТ с 99,3 ± 13,6 до 97,8 ± 13,1 см (р < 0,05).
При более подробном анализе установлено, что через 12 месяцев терапии снижение или сохранение исходной массы тела было зарегистрировано практически у 61,6% пациентов. Увеличение массы тела наблюдалось у 38,4% больных, ОТ – у 23,7%.
Несмотря на одинаковые дозы инсулина в обеих группах, повышение массы тела отмечалось преимущественно у женщин, пациентов более старшего возраста и с более низким ИМТ (табл. 6).
Гипогликемии и другие нежелательные эффекты. В течение 12 месяцев бессимптомные и симптоматические гипогликемии были зарегистрированы у небольшого числа пациентов при очень низкой частоте эпизодов на одного пациента в месяц. Однократные эпизоды ночной гипогликемии были зафиксированы через три и 12 месяцев и один эпизод тяжелой гипогликемии – через три месяца (табл. 7). Проанализировать взаимосвязь между частотой и типом эпизодов гипогликемии, а также клиническими и иными характеристиками пациентов не представлялось возможным вследствие низкой частоты таковых.
Общее число нежелательных явлений, включая симптоматическую гипогликемию, составило 57/5395 (1,06%). Суммарная частота эпизодов симптоматической гипогликемии – 0,61%.
Ни один из эпизодов, по мнению лечащих врачей, не был связан с введением инсулина гларгин. Единственный эпизод тяжелой гипогликемии, зарегистрированный во время исследования, также не был обусловлен проводившейся терапией и не привел к отмене препарата.
Вместе с тем один из пациентов был выведен из исследования из-за высокого риска развития ночной гипогликемии.
Другие нежелательные явления, в частности вирусные инфекции верхних дыхательных путей, назофарингиты, эпизоды повышения артериального давления, обострение бронхиальной астмы, также не были связаны с терапией инсулином гларгин.
Обсуждение результатов
Результаты 12-месячного многоцентрового наблюдательного исследования SERENITY продемонстрировали, что основными значимыми прогностическими факторами достижения целевых значений HbA1c через 12 месяцев от начала терапии инсулином являются возраст пациентов, исходные значения уровня HbA1c, ГПН, ППГ, а также ИМТ и ОТ.
В исследовании SERENITY инициация инсулинотерапии, а также смена препарата инсулина/режима инсулинотерапии привела к улучшению гликемического контроля у всех пациентов. Однако достижение индивидуальных целевых значений гликемического контроля было более вероятно у пациентов с исходно более низким уровнем HbA1c (8,9 ± 0,7 vs 9,1 ± 0,7%), а также более низкими значениями ГПН (9,8 ± 2,1 vs 10,3 ± 2,2 ммоль/л) и ППГ (11,5 ± 2,4 vs 12,0 ± 2,5 ммоль/л).
Исходный уровень HbA1c был назван основным предиктором достижения целей лечения при инициации базальной инсулинотерапии в целом ряде исследований [8, 10, 11]. Это подтверждает необходимость своевременно изменять схемы сахароснижающей терапии.
Пациенты, достигшие индивидуальных целей лечения, были старше (60,8 ± 9,8 vs 59,0 ± 9,2 года), что, возможно, определяло более высокие индивидуальные целевые значения гликемического контроля и, следовательно, большую вероятность их достижения. Это косвенно подтверждается тем фактом, что в группе достигших целей лечения было больше лиц с поздними осложнениями сахарного диабета. Последние сложно расценивать как прогностический фактор достижения индивидуальных значений гликемии, скорее это косвенный признак менее жестких целей лечения.
Следует отметить, что количество пациентов, достигших индивидуальных целевых значений HbA1c, было больше, чем пациентов, достигших стандартных уровней (< 7,0 и < 6,5%). Это объясняется тем, что практически у половины больных были более высокие целевые значения.
Применение стратифицированных индивидуальных целевых значений HbA1c позволяет объективно оценить эффективность терапии у конкретного пациента. В нашем исследовании, несмотря на улучшение гликемического контроля, отмеченное у всех пациентов после перехода на инсулин гларгин, а также стратификацию целей лечения, через 12 месяцев индивидуальных целей лечения достигли менее половины пациентов.
Более 90% пациентов самостоятельно проводили титрацию дозы инсулина, что свидетельствует о простоте применения препарата.
Средние дозы инсулина гларгин через 12 месяцев между группами пациентов, достигших/не достигших целевых значений HbA1c, не различались и были более низкими, чем в РКИ, проведенных в аналогичной популяции больных.
Ни стартовая доза инсулина гларгин, ни финальная не были прогностическими факторами достижения целевых значений HbA1c.
Ограничения исследования
Исследование SERENITY, как и все наблюдательные исследования, имело ряд ограничений, что прежде всего может быть обусловлено качеством и полнотой собранных данных [17]. В частности, в ходе исследования зарегистрирована достаточно низкая частота гипогликемических эпизодов и нежелательных явлений, что может свидетельствовать о недостаточной фиксации этих событий как врачами, так и пациентами.
Не предполагалось также использование центральной лаборатории. Лабораторные исследования проводились в локальных лабораториях, определение параметров исходно и в динамике – в одной и той же лаборатории.
Выводы
Наиболее значимыми прогностическими факторами достижения индивидуальных целевых значений HbA1c после перевода пациентов на терапию инсулином гларгин являются более низкие исходные значения HbA1c, ГПН и ППГ и более низкая масса тела.
В целом независимо от предшествующей сахароснижающей терапии перевод на инсулин гларгин или его добавление приводит к улучшению гликемического контроля при низкой частоте эпизодов гипогликемии. У большинства пациентов такая терапия не сопровождается увеличением массы тела.
Источники финансирования
Исследование проведено при поддержке компании «Санофи».
Конфликт интересов
Нет конфликта интересов.
Благодарность
Искренняя признательность врачам и пациентам, без которых проведение исследования было бы невозможным.
I.V. Glinkina
I.M. Sechenov First Moscow State Medical University
Contact person: Irina Vladimirovna Glinkina, irina_glinkina@rambler.ru
The Purpose of the Study: define clinical and non-clinical predictive factors associated with achieving glycaemic goal (HbA1c as targeted by the treating physician) in people with diabetes mellitus type 2 (T2DM) for whom an adjunct therapy with insulin was appropriate or an adjustment of the current insulin therapy was required.
Material and Methods. The study included 5395 patients meeting the inclusion/exclusion criteria: 1792 males (mean age – 57.5 ± 9.5 years) and 3603 females (mean age – 61.0 ± 9.3 years). Primary end-point: clinical and non-clinical parameters associated with achieving individually targeted HbA1c after 12 months.
Results. In this study patients who achieved individually targeted HbA1c after 12 months after insulin glargine U100 initiation were older, had a higher body weight (BMI 31.4 ± 5.2 vs 32.2 ± 5.4), lower baseline HbA1c, FPG, PPG (p < 0.001). The percentage of patients at 3, 6 and 12 months of observation reaching individual HbA1c target was much higher than in those who achieved HbA1c < 7% and < 6.5%. The total rate of AEs was 1.06%. The rate of hypoglycemia was 35/5395 (0.65%). The rate of symptomatic hypoglycemia was 0.61%, and no one of them was associated with insulin glargine treatment as per physician opinion. Other cases of AEs were not associated with insulin glargine treatment.
Conclusions. Among all investigated clinical and non-clinical parameters only three factors identified to be significantly associated with individual HbA1c target achievement in patients with T2DM treated with insulin glargine U100 in real clinical practice: older age, lower BMI and lower WC at baseline; lower HbA1c, FPG and PPG at baseline.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.