Улучшение перинатальных исходов на фоне применения антиагрегантов и гепарина при хронической болезни почек разных стадий
- Аннотация
- Статья
- Ссылки
- English
Материал и методы. В исследование включены 66 женщин с ХБП (40 пациенток с ХБП первой стадии, восемь – с ХБП второй стадии, 18 – с ХБП третьей стадии), имевшие в анамнезе желанные беременности. Выбранная группа женщин рассматривалась и как исследуемая, и как контрольная группа. Всего оценивались исходы 185 желанных беременностей. Были ретроспективно проанализированы исходы 117 анамнестических беременностей без использования антикоагулянтов и антиагрегантов (контрольная группа). Проспективно наблюдали за течением и исходом последующих 68 беременностей у тех же пациенток на фоне применения гепарина и дипиридамола (две пациентки вынашивали две последние беременности на фоне приема гепарина и антиагрегантов) (исследуемая группа). Гепарин и дипиридамол назначались с целью профилактики преэклампсии и фетоплацентарной недостаточности.
Результаты. В исследуемой группе частота благоприятных исходов беременности была достоверно выше по сравнению с группой контроля – 66 из 68 (97,1%) против 58 из 117 (49,6%), p < 0,001. Никому из пациенток не потребовалась постоянная заместительная почечная терапия в течение 12 месяцев после родов. Улучшение исходов беременности наблюдалось у всех женщин вне зависимости от стадии ХБП.
Выводы. При ХБП первой – третьей стадии применение гепарина и дипиридамола способствовало повышению частоты благоприятных исходов беременности – рождению живых детей и выживанию их в постнатальном периоде без значимого ухудшения почечной функции у матерей в течение года наблюдения после родов.
Материал и методы. В исследование включены 66 женщин с ХБП (40 пациенток с ХБП первой стадии, восемь – с ХБП второй стадии, 18 – с ХБП третьей стадии), имевшие в анамнезе желанные беременности. Выбранная группа женщин рассматривалась и как исследуемая, и как контрольная группа. Всего оценивались исходы 185 желанных беременностей. Были ретроспективно проанализированы исходы 117 анамнестических беременностей без использования антикоагулянтов и антиагрегантов (контрольная группа). Проспективно наблюдали за течением и исходом последующих 68 беременностей у тех же пациенток на фоне применения гепарина и дипиридамола (две пациентки вынашивали две последние беременности на фоне приема гепарина и антиагрегантов) (исследуемая группа). Гепарин и дипиридамол назначались с целью профилактики преэклампсии и фетоплацентарной недостаточности.
Результаты. В исследуемой группе частота благоприятных исходов беременности была достоверно выше по сравнению с группой контроля – 66 из 68 (97,1%) против 58 из 117 (49,6%), p < 0,001. Никому из пациенток не потребовалась постоянная заместительная почечная терапия в течение 12 месяцев после родов. Улучшение исходов беременности наблюдалось у всех женщин вне зависимости от стадии ХБП.
Выводы. При ХБП первой – третьей стадии применение гепарина и дипиридамола способствовало повышению частоты благоприятных исходов беременности – рождению живых детей и выживанию их в постнатальном периоде без значимого ухудшения почечной функции у матерей в течение года наблюдения после родов.



Актуальность
Вероятность неблагоприятного исхода беременности у пациенток с хронической болезнью почек (ХБП) выше, чем в общей популяции, из-за повышенной частоты акушерских и перинатальных осложнений: преэклампсии, внутриутробной задержки роста плода, его антенатальной, интранатальной или постнатальной гибели, преждевременной отслойки нормально расположенной плаценты, поздними потерями беременности. Причем риск такого исхода и для плода, и для матери нарастает по мере ухудшения функции почек [1, 2]. Несмотря на это, в настоящее время вероятность успешной беременности достаточно высока даже у женщин с хронической почечной недостаточностью (преимущественно ХБП третьей стадии, когда скорость клубочковой фильтрации составляет 30–59 мл/мин), особенно при соблюдении следующих условий: планирование беременности, интенсивное наблюдение командой специалистов, активная профилактика осложнений [2–6].
Преэклампсия – одно из наиболее грозных осложнений беременности – развивается после 16–18 недель гестации и проявляется артериальной гипертензией и протеинурией. Важнейшим патогенетическим механизмом преэклампсии служит дисбаланс ангиогенных и антиангиогенных факторов: снижение уровня фактора роста сосудистого эндотелия (vascular endothelial growth factor – VEGF) и повышение уровня его растворимых рецепторов (soluble fms-like tyrosine kinase-1 – sFlt1). Нарушение баланса приводит к неполноценной имплантации, снижению глубины инвазии трофобласта в спиральные артерии матки с последующим нарушением маточно-плацентарного и плодово-плацентарного кровотока. У пациенток с преэклампсией нарушение баланса между ангиогенными и антиангиогенными факторами имеет взаимосвязь с поражением почек: установлена обратная корреляция между скоростью клубочковой фильтрации и sFlt-1 и прямая – между скоростью клубочковой фильтрации и VEGF [7].
Патологические процессы, приводящие к преэклампсии, начинаются задолго до появления клинических симптомов. Развернутая клиническая картина преэклампсии всегда свидетельствует о достаточно глубоком поражении органов и систем. Эффективной терапии преэклампсии в настоящее время не существует, обычно беременность прерывают, в том числе и на таких сроках гестации, когда шансы новорожденного на выживание минимальны.
С одной стороны, частота развития преэклампсии увеличивается у женщин с ХБП по мере ухудшения почечной функции, достигая 40% при уровне креатинина сыворотки 125–180 мкмоль/л и 60% и более – при значениях этого показателя выше 180 мкмоль/л [6]. С другой стороны, риск развития ХБП повышен у женщин, ранее перенесших преэклампсию, а острое почечное повреждение вследствие преэклампсии может существенно ускорить прогрессирование почечной недостаточности у женщин с ХБП. Эти явления отчасти можно объяснить общими патогенетическими механизмами ХБП и преэклампсии – дисбалансом ангиогенных и антиангиогенных факторов, а также нарушением регуляции ренин-ангиотензин-альдостероновой системы [8].
Отсроченное развитие клинической симптоматики и отсутствие действенных методов лечения диктуют необходимость поиска эффективной профилактики преэклампсии. С этой целью широко используются антитромбоцитарные препараты. Описано успешное применение комбинации ацетилсалициловой кислоты и дипиридамола у женщин с заболеваниями почек [9]. По данным крупного систематического обзора, включившего более 32 000 пациенток с высоким риском преэклампсии, прием антитромбоцитарных препаратов (аспирина в низких дозах или дипиридамола) снижал риск преэклампсии, родов до 37 недель гестации и смерти новорожденных [10]. Однако необходимо подчеркнуть, что аспирин может назначаться только со второго триместра беременности, тогда как дипиридамол разрешен к применению в любые сроки гестации.
При высоком риске преэклампсии применяются и прямые антикоагулянты. Доказано, что у женщин с антифосфолипидным синдромом исходы беременности улучшаются при приеме аспирина в малых дозах и гепарина [11–13].
Опубликованы данные сравнительного исследования с участием женщин, имеющих привычное невынашивание вследствие антифосфолипидного синдрома. Женщины получали терапию низкомолекулярным гепарином второго поколения бемипарином в дозе 2500 МЕ/сут или аспирином в дозе 100 мг/сут. Лечение проводилось с периода прегравидарной подготовки до 36-й недели беременности. Бемипарин обладает самой малой молекулярной массой среди всех используемых на сегодняшний день низкомолекулярных гепаринов. Благодаря этому бемипарин демонстрирует максимальное соотношение анти-Ха/анти-IIа-факторной активности – 8:1, что обеспечивает выраженный антитромботический эффект при минимальном риске развития кровотечения [14, 15]. В группе лечения бемипарином частота рождения живых детей составила 86,25% по сравнению с 72,13% в группе пациенток, принимавших аспирин. Масса тела новорожденных детей, чьи матери прошли курс лечения бемипарином, была выше, а осложнений со стороны матери и плода не наблюдалось [14, 15].
Аналогичное исследование по применению бемипарина для профилактики тромбоэмболических заболеваний провели испанские исследователи, доказавшие безопасность и эффективность применения бемипарина у беременных с тромбофилиями [17, 18].
Не столь однозначные данные были получены при исследовании антикоагулянтов как препаратов для профилактики неблагоприятного исхода беременности у женщин с отягощенным акушерским анамнезом, но без очевидных тромбофилий, хотя и в этом случае наблюдались положительные результаты. Например, при тяжелой преэклампсии в анамнезе прием гепарина в сочетании с аспирином в качестве профилактики преэклампсии, внутриутробной задержки роста плода и неблагоприятного исхода беременности более эффективен, чем применение с этой целью только аспирина [17–19].
В экспериментальных работах показана важная роль гепарина в процессе инвазии и дифференцировки трофобласта [20]. У женщин с привычным невынашиванием беременности неясной этиологии использование низкомолекулярного гепарина начиная с первого триместра и на протяжении всей беременности существенно снижало частоту ранних и поздних потерь плода [21]. Недавно проведенный метаанализ показал эффективность низкомолекулярного гепарина в профилактике повторных тяжелых связанных с патологией плаценты осложнений беременности – преэклампсии, рождения детей с низким весом (менее 10-го перцентиля), преждевременной отслойки нормально расположенной плаценты, поздних выкидышей [22]. В то же время систематический обзор, выполненный P.G. de Jong и соавт., не подтвердил снижение частоты акушерских осложнений у женщин с необъяснимым повторным невынашиванием беременности (имеющих или не имеющих врожденную тромбофилию) на фоне применения низкомолекулярных гепаринов и/или антиагрегантов. Однако авторы отмечают необходимость проведения в дальнейшем хорошо организованных рандомизированных контролируемых исследований [23].
Безусловно, важную роль в описанном выше профилактическом эффекте гепарина играет его антикоагулянтное действие. Беременность в норме является гиперкоагуляционным состоянием, но чрезмерная гиперкоагуляция способствует развитию осложнений, в том числе тяжелой преэклампсии [23]. По этой причине патогенетически оправданно применение гепарина, но его действие не ограничивается антикоагулянтным эффектом. Гепарин прямо и опосредованно участвует в адгезии бластоцисты к эндометрию и последующей инвазии [24], усиливает ангиогенез в кондиционированной клетками человеческой плаценты среде, что косвенно подтверждает роль дополнительных (неантикоагулянтных) эффектов гепарина в профилактике преэклампсии [25]. Имеются клинические данные о достоверном повышении уровня циркулирующего плацентарного фактора в третьем триместре беременности у женщин, получавших низкомолекулярный гепарин, при этом уровень sFlt1 был сравним с контрольной группой [26]. Эти находки могут объяснить эффективность низкомолекулярных гепаринов в профилактике осложнений беременности, связанных с патологией плаценты. Особенно важным условием профилактического действия антиагрегантов и гепарина, по нашему мнению, является их своевременное назначение на этапе планирования или в ранние сроки беременности (первый триместр), это позволяет добиться полноценной имплантации и плацентации и снизить риск развития преэклампсии [20].
Известно очень небольшое число работ, в которых изучалась эффективность использования гепарина и антиагрегантов с целью улучшения исходов беременности у пациенток с ХБП, что и послужило побудительным мотивом при проведении нашего исследования.
Цель
Оценить эффективность применения гепарина и антиагрегантов для профилактики осложнений и улучшения исходов беременности у женщин с ХБП первой – третьей стадии.
Материал и методы
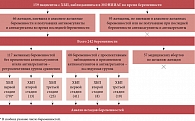
Из 159 пациенток с ХБП, наблюдавшихся во время беременности в Московском областном научно-исследовательском институте акушерства и гинекологии (МОНИИАГ) и у нефролога в Московском областном научно-исследовательском клиническом институте им. М.Ф. Владимирского, было отобрано 66 женщин, имевших в анамнезе желанные беременности. По этическим причинам невозможно провести рандомизированное сравнительное исследование эффективности влияния гепарина и антиагрегантов на исход беременности у женщин с хронической почечной недостаточностью. В этой связи выбранная для изучения группа женщин рассматривалась и как исследуемая проспективная группа, и как ретроспективная контрольная. Во время анамнестических беременностей женщины не получали лечение антикоагулянтами и антиагрегантами. Во время последней (последних) беременностей, протекавших под наблюдением специалистов МОНИИАГ, эти же пациентки принимали дипиридамол и гепарин (нефракционированный или низкомолекулярный). Сравнивались исходы желанных беременностей без использования антикоагулянтов и антиагрегантов (проанализированных ретроспективно) и результаты проспективного наблюдения за течением и исходом последующих беременностей у тех же пациенток на фоне применения гепарина и дипиридамола.
Всего оценивались исходы 242 беременностей, из них 185 желанных. 57 медицинских абортов, выполненных в прошлом по желанию женщин, не учитывались. На фоне использования гепарина и дипиридамола протекали 68 беременностей (две пациентки вынашивали две последние беременности на фоне приема гепарина и антиагрегантов) – исследуемая группа. Исходы 117 анамнестических беременностей без применения антикоагулянтов и антиагрегантов у тех же женщин оценивались ретроспективно – группа сравнения (контрольная) (рис. 1).
В исследуемой группе 41 беременность протекала при ХБП первой стадии, восемь – ХБП второй стадии, 19 – ХБП третьей стадии, а в группе сравнения – 79 беременностей – при ХБП первой стадии, 13 – ХБП второй стадии, 25 – ХБП третьей стадии. Стадия ХБП определялась в соответствии со значением скорости клубочковой фильтрации до беременности, поскольку из-за физиологических изменений почечного кровотока и плазмотока скорость клубочковой фильтрации возрастает уже в ранние сроки беременности [27, 28].
Беременности без профилактического применения антикоагулянтов и антиагрегантов протекали либо при той же стадии ХБП, либо ХБП была менее выраженной. Все пациентки в начале наблюдения в МОНИИАГ были проинформированы о высоком риске беременности для матери и для плода при ХБП, особенно при почечной недостаточности, однако женщины приняли решение о пролонгировании беременности.
Средний возраст на момент наступления последней беременности у пациенток с ХБП первой стадии составил 31,1 ± 4,5 года, с ХБП второй стадии – 30,2 ± 5,7 года, а с ХБП третьей стадии – 30,8 ± 4,3 года. Ни у кого из пациенток на момент зачатия (при последней беременности) не отмечалось обострения заболевания почек. В структуре причин ХБП всех стадий преобладали хронический гломерулонефрит и хронический пиелонефрит (табл. 1).
Благоприятным исходом беременности считалось рождение ребенка без аномалий развития и выживание его в постнатальном периоде при отсутствии значимого ухудшения почечной функции у матери после родов (отсутствие стойкого снижения скорости клубочковой фильтрации или снижение скорости клубочковой фильтрации менее чем на 25% от исходного уровня). Неблагоприятным исходом было решено считать антенатальную или интранатальную гибель плода, или смерть в младенческом возрасте (в течение первого года жизни), и/или стойкое снижение скорости клубочковой фильтрации у матери на 25% и более от уровня до беременности, или необходимость начала постоянной заместительной почечной терапии в течение года после родов.
С ранних сроков беременности (первый триместр) или уже на этапе прегравидарной подготовки пациентки начинали получать гепарин в той или иной форме. 41 беременной один из препаратов низкомолекулярного гепарина один-два раза в сутки вводился подкожно: эноксапарин 0,4 мл = 4000 анти-Ха МЕ (n = 2), надропарин 0,3 мл = 2850 МЕ (n = 18), бемипарин 0,2 мл = 3500 анти-Ха МЕ (n = 5). Остальные женщины исследуемой группы получали нефракционированный гепарин по 5000 МЕ два-три раза в сутки или в ингаляциях через небулайзер по 12,5–25 000 МЕ два раза в сутки с интервалом 12 часов. Все пациентки принимали дипиридамол внутрь в дозе 225 мг/сут (по 75 мг три раза в день). Антикоагулянты отменялись не позднее чем за 12 часов до родов, но в первые сутки послеродового периода (не ранее чем через шесть часов после родов) введение гепарина возобновлялось и продолжалось в течение пяти-шести недель.
С целью коррекции артериального давления в плановом порядке применялись дигидропиридиновые антагонисты кальция (нифедипин, амлодипин) иногда в сочетании с селективными бета-адреноблокаторами (бисопролол, небиволол) и метилдопой. Лечение преэклампсии включало магнезиальную терапию, при этом суточная доза сульфата магния уменьшалась в соответствии со снижением скорости клубочковой фильтрации, также контролировался уровень магния сыворотки.
Для лечения анемии во время беременности использовались препараты железа перорально или парентерально в сочетании с фолиевой кислотой. При развитии в послеродовом периоде тяжелой анемии прием препаратов железа продолжался, кроме того добавлялись стимулирующие эритропоэз препараты длительного действия (метоксиполиэтиленгликоль-эпоэтин бета одно-два введения по 75–100 мкг подкожно).
При развитии фетоплацентарной недостаточности беременным вводили Эссенциале Н, Актовегин, Ксантинола никотинат парентерально. В случае фетоплацентарной недостаточности с повышенной сократительной активностью матки назначали бета-адреномиметики – Гинипрал внутрь или в/в капельно. При высоком риске досрочного родоразрешения (угроза преждевременных родов, преэклампсия) всем пациенткам в течение двух суток проводилась профилактика респираторного дистресс-синдрома плода дексаметазоном (Дексазоном) в дозе 8 мг/сут в/м.
Статистическая обработка данных. Показатели, подчиняющиеся нормальному распределению, были представлены в виде M ± SD (среднее значение ± стандартное отклонение). Показатели с распределением, отличающимся от нормального, описывались при помощи медианы и диапазона колебаний, качественные показатели – в долях (процентах), либо в абсолютных значениях. Для оценки достоверности различия качественных признаков (долей в группах) использовался точный критерий Фишера. В качестве критического уровня достоверности различий был принят уровень 0,05.
Результаты
В группе проспективного наблюдения были проанализированы частота развития и тяжесть преэклампсии, а также сроки родоразрешения и масса тела детей при рождении (табл. 2). Частота преэклампсии на всех стадиях ХБП была выше, чем в общей популяции беременных, и возрастала по мере прогрессирования ХБП. При этом у беременных с ХБП третьей стадии преэклампсия развивалась достоверно чаще, чем у женщин с ХБП первой стадии (52,6 и 19,5% соответственно, p = 0,015). Тяжелая преэклампсия также наблюдалась чаще при ХБП третьей стадии по сравнению с ХБП первой стадии (21,0 против 2,4%, p = 0,017). Между беременностями на фоне ХБП второй и третьей стадии по этим показателям достоверных различий обнаружить не удалось. При сравнении беременностей, протекавших на фоне ХБП первой и второй стадии, отмечалась лишь тенденция к повышению частоты преэклампсии в целом (p = 0,088) и умеренной преэклампсии (p = 0,068) при ХБП второй стадии, хотя преэклампсия при ХБП второй стадии встречалась более чем в два раза чаще. По-видимому, отсутствие статистической достоверности объясняется небольшим числом пациенток с ХБП второй стадии.
Медиана срока родов при беременностях у женщин с ХБП третьей стадии, как и медиана массы тела детей при рождении, была достоверно ниже по сравнению с беременностями, протекавшими на фоне ХБП первой и второй стадии
Ни в одном случае у беременных и новорожденных не наблюдалось серьезных геморрагических осложнений. Никто из женщин не нуждался в заместительной почечной терапии в течение 12 месяцев после родов.
При сравнении исходов беременностей у пациенток с ХБП всех стадий оказалось, что в группе с профилактическим применением гепарина и дипиридамола по сравнению с группой без использования антикоагулянтов и антиагрегантов благоприятных исходов беременности было достоверно больше – 66 из 68 (97,1%) против 58 из 117 (49,6%), p < 0,001 (табл. 3). При этом беременности в исследуемой группе развивались в заведомо менее благоприятных условиях – при большем стаже ХБП, а у части женщин и при более выраженном снижении почечной функции.
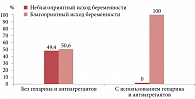
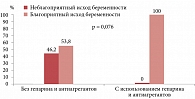
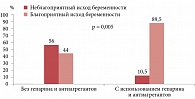
Мы также провели анализ исходов беременностей в зависимости от стадии ХБП у женщины. У пациенток с ХБП первой стадии при использовании гепарина и антиагрегантов беременности имели благоприятный исход в 100% случаев, в то же время анамнестические беременности у этих женщин в 49,4% случаев закончились неудачей, p < 0,001 (рис. 2). При ХБП второй стадии получены сходные результаты: на фоне применения антикоагулянтов и антиагрегантов все исходы были благоприятными, а в группе сравнения доля неблагоприятных исходов составила 46,2% (рис. 3). Статистические различия только стремились к достоверности (p = 0,076), вероятно, из-за небольшого числа пациенток в данной группе. У пациенток с ХБП третьей стадии при последней беременности использование гепарина и дипиридамола достоверно повышало долю благоприятных исходов беременности: их было 89,5% в исследуемой группе и только 44% в ретроспективной группе сравнения (p = 0,005), хотя эти женщины имели уже явную хроническую почечную недостаточность (рис. 4).
Обсуждение
В сравнительном ретроспективно-проспективном исследовании влияния гепарина и антиагрегантов на исход беременности при ХБП с участием 66 пациенток с ХБП (всего 185 желанных беременностей), было получено достоверное улучшение исходов для плода при проведении профилактики дипиридамолом и гепарином осложнений, связанных с патологией плаценты. Если в исследуемой группе было 97,1% (66 из 68) успешных беременностей, то в контрольной группе (без применения антиагрегантов и антикоагулянтов) только 49,6% (58 из 117). Это несмотря на то что, стаж ХБП у пациенток контрольной группы был меньше и у части женщин к моменту последней беременности (а именно последние беременности вошли в исследуемую группу) произошло снижение почечной функции. Статистически значимое улучшение исхода беременности наблюдалось у всех пациенток вне зависимости от стадии ХБП (в исследование включены беременные с ХБП первой – третьей стадии). Несмотря на более высокую по сравнению с общей популяцией частоту преэклампсии и более раннее родоразрешение (особенно при ХБП третьей стадии), у большинства пациенток, получавших во время беременности гепарин и дипиридамол, родились живые дети, которые выжили в постнатальном периоде. Беременность у этих женщин не привела к существенному снижению почечной функции по крайней мере в течение одного года наблюдения после родов.
Безусловно, данное исследование имеет существенные недостатки: оно относительно небольшое по числу включенных больных, не рандомизированное, не полностью проспективное (беременности контрольной группы анализировались ретроспективно). Кроме того, женщины принимали разные препараты гепарина, способы введения которого не были унифицированы: часть пациенток получала нефракционированный гепарин подкожно, другая часть – в виде ингаляций, а третья – один из препаратов низкомолекулярного гепарина подкожно.
Можно предположить, что на улучшение исходов беременностей на фоне профилактики осложнений гепарином и дипиридамолом оказал влияние «эффект центра»: более тщательное наблюдение и возможность более полного обследования пациенток в научно-исследовательском институте, лучшая техническая оснащенность параклинических подразделений, раннее распознавание осложнений и их лечение, своевременное принятие решений о необходимости досрочного родоразрешения, наличие современной неонатологической службы и т.д. Тем не менее наиболее существенным отличием протокола ведения беременных с ХБП, применявшегося в МОНИИАГ, стало использование гепарина и дипиридамола с ранних сроков беременности, что, как мы считаем, и позволило добиться высокой частоты благоприятных исходов беременности у женщин с неблагоприятным соматическим статусом и отягощенным акушерским анамнезом.
Выводы
У женщин с ХБП первой – третьей стадии применение гепарина и дипиридамола способствует повышению частоты благоприятного исхода беременности – рождению живых детей и их выживанию в постнатальном периоде без ускорения прогрессирования ХБП у матерей.
Препараты низкомолекулярных гепаринов наиболее удобны для длительного применения во время беременности и обладают оптимальным фармакокинетическим профилем, обеспечивающим пациенткам с ХБП стабильный клинический эффект.
Для уточнения механизмов благоприятного влияния антикоагулянтов и антиагрегантов на исход беременности при ХБП и разработки оптимальных режимов применения данных препаратов у беременных с заболеваниями почек требуются дальнейшие исследования.
Ye.I. Prokopenko, I.G. Nikolskaya
Moscow Regional Research and Clinical Institute
Moscow Regional Research Institute of Obstetrics and Gynecology
Contact person: Yelena Ivanovna Prokopenko, renalnephron@gmail.com
Objective: to assess the effectiveness of heparin and antiplatelet therapy for prevention of complications and improvement of pregnancy outcomes in women with CKD.
Subjects and methods. The study included 66 women with CKD (40 with CKD 1 stage, 8 with CKD 2 stage, 18 with CKD 3 stage) and a history of a wanted pregnancy, during which has not been treated with heparin and/or antiplatelet agents. At last pregnancy all were treated by heparin and dipyridamole for the prevention of preeclampsia and placental insufficiency. Two patients received heparin and dipyridamole during their two last pregnancies. Study group consisted of 68 pregnancies with heparin and antiplatelet agents, and the control group – 117 anamnestic pregnancies without receiving anticoagulants and antiplatelet agents in the same women.
Results. In the study group the frequency of favorable outcomes of pregnancies was significantly higher compared with the control group – 66 out of 68 (97.1%) versus 58 out of 117 (49.6%), p < 0,001. None of the patients did need to start a permanent renal replacement therapy during 12 months after delivery. Improving pregnancy outcomes observed in all stages of CKD.
Conclusion. In women with CKD 1–3 stages heparin and dipyridamole helped to improve pregnancy outcomes – live birth and survival in the postnatal period without significant deterioration in renal function in mothers during the year after delivery.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.