количество статей
7404
Загрузка...
Пожалуйста, авторизуйтесь:
Теория
Беременность у пациенток с терминальной почечной недостаточностью, получающих лечение программным гемодиализом
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Акушерство и гинекология" № 4 (45)
- Аннотация
- Статья
- Ссылки
- English
Представлен анализ публикаций последних лет, в которых раскрываются принципы ведения беременных с терминальной стадией хронической почечной недостаточности, находящихся на лечении гемодиализом. Благодаря усовершенствованию технологии заместительной почечной терапии в последние годы возросла фертильность у таких больных. Приведены аргументы, подтверждающие возможность вынашивания беременности у женщин с терминальной стадией хронической почечной недостаточности, находящихся на лечении гемодиализом. Пациентки нуждаются в индивидуальном подборе режима заместительной терапии, наиболее приемлемым является ежедневный гемодиализ. В этой группе пациентов необходимо постоянно контролировать уровни гемоглобина, гематокрита, проводить раннюю диагностику преэклампсии и фетоплацентарной недостаточности, тщательно следить за режимом питания, назначать внедиализную медикаментозную терапию. Авторами разработан общий алгоритм наблюдения и ведения беременных с терминальной стадией хронической почечной недостаточности, находящихся на лечении гемодиализом.
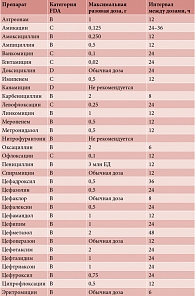
Таблица. Антимикробные препараты: рекомендуемые дозировки у больных с терминальной почечной недостаточностью
Введение
Любое прогрессирующее заболевание почек приводит к развитию хронической почечной недостаточности (ХПН). Терминальная стадия ХПН характеризуется значимым ухудшением всех почечных функций и резким снижением скорости клубочковой фильтрации менее 15 мл/мин. Терминальная ХПН соответствует пятой стадии хронической болезни почек по международной классификации, предложенной инициативной группой по улучшению глобальных исходов заболеваний почек (Kidney Disease: Improving Global Outcomes – KDIGO) [1–5]. На пятой стадии хронической болезни почек возможности консервативного лечения исчерпаны, поэтому возникает необходимость проведения заместительной почечной терапии: лечения диализом (перитонеальный диализ и гемодиализ) и трансплантации почки [5].
Определение хронической болезни почек как «наличие любых признаков повреждения почек, персистирующих в течение трех и более месяцев после их выявления» вне зависимости от нозологического диагноза, а также классификация стадий заболевания по показателям скорости клубочковой фильтрации впервые были предложены Национальным почечным фондом США в 2002 г. [1–5]. Необходимость введения данного наднозологического понятия была продиктована значимым увеличением частоты терминальной ХПН в мире и связанным с этим ростом экономических затрат по организации и деятельности новых диализных и трансплантационных центров.
Терминальная ХПН – это не только необходимость проведения дорогостоящей диализной терапии, но и значительное ухудшение качества жизни пациентов. Последнее обусловлено серьезными изменениями всех функциональных систем организма, что проявляется артериальной гипертензией, повышением жесткости сосудистой стенки, системным воспалением, окислительным стрессом, анемией, гипергомоцистеинемией, дислипидемией, костно-минеральными нарушениями, гиперпролактинемией, иммуносупрессией, нарушением коагуляции, дисменореей, бесплодием, депрессией, а также ощущением неполноценности и отстраненности от социума [5–10].
Беременность пациенток на диализе: история вопроса
У женщин, получающих лечение гемодиализом, фертильность снижена. Однако в последнее десятилетие в связи с усовершенствованием программ гемодиализа, аппаратов «искусственная почка», а также внедиализной терапии наблюдается рост частоты беременностей [11]. Так, этот показатель Европе в 1970-е гг. составлял менее 1%, в США – 1,4% в 1990–1992 гг. и 2,4% в 1992–1995 гг., в Японии – 3,4% в 1996 г., в Саудовской Аравии в начале 2000-х гг. – 5–7,9%. В настоящее время, по данным канадских врачей, доля беременных, находящихся на ночном гемодиализе, выросла до 15,9% [12, 13].
Первая публикация об успешном завершении беременности у пациентки, получавшей гемодиализ, появилась в 1971 г. [2, 3, 14]. С тех пор произошли значительные изменения в терапии гемодиализом: увеличилось число диализных центров и больных на гемодиализе, усовершенствовались диализные программы, мембраны диализаторов и составы диализирующих растворов. Кроме того, достигнут определенный прогресс в выхаживании глубоко недоношенных детей и детей с низкой массой тела, высокая частота рождения которых характерна для пациенток с терминальной стадией ХПН. Все это создает предпосылки для увеличения частоты благоприятных исходов беременностей у диализных пациенток в наши дни. Так, если доля живорожденных детей у диализных пациенток в 1980 г. составляла менее 23%, то в 2010 г. она возросла более чем в 3,5 раза, достигнув 81–87% [9, 10, 12, 13].
Между тем отношение к проблеме вынашивания беременности у таких пациенток неоднозначно. Особенности течения и исходы беременностей трудно систематизировать в связи с их крайней редкостью: врачи наблюдают максимум один-два подобных случая за всю свою практику. Режимы гемодиализа, как и сами диализные аппараты, в разных центрах существенно различаются между собой, еще более затрудняя обобщение подобных публикаций. Этим объясняется недостаточное внимание к данной проблеме, отсутствие мотивации изучения гинекологической заболеваемости и фертильности таких пациенток, нигилистическое отношение к самому факту их беременности, распространенные рекомендации «вначале провести трансплантацию, восстановить нормальную функцию почек, а далее – беременеть и рожать» [9]. В какой-то степени такие рекомендации оправданы тем, что хорошо функционирующий трансплантат создает более благоприятные условия для вынашивания беременности. Но что делать, если беременность у пациентки, получающей лечение диализом, уже наступила?
По мнению нефрологов и акушеров-гинекологов, занимающихся проблемой гемодиализа у беременных, настороженному отношению к проблеме беременности у диализных пациенток можно противопоставить несколько фактов.
Во-первых, трансплантация почки больным с терминальной стадией ХПН не всегда оправданна. Некоторые болезни обмена, генетические мальформации будут автоматически продолжать провоцировать сходные повреждения в трансплантированной почке, делая этот вид лечения малоперспективным.
Во-вторых, постоянная нехватка донорских органов, длительное нахождение пациенток в «листах ожидания» трансплантации, рекомендации планировать беременность лишь спустя полтора-два года после трансплантации могут отрицательно влиять на фертильность, особенно в группе пациенток позднего репродуктивного возраста. Кроме того, невозможно гарантировать 100%-ную вероятность повторного зачатия у пациентки после прерывания беременности на фоне лечения гемодиализом и выполненной впоследствии трансплантации почки.
В-третьих, гемодиализ становится все более распространенным видом лечения, особенно в мусульманских странах, где религиозные, культурные и исторические традиции поддерживают культ больших семей, запрещая прерывание беременности.
В-четвертых, диализная терапия не влияет на плод (частота врожденных аномалий развития у таких детей не превышает общепопуляционные значения). Кроме того, определенный оптимизм вызывает и значительное улучшение перинатальных исходов у данного контингента пациенток в новом тысячелетии (76% случаев рождения живых детей).
В отличие от западных стран, где выпущены многочисленные статьи по вопросам вынашивания беременности и родоразрешения пациенток с терминальной ХПН, получающих лечение гемодиализом, в отечественной медицинской литературе публикации по этой проблеме до сих пор остаются единичными и уникальными [5, 15].
Ведение беременности у диализных пациенток
Беременность предъявляет к организму будущей матери значительные требования, которые также должны быть учтены и у пациенток, находящихся на лечении гемодиализом. Первым из необходимых условий для нормального развития плода считается снижение вариабельности и скачкообразности показателей гомеостаза будущей матери с максимальным приближением их к нормальным значениям. Вторым – введение в рацион достаточного количества белка и кальция – нутриентов, столь необходимых плоду, с минимальным вредом для организма беременной с подобной патологией. Общим правилом является изменение режима гемодиализа в пользу его удлинения и увеличения кратности процедур в течение недели [9, 12, 16–18].
Увеличение диализного времени способствует более плавному уменьшению уровня уремических токсинов и метаболитов в крови будущей матери, а также снижению скорости перемещения электролитов, что позволяет избежать высокой вариабельности этих показателей [5, 19]. Ежедневный диализ во время беременности (в противоположность режиму «три раза в неделю» для небеременных) – самый распространенный режим гемодиализа, а его общая продолжительность составляет как минимум 20–24 часа в неделю [8, 9, 12, 20, 21]. Итальянские нефрологи J.B. Piccoli и соавт. [22] в 2012 г. проанализировали литературу по тактике ведения беременности и режимам гемодиализа у пациенток с терминальной ХПН. Всего в обзор была включена 241 медицинская статья, где сообщалось о 90 беременностях у 82 пациенток с этой патологией. Частота благополучного исхода беременности составила 76,25% и была тем выше, чем дольше была продолжительность гемодиализа за неделю. Исходы беременностей при режиме диализа «столько, сколько пациентка могла выдержать» были наиболее благоприятными. В анализируемых исследованиях минимальная длительность диализа составила 15 часов в неделю [17], а самая высокая – 40 часов в неделю [23]. Тип использованных мембран и скорость потока крови также были очень вариабельны. По данным M. Barua и соавт., ночной гемодиализ обладал большими преимуществами по длительности и удобству для пациенток с терминальной ХПН и оказал наилучшее влияние на исход беременностей, которые завершились рождением живых и впоследствии выживших детей в 92% случаев [24].
Особенностью подбора режима гемодиализа во время беременности является систематическая переоценка величины «сухого» (постдиализного) веса пациентки, а также обеспечение прироста ее веса за счет увеличивающейся массы плода. В первом триместре общая прибавка в массе тела должна составлять всего 1–1,5 кг, в то время как во втором и третьем триместрах допустима прибавка 300–500 г в неделю. Материнский «сухой» вес и прибавка массы тела за беременность должны постоянно сопоставляться с прибавкой веса плода, что контролируется в третьем триместре во время ультразвукового исследования (УЗИ) [7, 25]. Эффективность правильно подобранного режима гемодиализа определяется по показателям азотистого метаболизма в сыворотке крови в преддиализный период [13]. Целевое значение остаточного азота сыворотки крови перед сеансом гемодиализа не должно превышать 17,1 ммоль/л или быть как можно ближе к этому значению [12, 13, 26].
По мнению K.R. Furas Czerpak и соавт. [18], лучше всего зарекомендовали себя мембраны диализаторов с высокой биосовместимостью и сниженной функциональной площадью, которые в комбинации с увеличением диализного времени позволяют минимизировать излишнюю потерю жидкости, а также избегать осложнений гемодиализа: эпизодов гипотонии и внезапного изменения осмолярности крови [18]. Неправильно подобранный режим ультрафильтрации, вызывающий эти осложнения, может снизить плодово-плацентарный кровоток и вызвать острое внутриутробное страдание плода [18, 27, 28].
Немаловажную роль для правильного формирования режима гемодиализа играет и остаточная функция почек. По мнению С. Luders и соавт. [9], режим диализа должен формироваться в зависимости от клинико-лабораторных показателей, данных УЗИ плода и околоплодных вод и остаточной функции почек. Так, пациентки, имеющие остаточную функцию почек с диурезом более одного литра в сутки, находящиеся на гемодиализе менее года, массой тела менее 70 кг, имели режим диализа по полтора-два часа шесть раз в неделю. Те же пациентки, диурез которых был менее литра в сутки, находящиеся на лечении гемодиализом более года или имеющие массу тела более 70 кг, получали двух-трехчасовые сеансы гемодиализа также шесть раз в неделю. Такие осложнения, как тяжелая артериальная гипертензия, анорексия, частая тошнота или рвота, выраженные отеки, большая прибавка веса, нарастание многоводия, служат показанием к увеличению времени каждого сеанса гемодиализа на 30 минут [13]. Следовательно, режим гемодиализа во время беременности невозможно стандартизировать, он должен быть подобран индивидуально.
Изменение режима гемодиализа в пользу увеличения его длительности и кратности сеансов может иметь и отрицательные последствия в виде повышенной эвакуации некоторых витаминов, микроэлементов и электролитов из организма беременной. Коррекция этих потерь осуществляется за счет специфики диализной или внедиализной терапии.
При установлении факта беременности и изменении диализного режима содержание калия в диализирующем растворе должно быть повышено до 3–3,5 ммоль/л с целью предупреждения гипокалиемии [20]. Увеличение частоты гемодиализа также может привести к значительному алкалозу [7, 29, 30], развитию гипофосфатемии, которые могут быть скорректированы назначением содержащих фосфаты лекарственных средств или употреблением продуктов, богатых фосфатами (в обычных условиях запрещенных к употреблению у диализных пациентов) [19, 31].
Концентрация бикарбонатов в диализирующем растворе должна быть низкой и соответствовать 25 мг экв/л. Рекомендуемая концентрация кальция в диализате, предотвращающая гиперкальциемию, – 1,75 ммоль/л [10, 21, 31]. При гиперкальциемии, а также с целью ощелачивания плазмы применяется раствор глюкозы в количестве 300–500 мл. Коррекция нарушений метаболизма кальция в случае снижения его уровня в сыворотке крови осуществляется путем назначения карботана кальция перорально [11]. Нормализация уровня фосфора позволяет корригировать уровень паратгормона, который может значительно повышаться у таких пациенток, и снизить степень вторичного гиперпаратиреоза [32]. Большую роль в нормализации уровня фосфора играет диета, ограничивающая прием фосфора (в случае гиперфосфатемии) с пищей до 800 мг/сут. Для снижения гиперфосфатемии могут назначаться фосфатсвязывающие препараты, уменьшающие всасывание фосфатов в кишечнике (содержащие или не содержащие кальций) [5, 15].
Удлинение времени диализа способствует снижению уремической интоксикации плода и дает возможность будущей матери расширить пищевой рацион, увеличив потребление белка и калия, а также жидкости. Высокая частота сеансов диализа позволяет лучше контролировать артериальную гипертензию, снизить дозы гипотензивных средств, применяемых во внедиализный период.
В связи с вероятностью повышения или снижения содержания жизненно важных электролитов и микроэлементов, обусловленной удлинением диализного времени, с одной стороны, и возрастающей потребностью в них плода – с другой, особенно важно определять показатели электролитов крови до и после гемодиализа. Контроль уровня паратгормона также очень важен для назначения своевременного лечения.
Практически все больные с ХПН имеют анемию различной степени тяжести, которая усугубляется во время беременности. Это объясняется участием почек в эритропоэзе и существенным повышением потребности в железе во время гестации. В лечении анемии обязательно используются препараты железа, эритропоэтина, фолиевой кислоты, в некоторых случаях – витамина B12. Целевой уровень гемоглобина у беременных, получающих лечение гемодиализом, составляет 100–110 г/л, гематокрита – 30–35% [12, 33].
В связи с возрастающими потребностями организма беременной и плода в железе только перорального приема бывает недостаточно, что может компенсироваться назначением препаратов железа внутривенно [7]. Дозы эритропоэтина увеличиваются во время беременности в полтора-два раза. Подтверждена эффективность препаратов эритропоэтина во время беременности, их прием не сопровождается гипертензионными осложнениями и не оказывает тератогенного действия [7, 34].
Тем не менее даже назначение всего рекомендованного комплекса лечения анемии не всегда позволяет достичь целевых значений гемоглобина и гематокрита. В таком случае проводится гемотрансфузионная терапия [12, 13]. Частое мониторирование гемоглобина и гематокрита крови позволяет контролировать как объем антианемической терапии, так и ее эффективность, четко отражающиеся на перинатальных исходах.
Y. Asamiya и соавт. [9], проанализировав исход 24 беременностей у пациенток, находящихся на гемодиализе, сделали заключение о прямой зависимости благоприятного исхода беременности и рождения живого новорожденного от нормального уровня материнского гемоглобина. К такому же выводу пришли C. Luders и соавт. [9], а также S. Reddy и соавт. [28], указывающие на прямую корреляцию нормальных показателей гемоглобина в третьем триместре беременности с рождением живого и впоследствии выжившего новорожденного, а также на корреляцию нормальных значений гематокрита в тех же сроках гестации с большей массой тела этих новорожденных при рождении.
Введение антикоагулянтов, осуществляемое в любом режиме гемодиализа, продолжается и во время беременности. Для профилактики сосудистых тромбозов, микротромбозов, гиперкоагуляции назначаются нефракциониронный или низкомолекулярные гепарины. Дозы гепарина, применяемые во время сеанса гемодиализа, должны быть минимальными [7, 13, 35].
Назначение антикоагулянтов во время процедуры гемодиализа необходимо, так как происходящая активация высокомолекулярных белков плазмы – кининогена и прекалликреина – активирует каскад свертывающей системы плазмы крови и тромбоцитов. Центральное место в этом каскаде отводится усиленной активации Х-фактора свертывания. Авторы последних европейских рекомендаций по оптимальной практике гемодиализа отдают предпочтение низкомолекулярным гепаринам, которые имеют значительно большую активность по сравнению с нефракционным гепарином в отношении X-фактора свертывания, обладая при этом меньшей частотой геморрагических осложнений.
Помимо этого, применение именно низкомолекулярных гепаринов корригирует основные патогенетические осложнения, вызванные прогрессированием хронической болезни почек: улучшает липидный профиль (низкомолекулярные гепарины не активируют, в отличие от нефракционного гепарина, фермент липопротеинлипазу), а также снижает эффект потери костной массы. Считается, что к концу сеанса гемодиализа активность Xa-фактора не должна превышать 0,4 МЕ/мл, а медиана дозы низкомолекулярных гепаринов при длительности сеанса не менее четырех часов составлять 3870 МЕ. В настоящее время интерес представляет современный препарат II поколения низкомолекулярных гепаринов, который уже применяется с целью профилактики свертывания крови в системе экстракорпорального кровообращения при процедуре гемодиализа, – бемипарин натрия (торговое название Цибор®).
Отличительной особенностью бемипарина от других низкомолекулярных гепаринов является:
- самый низкий молекулярный вес;
- минимальное по сравнению с другими низкомолекулярными гепаринами ингибирование IIa-фактора;
- самая высокая среди низкомолекулярных гепаринов анти-Xa-активность;
- самое высокое соотношение анти-Xa/IIa-факторной активности, позволяющее минимизировать серьезные геморрагические осложнения.
Бемипарин в дозе 2500 МЕ или 3500 МЕ у пациентов с массой тела менее 60 кг или более 60 кг соответственно вводится в артериальную линию экстракорпорального контура однократно в начале сеанса гемодиализа, в отличие от дробного введения нефракционного гепарина, и позволяет достичь лучшего соотношения эффективности/безопасности по сравнению с другими низкомолекулярными гепаринами.
Питание беременной, находящейся на терапии гемодиализом, также претерпевает изменения. Для нормального роста и развития плода возникает необходимость увеличения потребности в белке до 1,5–1,8 г на кг массы тела беременной в сутки, а также увеличения калорийности пищи: общая ежедневная калорийность должна составлять 30–35 ккал/кг массы тела беременной плюс 300 ккал [12, 14].
Рекомендуется также внедиализная медикаментозная терапия, включающая:
- прием 1 мг/сут фолиевой кислоты начиная с первого триместра (профилактика врожденных аномалий развития плода и профилактика/лечение анемии) [7];
- прием 1500 мг/сут кальция, необходимого плоду [26];
- прием водорастворимых витаминов (витамина С, тиамина, рибофлавина), доза которых должна быть увеличена вдвое (усиленный режим диализа способствует их выведению) [26];
- прием низких доз аспирина 75–100 мг/сут начиная с первого триместра беременности (для профилактики преэклампсии) [36].
Возможные осложнения беременности у пациенток на диализе
Инфекционные осложнения
Сама по себе процедура гемодиализа увеличивает риск инфекционных осложнений и заболеваний, в том числе риск внутриутробного инфицирования плода, что служит основанием для проведения специфических исследований. При выявлении патогенной флоры назначается своевременная патогенетическая терапия с учетом установленных возбудителей. Пациентки, получающие лечение гемодиализом, нередко инфицированы вирусами гепатита С, В, вирусами простого и опоясывающего герпеса, цитомегаловирусом. У беременных с вирусными гепатитами уровень печеночных ферментов должен мониторироваться особенно тщательно в течение всего периода гестации. Новорожденным при наличии гепатитов у их матерей проводится специфическая иммунизация вакциной в раннем неонатальном периоде, в возрасте один, два, 12 месяцев или совместная активная и пассивная иммунизации вакциной и гиперактивным гамма-глобулином сразу после рождения, в трех- и шестимесячном возрасте.
Важно отметить малосимптомность клинических признаков многих инфекционных осложнений у таких пациенток. В случае необходимости назначения антибактериальных препаратов их дозы должны учитывать терминальную стадию ХПН у пациенток. Назначение препаратов беременным должно основываться на принципах учета тератогенного влияния на плод (разрешены препараты категории В по классификации FDA). Однако по жизненным показаниям возможно применение препаратов категории С, ожидаемая польза от применения которых превышает потенциальное отрицательное влияние на состояние плода (таблица [15]).
Многоводие
Одним из наиболее часто встречающихся осложнений беременности у пациенток, находящихся на заместительной терапии гемодиализом, является многоводие. Многоводие при гемодиализе объясняется резкими изменениями уровня азотистых соединений крови до и после процедуры гемодиализа. Высокий уровень мочевины перед сеансом гемодиализа может вызвать осмотический диурез у плода, что приводит к увеличению продукции амниотической жидкости. Лечение или предупреждение этого осложнения осуществляется коррекцией режима гемодиализа с увеличением диализного времени, также в некоторых случаях может быть применен амниоцентез [7, 9, 12, 13, 22].
Согласно данным ряда исследований, индометацин, с успехом применяющийся у женщин с многоводием, при терминальной стадии почечной недостаточности теряет свою эффективность. Его употребление более 72 часов коррелирует с ухудшением внутриутробного состояния плода, что делает невозможным его длительное использование [7]. Многоводие в свою очередь значительно увеличивает частоту преждевременных родов. В случае необходимости лечения угрозы прерывания беременности проводится токолитическая терапия. Это может быть введение сернокислой магнезии (с большой осторожностью и под контролем концентрации магния в крови), антагонистов кальция и бета-адреномиметика гексопреналина [7, 12]. Согласно сообщениям C. Pipili и cоавт. [10], с целью лечения угрозы прерывания беременности может быть использован прогестерон в дозе 300 мг/сут, а выявление истмико-цервикальной недостаточности при УЗИ служит показанием к наложению швов на шейку матки.
Артериальная гипертензия и преэклампсия
Артериальная гипертензия наблюдается у 80% беременных с терминальной ХПН, получающих лечение гемодиализом. Целевое артериальное давление составляет 140/80–90 мм рт. ст. [13]. Наряду с коррекцией режима диализа применяются стандартные гипотензивные препараты, разрешенные во время беременности. Следует знать, что изменение режима гемодиализа не корригирует артериальную гипертензию, обусловленную преэклампсией.
При лечении артериальной гипертензии у беременных запрещены к применению ингибиторы ангиотензинпревращающего фермента, блокаторы рецепторов ангиотензина II, а также диуретики. Между тем прием этих средств в первом триместре беременности до установки факта гестации (явление, часто встречающееся у подобного контингента больных) не относится к абсолютным показаниям для прерывания беременности, а требует консультации генетиков и тщательного УЗ-контроля с целью исключения пороков развития плода [5].
Лечение артериальной гипертензии у беременных должно соответствовать следующим принципам:
- максимальная эффективность для матери и безопасность для плода;
- максимально раннее начало и постоянный режим приема препаратов;
- необходимость в комбинации лекарственных средств при неэффективности монотерапии;
- индивидуальный подбор доз, поскольку интенсификация диализного режима может снизить потребность в гипотензивных средствах по сравнению с таковой до беременности.
С целью нормализации артериального давления применяются антагонисты кальция (нифедипин, верапамил), селективные бета-адреноблокаторы (атенолол, метопролол, небиволол), препараты центрального действия (метилдопа). В экстренных ситуациях для снижения артериального давления можно рекомендовать внутривенное введение гидралазина [7, 9, 12, 13].
При лечении преэклампсии гипотензивную терапию следует сочетать с сульфатом магния, однако данное лечение требует большой осторожности во избежание передозировки препарата и необходимости определения концентраций магния в крови. Дозы сульфата магния снижают в два-три раза, а концентрацию магния в крови контролируют до, во время введения и после него. Терапевтической концентрацией магния в сыворотке крови на фоне лечения считается 2,0–4,0 ммоль/л, а уровень 5,0 ммоль/ является пограничным в отношении развития осложнений (парезов, нарушения дыхания).
Классификация гипертензивных состояний у беременных, предложенная Всероссийским научным обществом кардиологов, включает [5]:
- хроническую артериальную гипертензию;
- гестационную артериальную гипертензию;
- преэклампсию (умеренную и тяжелую);
- преэклампсию на фоне хронической артериальной гипертензии.
Диагностика преэклампсии у беременных, получающих лечение гемодиализом, крайне сложна и требует от врача определенных навыков. Ситуация осложняется тем, что у пациенток с анурией определение протеинурии – одного из ведущих признаков преэклампсии – невозможно. Если же у пациентки остаточная функция почек сохранена и возможность определения протеинурии существует, то преэклампсия диагностируется (в гестационном сроке более 20 недель) в следующих ситуациях:
- у беременных без исходной артериальной гипертензии и протеинурии или с протеинурией менее 0,3 г/сут в случае появления артериальной гипертензии и протеинурии более 0,3 г/сут;
- у беременных, имеющих исходную артериальную гипертензию и протеинурию более 0,3 г/сут, в случае прогрессирования артериальной гипертензии, отсутствия эффекта от проводимой гипотензивной терапии, а также в случае двукратного повышения протеинурии;
- при наличии таких клинико-лабораторных признаков, как тромбоцитопения, гемолиз, повышение печеночных ферментов, признаки ДВС-синдрома, неврологические проявления (головная боль, боль в эпигастрии, нарушение зрения, тошнота, рвота, парестезии, повышенная возбудимость или сонливость, затруднение носового дыхания, покашливание, слюнотечение, ощущение удушья), повышение индекса резистентности в маточных артериях при УЗ-допплерометрии [37, 38].
Вышеуказанные клинико-лабораторные симптомы позволяют диагностировать преэклампсию у пациенток с отсутствием остаточной функции почек и анурией, а следовательно, невозможностью определения у них протеинурии [34].
Новые открытия в патофизиологии преэклампсии привели к появлению диагностических инструментов, которые могут иметь преимущество в ранней диагностике и лечении этого осложнения [14, 28]. Выявлено, что концентрация ангиогенного плацентарного фактора роста (placental growth factor – PLGF) и его антагониста растворимой fms-подобной тирозинкиназы 1 (soluble fms-like tyrozine kinase – sFlt-1), являющейся рецептором фактора роста эндотелия сосудов, а также их соотношение существенно меняются в крови беременных с преэклампсией, вызывая рост sFlt-1, снижение PLGF и увеличение соотношения sFlt-1/PIGF, называемого ангиогенным коэффициентом.
По мнению H.Y. Shan и соавт. [39], эти исследования в будущем могут значительно облегчить диагностику преэклампсии у беременных, получающих гемодиализ. C. Luders. и соавт. [9] называют преэклампсию грозным предиктором неудачных исходов беременности у данного контингента пациенток, обращая внимание, что частота ее выявления достигает 29–50%, а благоприятный исход беременности при этом осложнении наблюдается лишь в 60% случаев по сравнению с 92,9% без него. Это также касается гестационных сроков родоразрешения: при преэклампсии родоразрешение в 30 недель беременности происходит в 77,8% случаев, без преэклампсии – в 3,3% случаев.
Фетоплацентарная недостаточность
Профилактика, выявление и лечение фетоплацентарной недостаточности – это обязательное условие успешного завершения беременности у пациенток, находящихся на гемодиализе. Для профилактики/лечения фетоплацентарной недостаточности возможно применение метаболитов, витаминов, антигипоксантов, а также других активаторов клеточного метаболизма. Однако основным направлением профилактики фетоплацентарной недостаточности все же считается поддержание гомеостаза будущей матери в параметрах, максимально приближенных к нормальным, лечение анемии, гипертензии и коррекция фосфорно-кальциевого обмена.
Преждевременные роды
Частота преждевременных родов у пациенток, получающих лечение диализом, очень высока. Как правило, родоразрешение происходит в среднем на сроке 32 недели, что в большинстве случаев обусловлено двумя основными осложнениями: преэклампсией с прогрессирующей фетоплацентарной недостаточностью и спонтанным началом родов [23]. С целью улучшения созревания легких плода и профилактики респираторного дистресс-синдрома по стандартным схемам применяется дексаметазон.
Учитывая тяжесть заболевания пациенток и малые сроки беременности, врачи чаще всего прибегают к кесареву сечению. Однако проведение кесарева сечения при доношенном сроке гестации только из-за специфики экстрагенитальной патологии не оправдано. По мнению K.R. Furas Czerpak и соавт. [18], оперативное родоразрешение должно проводиться по показаниям, принятым для здоровых беременных.
Тактика родоразрешения
Родоразрешение беременных, получающих гемодиализ, требует пребывания пациенток в крупных перинатальных центрах и междисциплинарного подхода с участием квалифицированных бригад нефрологов, акушеров, неонатологов и реаниматологов. Новорожденные должны наблюдаться в отделении интенсивной терапии, так как наряду с недоношенностью и, как правило, низкой массой тела они обычно рождаются с повышенными (идентичными показателям их матерей) уровнями креатинина и мочевины и могут иметь в первые-вторые сутки жизни полиурию с соответствующими этому состоянию электролитными нарушениями [7, 20].
Основные рекомендации по ведению беременных на диализе
Анализируя рекомендации по тактике ведения и лечения беременных, находящихся на лечении гемодиализом, можно составить общий алгоритм их наблюдения [5, 7, 9, 13, 22, 40], который включает несколько важных пунктов.
- Необходимость пребывания пациенток в крупных многопрофильных медицинских центрах, имеющих в своей структуре отделения акушерства, реанимации, неонатологии, интенсивной терапии новорожденных, нефрологии, диализа, лабораторной диагностики.
- Междисциплинарный подход: совместное наблюдение и лечение пациенток акушерами-гинекологами, диетологом, нефрологом. При этом рекомендации нефролога (коррекция электролитного баланса, индивидуальный подбор режима диализной терапии) могут считаться координирующими и определяющими не только в тактике ведения процедуры гемодиализа, но и в выборе доз медикаментов для поддерживающей внедиализной терапии. Крайне необходимым является психоэмоциональный контакт с пациенткой, от которой само вынашивание беременности требует большого терпения и организованности.
- Информированность пациентки и ее родственников о большой частоте гестационных осложнений и высокой степени риска их развития, требующих длительной госпитализации и частых лабораторных обследований.
- Необходимость немедленной коррекции режимов гемодиализа при установлении факта беременности и принятии решения о ее пролонгировании, переход на ежедневный гемодиализ длительностью более 20 часов в неделю кратностью не менее шести раз в неделю, эффективность которого контролируется показателями азотистого метаболизма накануне диализа; коррекция пищевого рациона.
- Еженедельные скрининговые исследования показателей электролитов, паратгормона, азотистого метаболизма (креатинин, мочевина), белкового обмена (общий белок, альбумин, С-реактивный белок), состояния свертывающей системы крови, гемоглобина, гематокрита, тромбоцитов, печеночных ферментов, протеинурии (при имеющейся остаточной функции почек). В случае развития осложнений (гипертермия, усугубление артериальной гипертензии, присоединение преэклампсии, прогрессирование фетоплацентарной недостаточности, электролитные нарушения, отеки) кратность обследования учащается и осуществляется до и после процедуры гемодиализа.
- Определение риска хромосомной патологии плода и врожденных аномалий его развития путем УЗ-диагностики в 9–13 недель гестации и 20 недель гестации, а также исследований ассоциированного с беременностью протеина-А плазмы и бета-хорионического человеческого гонадотропина в 9–13 недель беременности. Необходимо отметить: указанные выше протеин и гонадотропин коррелируют со стадией ХПН, поэтому только их повышение является для таких пациенток нормой [24, 41].
- Поддержание целевых значений гомеостаза: целевое артериальное давление ≤ 140/85–90 мм рт. ст., целевой гемоглобин ≥ 100–110 г/л; целевой гематокрит – 30–35%; коэффициент насыщения трансферрина железом ≥ 30%, остаточный азот сыворотки крови накануне диализа < 17 ммоль/л или максимально приближен к этому показателю.
- Применение минимальных доз гепарина во время процедуры гемодиализа.
- Проведение цервикометрии в сроки 1–20 недель гестации для исключения истмико-цервикальной недостаточности.
- Обследование пациенток на наличие вирусных инфекций (гепатита В, С, хронической цитомегаловирусной инфекции).
- Адекватный плодовый мониторинг, включающий проведение УЗИ плода начиная с 26-й недели гестации каждые 10–14 дней (подтверждение соответствия размеров плода срокам гестации, оценка состояния плодовой гемодинамики, веса плода, зрелости и других особенностей плаценты, индекса амниотической жидкости); ежедневный мониторинг кардиотокографии плода и артериального давления пациентки до, во время и после каждой процедуры гемодиализа, выявление и лечение фетоплацентарной недостаточности.
- Проведение дифференциальной диагностики прибавки веса пациентки, обусловленной прогрессированием беременности, от прибавки веса вследствие гипергидратации при неадекватно подобранном диализном режиме.
- Применение поддерживающей внедиализной терапии (лечение анемии, гипертензии, инфекционных осложнений, угрозы прерывания беременности, фетоплацентарной недостаточности, нормализация фосфорно-кальциевого обмена).
- Своевременное родоразрешение пациенток в случаях присоединения преэклампсии, неуправляемой артериальной гипертензии, декомпенсации фетоплацентарной недостаточности. При отсутствии вышеуказанных осложнений возможно пролонгирование беременности до срока, максимально приближенного к доношенному.
- Возможность родоразрешения через естественные родовые пути при отсутствии показаний для оперативного родоразрешения, идентичных для здоровой беременной.
Заключение
Несмотря на востребованность вынашивания беременности среди пациенток, получающих лечение гемодиализом, риск акушерских осложнений и плохих перинатальных исходов у таких женщин по-прежнему достаточно высок. Так, для этой группы пациенток характерны высокая частота преждевременных родов (70–100%) [6, 22], синдрома задержки роста плода или рождения детей с низкой массой тела (100%) [22], преэклампсии (19–50%), артериальной гипертензии (67–80%) [42], многоводия (40–71%) [7, 9, 12], респираторного дистресс-синдрома (14–80%) [12], родоразрешения путем кесарева сечения (37–65%) [9, 12].
Благоприятного акушерского исхода можно ожидать при междисциплинарном наблюдении, увеличении времени диализной терапии, достижении низкого преддиализного уровня азотистых оснований, профилактике преждевременных родов, строгом контроле артериального давления и показателей электролитов, профилактике/лечении инфекционных осложнений, адекватном фетальном мониторинге, лечении анемии.
Из-за отсутствия достаточного количества наблюдений, разнородности режимов гемодиализа тактика ведения беременности у пациенток, находящихся на гемодиализе, до сих пор основывается на эмпирическом опыте врача [22]. В России к этой проблеме присоединяется еще одна: как правило, крупный перинатальный центр и отделение гемодиализа не находятся на одной территории. Это создает множество организационных проблем, велика вероятность запоздалого оперативного родоразрешения в случае экстренных показаний, диагностированных при фетальном мониторинге, во время или сразу после процедуры гемодиализа.
По-видимому, международная регистрация беременностей пациенток, получающих лечение гемодиализом, – необходимость, которая становится очевидным фактом. Это поможет ответить на многие вопросы, касающиеся режимов диализного лечения, поддерживающей внедиализной терапии, прогнозирования осложнений беременности и потенциальных заболеваний новорожденных, и в перспективе позволит улучшить исходы беременностей у женщин, получающих лечение диализом.
1. Никольская И.Г., Новикова С.В., Будыкина Т.С. и др. Беременность у пациенток с хронической почечной недостаточностью: тактика ведения родоразрешения при консервативно-курабельной стадии // Российский вестник акушера-гинеколога. 2012. Т. 12. № 6. С. 21–28.
2. Прокопенко Е., Никольская И. Беременность у женщин с хронической почечной недостаточностью (ч. 1) // Врач. 2013. № 8. С. 9–12.
3. Прокопенко Е., Никольская И. Беременность у женщин с хронической почечной недостаточностью (ч. 2) // Врач. 2013. № 8. С. 13–18.
4. Прокопенко Е.И., Никольская И.Г., Ватазин А.В. и др. Беременность у женщин с хронической почечной недостаточностью // Нефрология и диализ. 2013. Т. 15. № 2. С. 124–134.
5. Экстрагенитальная патология и беременность. Руководство / под ред. Л.С. Логутовой. М.: Литтерра, 2012.
6. Bahadi A., El Kabbaj D., Guelzim K. et al. Pregnancy during hemodialysis: a single center experience // Saudi J. Kidney Dis. Transpl. 2010. Vol. 21. № 4. P. 646–651.
7. Espinoza J., Romero R., Nien J.K. et al. Identification of patients at risk for early onset and/or severe preeclampsia with the use of uterine artery Doppler velocimetry and placental growth factor // Am. J. Obstet. Gynecol. 2007. Vol. 196. № 4. P. 326.e1–326.e13.
8. Levy A., Fraser D., Katz M. et al. Maternal anemia during pregnancy is an independent risk factor for low birthweight and preterm delivery // Eur. J. Obstet. Gynecol. Reprod. Biol. 2005. Vol. 122. № 2. P. 182–186.
9. Luders C., Castro M.C., Titan S.M. et al. Obstetric outcome in pregnant women on long-term dialysis: a case series // Am. J. Kidney Dis. 2010. Vol. 56. № 1. P. 77–85.
10. Pipili C., Grapsa E., Koutsobaili A. et al. Pregnancy in dialysis-dependent women – the importance of frequent dialysis and collaborative care: a case report // Hemodial. Int. 2011. Vol. 15. № 3. P. 306–311.
11. Hladunewich M., Hercz A.E., Keunen J. et al. Pregnancy in end stage renal disease // Semin. Dial. 2011. Vol. 24. № 6. P. 634–639.
12. Asamiya Y., Otsubo S., Matsuba Y. et al. The importance of low blood urea nitrogen levels in pregnant patients undergoing hemodialysis to optimize birth weight and gestational age // Kidney Int. 2009. Vol. 75. № 11. P. 1217–1222.
13. Harrington K., Fayyad A., Thakur V. et al. The value of uterine artery Doppler in the prediction of uteroplacental complications in multiparous women // Ultrasound Obstet. Gynecol. 2004. Vol. 23. № 1. P. 50–55.
14. Руководство по диализу / под ред. Дж.Т. Даугирдас, П.Дж. Блейк, Т.С. Инг / пер. с англ. под ред. А.Ю. Денисова, В.Ю. Шило. 3-е изд. Тверь: Триада, 2003.
15. Хатшуков А.Х., Османов А.Х., Мамхегова Т.Р. Ведение беременности у пациенток на диализе // Нефрология и диализ. 2005. Т. 7. № 2. С. 177–180.
16. Bailie G.R., Elder S.J., Mason N.A. et al. Sexual dysfunction in dialysis patients treated with antihypertensive or antidepressive medications: results from the DOPPS // Nephrol. Dial. Transplant. 2007. Vol. 22. № 4. P. 1163–1170.
17. Chan C.T. Nocturnal hemodialysis: an attempt to correct the ‘unphysiology’ of conventional intermittent renal replacement therapy // Clin. Invest. Med. 2002. Vol. 25. № 6. P. 233–235.
18. Furaz-Czerpak K.R., Fernandez-Juarez G., Moreno-de la Higuera M.A. et al. Pregnancy in women on chronic dialysis: a review // Nefrologia. 2012. Vol. 32. № 3. P. 287–294.
19. Hou S. Pregnancy in women treated with dialysis: lessons from a large series over 20 years // Am. J. Kidney Dis. 2010. Vol. 56. № 1. P. 5–6.
20. Furaz Czerpak K.R., Puente Garcia A., Corchete Prats E. et al. Successful pregnancy in a patient with chronic renal failure undergoing haemodialysis // Nefrologia. 2011. Vol. 31. № 2. P. 219–221.
21. Hou S. Pregnancy in women on dialysis: is success a matter of time? // Clin. J. Am. Soc. Nephrol. 2008. Vol. 3. № 2. P. 312–313.
22. Piccoli G.B., Conijn A., Consiglio V. et al. Pregnancy in dialysis patients: is the evidence strong enough to lead us to change our counseling policy? // Clin. J. Am. Soc. Nephrol. 2010. Vol. 5. № 1. P. 62–71.
23. Вишневский К.А., Земченков А.Ю., Герасимчук Р.П. Антикоагуляция на гемодиализе: перспективы применения низкомолекулярных гепаринов в оптимизации диализа // Клиническая нефрология. 2013. № 3. С. 38–41.
24. Barua M., Hladunewich M., Keunen J. et al. Successful pregnancies on nocturnal home hemodialysis // Clin. J. Am. Soc. Nephrol. 2008. Vol. 3. № 2. P. 392–396.
25. Barua M., Hladunewich M., Keunen J. et al. Successful pregnancies on nocturnal home hemodialysis // Clin. J. Am. Soc. Nephrol. 2008. Vol. 3. № 2. P. 392–396.
26. Hou S. Pregnancy in dialysis patients: where do we go from here? // Semin. Dial. 2003. Vol. 16. № 5. P. 376–378.
27. Reddy S.S., Holley J.L. The importance of increased dialysis and anemia management for infant survival in pregnant women on hemodialysis // Kidney Int. 2009. Vol. 75. № 11. P. 1133–1134.
28. Buckner C.L., Wilson L., Papadea C.N. An unusual cause of elevated serum total beta hCG // Ann. Clin. Lab. Sci. 2007. Vol. 37. № 2. P. 186–191.
29. Hofmeyr G.J., Atallah A.N., Duley L. Calcium supplementation during pregnancy for preventing hypertensive disorders and related problems // Cochrane Database Syst. Rev. 2006. Vol. 19. № 3. CD001059.
30. Hou S. Modification of dialysis regimens for pregnancy // Int. J. Artif. Organs. 2002. Vol. 25. № 9. P. 823–826.
31. Holley J.L., Reddy S.S. Pregnancy in dialysis patients: a review of outcomes, complications, and management // Semin. Dial. 2003. Vol. 16. № 5. P. 384–388.
32. Hussain S., Savin V., Piering W. et al. Phosphorus-enriched hemodialysis during pregnancy: Two case reports // Hemodial. Int. 2005. Vol. 9. № 2. P. 147–152.
33. Shemin D. Dialysis in pregnant women with chronic kidney disease // Semin. Dial. 2003. Vol. 16. № 5. P. 379–383.
34. Vazquez-Rodriguez J.G. Hemodialysis and pregnancy: technical aspects // Cir. Cir. 2010. Vol. 78. № 1. P. 99–102.
35. Chou C.Y., Ting I.W., Lin T.H., Lee C.N. Pregnancy in patients on chronic dialysis: a single center experience and combined analysis of reported results // Eur. J. Obstet. Gynecol. Reprod. Biol. 2008. Vol. 136. № 2. P. 165–170.
36. Dixon J.C., Kinney G.A., Block C., Daley V. Chronic kidney disease and dialysis management in a pregnant woman // Dial. Transplant. 2006. Vol. 35. № 6. P. 372–374.
37. Haase M., Morgera S., Bamberg C. et al. A systematic approach to managing pregnant dialysis patients – the importance of an intensified haemodiafiltration protocol // Nephrol. Dial. Transplant. 2005. Vol. 20. № 11. P. 2537–2542.
38. Shan H.Y., Rana S., Epstein F.H. et al. Use of circulating antiangiogenic factors to differentiate other hypertensive disorders from preeclampsia in a pregnant woman on dialysis // Am. J. Kidney Dis. 2008. Vol. 51. № 6. P. 1029–1032.
39. Malik G.H., Al-Harbi A., Al-Mohaya S. et al. Pregnancy in patients on dialysis – experience at a referral center // J. Assoc. Physicians India. 2005. Vol. 53. P. 937–941.
40. Coomarasamy A., Honest H., Papaioannou S. et al. Aspirin for prevention of preeclampsia in women with historical risk factors: a systematic review // Obstet. Gynecol. 2003. Vol. 101. № 6. P. 1319–1332.
41. Leypoldt J.K., Jaber B.L., Zimmerman D.L. Predicting treatment dose for novel therapies using urea standard Kt/V // Semin. Dial. 2004. Vol. 17. № 2. P. 142–145.
Pregnancy in Patients with End-Stage Kidney Failure Receiving Program Hemodialysis
I.G. Nikolskaya, Ye.I. Prokopenko
Moscow Regional Research Institute of Obstetrics and Gynecology
Moscow Regional Research Clinical Institute named after M.F. Vladimirskiy
Contact person: Irina Georgiyevna Nikolskaya, guzmoniiag@gmail.com
There have been analyzed publications of the recent years presenting principles for maintenance of pregnant women with end-stage kidney failure receiving hemodialysis. Owing to advances in technology of renal replacement therapy it allowed to increase fertility in women receiving hemodialysis. Arguments proving a possibility for carrying a pregnancy in patients with end-stage kidney failure receiving hemodialysis are provided. Such patients are needed in performing an individually selected replacement therapy, and daily hemodialysis is the most appropriate mode. Level of hemoglobin, hematocrit must be checked at regular basis in such patients, with early detection of pre-eclampsia and feto-placental insufficiency, carefully monitoring dietary regimen, and providing non-dialysis therapy. Here, we propose a general algorithm for observation and maintenance of pregnant women with end-stage kidney failure receiving hemodialysis.
Новости на тему
19.08.2022 01:00:00
15.08.2022 01:00:00
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.