Неоадъювантная эндокринотерапия рака молочной железы
- Аннотация
- Статья
- Ссылки



Неоадъювантная эндокринотерапия представляется эффективной и хорошо переносимой. Новое поколение ингибиторов ароматазы (летрозол, анастразол, эксеместан) чаще, чем тамоксифен вызывает объективный регресс опухоли, что в свою очередь позволяет нередко выполнить органосохраняющие операции. Больные с высоким уровнем экспрессии рецепторов стероидных гормонов (Allred scores ≥ 6) получают наибольший выигрыш от неоадъювантной эндокринотерапии из-за более частой регрессии опухоли. Оптимальная продолжительность неоадъювантной терапии детально не исследована.
Еще совсем недавно неоадъювантная терапия РМЖ заключалась преимущественно в проведении цитотоксической химиотерапии. Неоадъювантная терапия позволяет уменьшить размер опухоли для выполнения органосохраняющих операций вместо мастэктомии. Эндокринное лечение сейчас рассматривается как привлекательная альтернатива химиотерапии при положительных гормональных рецепторах в опухолях пожилых пациентов, многие из которых не в состоянии перенести токсическую химиотерапию (1).
Наиболее крупным исследованием неоадъювантной эндокринотерапии оказалось испытание Р024 с участием НИИ онкологии им. Н.Н. Петрова. Рандомизированное, двойное слепое, многоцентровое испытание Р024 было проведено для того чтобы сравнить противоопухолевую активность летрозола с активностью тамоксифена у 337 постменопаузальных женщин с ЭР+ и/или ПР+ первичным РМЖ. В соответствии с рандомизацией пациенты получали ежедневное лечение или летрозолом (2,5 мг) или тамоксифеном (20 мг) в течение 4 месяцев. До начала лечения ни одна из больных не считалась кандидатом для выполнения органосохраняющей операции, а 14% больных имели неоперабельные опухоли. Главной целью исследования было сравнить клинический общий ответ (CR+ PR) на лечение. Следующей целью была оценка объективного ответа, определяемого ультразвуковым исследованием и маммографией, а также определением числа больных, которым стало возможным выполнение органосохраняющих операций в результате неоадъювантного лечения (5). В этом исследовании ответ опухоли на лечение был связан со статусом гормональных рецепторов. Более частый объективный ответ наблюдался у пациентов, опухоли которых впоследствии (после исследования операционного препарата) подтверждались как ЭР-положительные в сравнении с больными, чьи опухоли при последующем послеоперационном тесте оказались ЭР-негативными. При любом уровне экспрессии эстрогенов частота ответов опухоли на летрозол была выше, чем на тамоксифен. Кроме того, было изучено значение экспрессии опухолью erb-В1 и erb-В2. Выявилось высокое отличие в частоте ответов ЭР+ опухолей с повышенной экспрессией erb-В1 и/или erb-В2: 88% объективных ответов в группе, получавших летрозол и лишь 21% ответов в группе, получавших тамоксифен (р=0,0004). С другой стороны при ЭР+ опухолях не экспрессирующих erb-В1 и/или erb-В2 частота клинических ответов на лечение оказалась схожей: 52% для летрозола и 42% для тамоксифена (p=0,078) (6). Частота клинических объективных ответов на летрозол равнялась 55% против 36% при лечении тамоксифеном (р=0,001). В отличие от анастразола в испытании IMPACT вероятность достижения общего объективного ответа (CR+PR) оказалась в два раза выше в группе, получавших летрозол, в сравнении с получавшими тамоксифен (р=0,0005). Учитывая, что объективный ответ оказался высоким при 4-месячном лечении летрозолом, ряд авторов начали проверку гипотезы – увеличивается ли частота объективных ответов опухоли при более продолжительном неоадъювантном лечении. В открытом клиническом испытании Paepke (2003) включено 33 больных РМЖ, получавших летрозол (2,5 мг ежедневно) от 4 до 8 месяцев. Автор сообщил, что более длительная терапия привела к достоверному уменьшению размера опухоли (р=0,0393).
Более того, у 60% больных, получавших предоперационное лечение летрозолом свыше 4 месяцев, наблюдался объективный ответ против 57% полных ответов (CR+PR) среди получавших лечение в более короткие сроки.
Аналогичное исследование выполнил Renshaw (2004), в которое были включены 142 постменопаузальные женщины с ЭР+ опухолями. Первоначальный клинический ответ оценивался после З месяцев лечения летрозолом (2,5 мг ежедневно). Не отвечающие на лечение больные и те, чьи опухоли стали подходящими для выполнения органосохраняющей хирургии, подверглись операциям. Остальные больные продолжали получать летрозол на протяжении 6-12 месяцев. В первые 3 месяца лечения наблюдалось 9,5% полных ответов, через 6 месяцев – 29% полных ответов, а к 12-му месяцу лечения – 36% полных ответов. Таким образом, у пациентов, чьи опухоли отвечают на летрозол после 3 месяцев лечения, можно ожидать дальнейшее уменьшение объема опухоли при продолжении лечения. Другими словами, пролонгация неоадъювантной эндокринотерапии увеличивает непосредственные результаты лечения у больных изначально чувствительных к гормонотерапии.
Smith и Dowsett (2003) недавно опубликовали результаты многоцентрового, двойного слепого клинического испытания IMPACT (Один аримидекс против тамоксифена против комбинации AT). Сравнивалась непосредственная эффективность неоадъювантного лечения анастразолом (1 мг ежедневно) против тамоксифена (20 мг ежедневно) против их комбинации (AT), в исследование вошли 330 постменопаузальных больных с ЭР+ и/или ПР+ РМЖ, с крупными, но операбельными опухолями или местнораспространенными опухолями. Лечение продолжалось 3 месяца, и в случаях, когда отмечался объективный ответ на неоадъювантное лечение, такое лечение рекомендовалось и в адъювантном режиме до 5 лет.
Основной целью исследования была оценка объективного ответа на лечение, дополнительная цель состояла в определении частоты выполнения органосохраняющих операций и оценка ключевых биологических маркеров, включая пролиферацию, апоптоз и изменение гормональных рецепторов.
При первичном анализе клинического материала оказалась схожая частота ответов на применения анастрозола, тамоксифена и их комбинацию (37%, 36%, 39% соответственно). Но достоверно большее число больных, получавших анастразол, подверглись органосохраняющим операциям (46% против 22%, р=0,0З). При erb-B2-положительных опухолях частота клинических ответов на анастразол была выше, чем на тамоксифен (58% против 22%, р=0,09). Эти результаты свидетельствуют о том, что лечение анастразолом как и летрозолом предпочтительнее тамоксифена при erb-B2-положительных опухолях молочной железы.
Эксеместан (Аромазин®) в неоадъювантном лечении
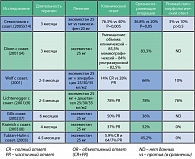
Результаты изучения эксеместана в неоадъювантном лечении кратко представлены в таблице 1. Нами проведено сравнительное и наиболее крупное исследование III фазы эффективности эксеместана и тамоксифена (14).
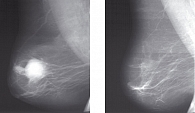
В него вошли более 150 постменопаузальных женщин с ЭР+ и/или ПР+ РМЖ (T2N1-2; ТЗN0-1; T4N0M0) рандомизированных на получение эксеместана (25 мг ежедневно) или тамоксифена (20 мг ежедневно) в течение 3 месяцев. Неоадъювантное лечение эксеместаном достоверно улучшило клинический объективный ответ (76,3% против 40%, р=0,05) (рисунок 1) и частоту выполнения органосохраняющих операций (36,5% против 20%, р=0,05), но не отмечалось достоверных отличий маммографического и ультразвукового «ответов». Частота полного патоморфологического регресса опухоли оказалась незначительной в обеих группах (3% против 1%, р=0,5). Сделан вывод, что эксеместан эффективнее тамоксифена в неоадъювантном лечении постменопаузальных женщин с ЭР+ РМЖ.
Кроме того, имеется еще ряд мелких испытаний I-II фазы (от 11 до 38 больных) неоадъювантного применения эксеместана, дизайн которых в отличие от нашего проекта не предполагал сравнение с тамоксифеном. Так, Dixon с соавт. (2001) оценили во II фазе эффект неоадъювантного эксеместана у 13 постменопаузальных женщин с ЭР+ операбельным (Т2) или местнораспространенным РМЖ. Эксеместан назначался по 25 мг (ежедневно) в течение 3 месяцев. Среднее сокращение объема опухоли клиническое, маммографическое и ультразвуковое достигло 85,5%, 84% и 82,5% соответственно. После лечения эксеместаном у 83,3% больных оказалось возможным выполнение органосохраняющих операций. Наиболее частыми побочными эффектами были утомляемость, бессонница и парестезия (у 25% больных). Из испытаний неоадъювантной химиотерапии известно, что достижение полного патоморфологического регресса (pCR) является ключевым моментом, определяющим благоприятные отдаленные результаты. Эта же идея использована в ряде испытаний неоадъювантной эндокринотерапии. Для того, чтобы увеличить частоту полных патоморфологических регрессов опухоли проведено два испытания I фазы сочетанной эндокринно-химиотерапии. Они основывались на результатах предклинических исследований, показавших, что эксеместан добавляет высокий цитотоксический потенциал к субтоксическим дозам эпирубицина и доцетаксела. Так, Wolf с соавт. (2001) лечили 14 больных местнораспространенным РМЖ с помощью эксеместана (25 мг ежедневно) в сочетании с эпирубицином в увеличивающихся дозах (25, 30, 35 мг/м2 еженедельно) на протяжении 8-12 недель. Оценены результаты у 10 из 14 больных. Полный объективный ответ наблюдался у 14% больных, частичный ответ – у 28% больных, у 30% больных – стабилизация заболевания, у 10% – прогрессирование. Органосохраняющие операции выполнены у 66% пациентов. Полный патоморфологический регресс получен у 10% больных, у остальных – частичный регресс.
Применяя тот же подход, Lichtenegger с соавт. (2001) провели исследование I фазы, включив 11 больных местнораспространенным РМЖ, получавших эксеместан (25 мг ежедневно) в сочетании с доцетакселом в увеличивающихся дозах (20, 25, 30 мг/м2 еженедельно) на протяжении 8-12 недель. Оценены результаты у 9 из 11 больных. Сообщается о 78% частичных ответов и 22% – о стабилизации заболевания. Патоморфологический ответ был высоким у 78% больных с опухолями I степени злокачественности и у 22% больных – II степени злокачественности (морфологический регресс по классификации Chevallier с соавт., 1993). Учитывая, что комбинация ингибиторы ароматазы + субтоксические дозы эпирубицина и таксотера представляется эффективной, планируется проведение исследования II фазы.
Gill с соавт. (2002) выполнил исследование II фазы, включив в него 33 постменопаузальных больных РМЖ. Основной целью исследования было оценить непосредственную эффективность неоадъювантного применения эксеместана. До лечения крупные размеры опухоли не позволяли выполнить органосохраняющие операции ни у одной больной. Они получали эксеместан (25 мг ежедневно) в течение 6 месяцев. Среди 28 оцененных больных у 50% наблюдался частичный ответ на лечение эксеместаном, у 45% – стабилизация и у 5% – прогрессирование заболевания. Половина больных после успешного лечения эксеместаном были прооперированы, из них 64% больных подверглись мастэктомии, а 36% – органосохраняющим операциям.
Krainick с соавт. (2003) сообщают об исследовании II фазы, где 29 больных получали лечение эксеместаном (25 мг ежедневно) на протяжении 16 недель. Данные о 27 больных были оценены. Частичный ответ на лечение отмечался у 37% больных, а у 63% пациентов – стабилизация заболевания. Не было ни одного случая полного патоморфологического регресса опухоли (таблица1).
В исследовании Tubiana-Hulin с соавт. (2003) 38 постменопаузальных больных с ЭР+ РМЖ получали эксеместан (25 мг ежедневно) в течение 4-5 месяцев. Ответ опухоли оценивался по критерию RECIST у 31 больной. У 5,9% больных отмечен полный регресс, у 64,7% – частичный ответ опухоли, у 23,5% – стабилизация. Органосохраняющие операции выполнены у 45,2% больных.
Если судить по данным литературы и по результатам собственных исследований, неоадъювантная эндокринотерапия представляется высокоэффективным и перспективным методом лечения РМЖ. Использование ингибиторов ароматазы нового поколения (летрозол, анастразол, эксеместан) предпочтительнее тамоксифена для достижения объективного ответа опухоли на лечение и выполнения органосохраняющего лечения.
Отбор больных для неоадъювантной системной терапии должен основываться, прежде всего, на данных о гормоночувствительности опухоли. При этом наибольший эффект от проводимой неоадъювантной эндокринотерапии наблюдается у больных с высоким уровнем экспрессии гормональных рецепторов (Allred score ≥ 6). Ингибиторы ароматазы способны вызывать ответ опухоли и при относительно низком уровне экспрессии ЭР и ПР, в то время как тамоксифен на обладает такими свойствами. Поэтому было бы важным оценить предсказывающее значение степени экспрессии рецепторов стероидных (шкала Allred в баллах от 0 до 8 или количественное определение биохимическим методом от 10 фмоль/мг белка до 300 и выше фмоль/мг белка), для определения порогового значения для тамоксифена и для ингибиторов ароматазы. Такой анализ может быть осуществлен только в условиях клинических испытаний, но не в обычной практике.
У больных с гормононезависимыми опухолями (ЭР-/ПР-) не выявлено объективного ответа на терапию как ингибиторами ароматазы, так и тамоксифеном (Eirmann ,2001). Наоборот, по данным Buzdar (2003) и Gianni (2006) у больных с отрицательными рецепторами эстрогенов (ЭР-) патоморфологический полный регресс на неоадъювантную химиотерапию, включающую таксаны, наблюдался в четыре раза чаще чем у больных с ЭР-положительными (гормоночувствительными) опухолями.
С помощью иммуногистохимического определения маркера пролиферации Ki67 и рецепторов прогестерона (ПР) возможно объективное измерение биологических эффектов эндокринотерапии и отличий ингибиторов ароматазы от тамоксифена. В противоположность тамоксифену лечение летрозолом и анастразолом сопровождается сокращением частоты определения Ki67 и снижением числа ПР+ опухолей. Уже упоминалось, что ингибиторы ароматазы эффективны безотносительно уровня экспрессии erb-B2, тогда как тамоксифен мало эффективен при erb-B2 (+) опухолях (6, 16).
Что касается продолжительности неоадъювантной системной терапии, то практическим стандартом для неоадъювантной химиотерапии является проведение 4-6 циклов до операции, период достаточный для определения чувствительных и не чувствительных к лечению опухолей. Оптимальная продолжительность неоадъювантной эндокринотерапии детально не исследована. По упоминавшимся данным Paepke (2003) у больных, получавших неоадъювантный летрозол в течение 8 месяцев, отмечался более частый регресс опухоли в сравнении с 4-х месячным лечением. В исследовании Renshaw (2004) отмечено, что у больных, чьи опухоли объективно отвечают на лечение летрозолом в течение 3 месяцев, можно ожидать дальнейшего уменьшения объема опухоли при продолжении лечения (9,5% объективных ответов после 3 месяцев лечения и 36% – после 12 месяцев терапии).
Практически все опубликованные исследования характеризуются слишком коротким периодом наблюдения, чтобы можно было определить, приводит ли лечение ингибиторами ароматазы к улучшению выживаемости больных РМЖ. Популяция больных, получающих неоадъювантную эндокринотерапию, характеризуется более пожилым возрастом, а такие больные имеют немало сопутствующих заболеваний. Многие из них, несмотря на наличие местнораспространенного заболевания могут погибать от других причин (не связанных с прогрессированием РМЖ). Поэтому представляется сложным объективно оценить долгосрочную выживаемость у этих пациентов.
На сегодняшний день нет крупных рандомизированных исследований, сравнивающих неоадъювантную эндокринотерапию с химиотерапией, т. к. больные, получающие неоадъювантную химиотерапию, чаще всего пременопаузального возраста с ЭР- негативными опухолями.
Практически два исследования, сравнивающих неоадъювантную химиотерапию с эндокринотерапией выполнены и опубликованы нами (12, 13). В этих исследованиях постменопаузальные женщины с ЭР+ и/или ПР+ опухолями после рандомизации получали или неоадъювантную химиотерапию (доксорубицин + паклитаксел, 4 цикла) или эндокринотерапию (анастразол 1 мг ежедневно или эксеместан 25 мг ежедневно в течение 3 месяцев). Объективный ответ опухолей на лечение оценен в соответствии с критериями ВОЗ клиническим методом (пальпация), маммографией и ультразвуковым исследованием. Как видно из таблиц 2 и 3, показатели общего объективного ответа (CR+PP) оказались статистически схожими в химиотерапевтической и эндокринной группах.
Средняя продолжительность до клинического ответа равнялась 57 дням в группе, получавших эндокринотерапию, и 51 дню, среди подвергавшихся химиотерапии (р>0,05). Патоморфологический полный ответ в первичной опухоли наблюдался у 5,9% среди получавших неоадъювантную химиотерапию и лишь у 3,2% больных в группе, получавших эндокринотерапию.
Органосохраняющие операции выполнены у 33% больных из эндокринной группы и у 23,9% больных, подвергавшихся химиотерапии (р=0,058). При высоком уровне экспрессии рецепторов эстрогенов (≥ 6 Allred) наблюдалась тенденция более частых полных клинических ответов (70% против 60%) и более частого выполнения органосохраняющих операций (42,8% против 23,7%) в группе больных, получавших неоадъювантную эндокринотерапию эксеместаном или анастразолом в сравнении с неоадъювантной химиотерапией (таблица 4).
Прогрессирование заболевания наблюдалось у 9% больных эндокринной группы и 8,5% – у химиотерапевтической группы. 31 женщина (12,9%) не подверглась хирургическому лечению после неоадъювантной терапии: 5,7% в эндокринной группе и 7,2% в химиотерапевтической группе. Из них 22 больные не оперированы из-за прогрессирования заболевания и получили альтернативное лечение: химиотерапию в эндокринной группе и эндокринотерапию в химиотерапевтической группе. Девять больных остались неоперабельными после неоадъювантного лечения.
За средний период наблюдения (36 месяцев) местный рецидив выявлен в 3,3% случаев в эндокринной группе и у 3,4% больных, получавших химиотерапию (р>0,5).
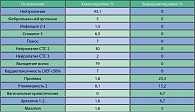
Клиническая характеристика и частота обычно наблюдаемых побочных эффектов представлена в таблице 5. Как видно, основные гематологические и негематологические осложнения достоверно чаще встретились у пациентов, подвергавшихся химиотерапии. Не было серьезных токсических событий среди больных, получавших эндокринотерапию. Не отмечено случаев смертельных исходов во время проведения неоадъювантной системной терапии.
Неоадъювантная эндокринотерапия эксеместаном и анастразолом представляется эффективной и безопасной у постменопаузальных женщин с ЭР+ опухолями. Такое лечение кажется реальной альтернативой химиотерапии у пожилых пациентов с ЭР+ и/или ПР+ РМЖ, для которых низкая токсичность терапии представляется на настоящий момент наиболее предпочтительной и целесообразной.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.