количество статей
7376
Загрузка...
Пожалуйста, авторизуйтесь:
Клинические случаи
Новый индуктор интерферона Кагоцел® в терапии простого герпеса: возможности и перспективы
"ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Дерматовенерология и дерматокосметология" № 2
- Аннотация
- Статья
- Ссылки
Одной из актуальных проблем современной клинической медицины являются вирусные заболевания, в том числе вирусные дерматозы. Особое место среди них занимает простой герпес (ПГ).
Термин «герпес» (от греч. hеrро – «ползти») известен в медицине почти 25 веков. Лихорадочный герпес («простуда») был описан римским врачом Геродотом еще в 100 г. до н. э. Упоминания о нем встречаются в трактатах таких знаменитых врачей прошлого, как Гиппократ, Авиценна и Парацельс.
Через 110 лет, прошедших со времени выделения возбудителя заболевания – вируса простого герпеса (ВПГ) – и последовавшего за этим активного изучения вопросов эпидемиологии, патогенеза, клиники и терапии ПГ, актуальность многих аспектов проблемы остается достаточно высокой.
По современным оценкам, частота инфицированности населения ВПГ приближается к 100%. Сероэпидемиологические исследования показали, что уже сегодня свыше 95% взрослого населения имеют антитела к вирусу того или иного типа, при этом была выявлена стойкая тенденция к росту числа инфицированных. Так, количество носителей только 2 типа ВПГ за последние 15 лет увеличилось примерно на 20% [1].
Такая же ситуация наблюдается в отношении заболеваемости ПГ. Сегодня можно говорить о том, что частота развития клинических проявлений инфекции крайне высока. Она занимает второе место среди вирусных поражений человека, уступая лишь гриппу. Ряд исследований свидетельствуют о том, что, по одним данным, в 20–25% случаев, а по другим – в 60–70% герпетическая инфекция проявляется клинически [2].
Все более возрастающий интерес к проблеме ПГ со стороны врачей различных специальностей связан с рядом объективных моментов.
В частности, с крайне выраженным клиническим полиморфизмом заболевания – от ограниченных поражений кожи, слизистых и глаз до системных, генерализованных форм с вовлечением в вирусный процесс жизненно важных внутренних органов, а также развитием на фоне хронической персистенции ВПГ бесплодия, невынашивания беременности и злокачественных новообразований [3, 9].
В связи с этим в настоящее время наряду с понятием ПГ все большее распространение получает термин «герпетическая болезнь» (ГБ), который как нельзя лучше отражает системный характер негативного действия ВПГ на организм в целом.
Доказано, что местом «обитания» или персистенции ВПГ 1–2 типов, являются чувствительные паравертебральные ганглии вегетативной нервной системы. Механизмы, сдерживающие развитие герпетической инфекции, известны. Это факторы неспецифической (интерфероновой) и специфической (иммунной) систем защиты. Образование интерферонов (ИФН) является врожденной реакцией организма на внедрение вирусов. ИФН (прежде всего α и β) подавляют внутриклеточное размножение вирусов сразу же после внедрения в организм, с помощью естественных киллеров удаляют инфицированный материал и, окружая незараженные клетки, защищают их от вирусной инвазии. На следующем этапе образование ИФН-α и -β увеличивается, начинается синтез ИФН-γ, увеличивается экспрессия генов интерлейкина 1 (ИЛ-1), фактора некроза опухолей (ФНО) и других цитокинов с последующим развитием Т- и В-клеточного иммунитета. Считают, что реакции первого этапа способны уничтожить вирус или блокировать его дальнейшее распространение в течение неопределенно долгого периода времени.
Причиной реактивации вируса, проявляющейся в виде клинических обострений, являются дефекты в системах сдерживания герпетической инфекции, образующиеся под влиянием разнообразных факторов. Триггерами активации латентной инфекции могут быть: стресс, хронические заболевания, сезонные ОРВИ, экологическая обстановка, социально-экономические факторы, недостаточное питание и пр. В большинстве своем они носят презумптивный характер и часто анамнестически не определяются, что ограничивает эффективность лечебных воздействий.
В основе герпетических заболеваний лежат нарушение иммунологического и интерферонового статусов, вторичная негативная иммунная перестройка (угнетение реакций клеточного иммунитета, интерферон-продуцирующей способности лейкоцитов).
Открытие с помощью методов молекулярной биологии механизмов репликации ВПГ, а также изучение взаимодействия вирусов герпеса с чувствительными клетками позволили создать ряд эффективных химиотерапевтических средств, обладающих противогерпетической активностью.
В первую очередь это ацикловир, валацикловир и фамцикловир, которые являются надежными противовирусными средствами. Клинический опыт применения этих препаратов показал, что, быстро и эффективно купируя острые проявления герпесвирусной инфекции (ГВИ), они не предотвращают повторного рецидивирования хронической ГВИ. Существуют и другие недостатки этих препаратов: формирование резистентности штаммов вируса к химиопрепаратам, сохранение терапевтического эффекта только на фоне приема препарата, возможные токсические эффекты (энцефалопатии, диспепсия, поражение печени, органов кроветворения, снижение артериального давления).
Поэтому необходимы меры по активизации системы собственной защиты (интерферонов) для лечения и профилактики вирусных инфекций. Существует два способа такой активизации: введение готовых продуктов (синтетических ИФН) и стимуляция образования собственных ИФН с помощью индукторов.
Однако при применении синтетических интерферонов в лечении ПГ был выявлен ряд недостатков:
- гриппоподобный синдром (ухудшение общего состояния, повышение температуры, головные боли, высокая утомляемость);
- диспепсические явления (снижение аппетита, рвота, ускорение моторики, изжога);
- кожные реакции;
- лейко- и тромбоцитопения, снижение гематокрита;
- повышение уровня печеночных ферментов, развитие протеин- и альбуминурии;
- возможность формирования аутоантител к ИФН.
Применение индукторов интерферона имеет преимущества по сравнению с использованием синтетических интерферонов, что обусловлено следующими факторами:
- образование эндогенного ИФН – более физиологичный процесс, чем постоянное введение больших доз чужеродного ИФН, который к тому же быстро выводится из организма и блокирует по принципу отрицательной обратной связи синтез аутологичных ИФН;
- индукторы ИФН не приводят к образованию в организме антител к ИФН и большей частью низкоаллергенны;
- индукторы ИФН вызывают пролонгированное образование эндогенного ИФН в физиологических дозах;
- индукторы ИФН обладают наряду с прямой противовирусной активностью иммунокорригирующим эффектом, что позволяет отнести их к новому поколению препаратов с универсальным действием.
В последние годы для лечения и профилактики часто рецидивирующего ПГ стал широко применяться новый отечественный пероральный индуктор интерферона Кагоцел® [4, 10, 11].
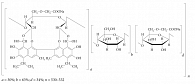
Кагоцел® – гетероцепный полимер молекулярной массой 120–130 кДа, полученный путем химического синтеза из растительного сырья – водорастворимой карбоксиметилцеллюлозы и низкомолекулярного полифенола. После введения в молекулу карбоксиметилцеллюлозы полимера низкомолекулярного полифенола образуется новое соединение с высокой биологической активностью (рис.).
С помощью экспериментальных и клинических исследований была установлена мощная иммуномодулирующая активность препарата Кагоцел®. Основным его свойством является способность индуцировать продукцию ИФН. Он вызывает образование в организме человека смеси так называемых поздних ИФН-α и ИФН-β, которые обладают высокой противовирусной активностью. Кагоцел® стимулирует продукцию ИФН практически во всех популяциях клеток, принимающих участие в иммунном ответе организма на внутриклеточные агенты: Т- и В-лимфоцитах, макрофагах, гранулоцитах, фибробластах, эндотелиальных клетках. При приеме внутрь одной дозы препарата титр ИФН в сыворотке крови достигает максимальных значений через 48 ч. ИФН-ответ организма на введение Кагоцела® характеризуется продолжительной (до 4–5 суток) циркуляцией ИФН в кровотоке. Продукция ИФН в сыворотке крови достигает высоких значений лишь через 48 ч после приема Кагоцела®, в то время как в кишечнике максимум продукции ИФН отмечается уже через 4 ч.
Кагоцел® выпускается в виде таблеток по 0,1 г, содержащих 12 мг активного вещества. Другие компоненты таблеток – крахмал картофельный, кальция стеарат, лудипресс. При назначении в терапевтических дозах Кагоцел® нетоксичен, не накапливается в организме. Препарат не имеет мутагенных и тератогенных свойств, неканцерогенен и не обладает эмбриотоксическим действием. Наибольшая эффективность при лечении Кагоцелом® достигается при его назначении не позднее 4 суток от начала острой инфекции.
Экспериментальные исследования показали, что Кагоцел® в культуре клеток Vero подавляет репродукцию ВПГ 1 и 2 типа, включая мутантные штаммы ВПГ-1,
резистентные к ацикловиру. По мнению авторов, выявление прямой антигерпетической активности, а также эффективности препарата Кагоцел® в отношении мутантных резистентных к антигерпетическим препаратам штаммов ВПГ расширяет перспективы клинического применения препарата, в частности, для комбинированной терапии.
Проведенные клинические испытания эффективности препарата Кагоцел® в терапии хронической рецидивирующей герпетической инфекции показали, что под его влиянием происходит нормализация показателей системы ИФН как α-, так и β-звена у 80–86% больных. Соответственно уменьшаются продолжительность рецидива и сроки реэпителизации эрозивных элементов. В противоположность большинству других индукторов ИФН Кагоцел® стимулирует длительную продукцию ИФН: при однократном его применении ИФН циркулирует в организме пациента на терапевтическом уровне в течение 1 недели, что позволяет эффективно использовать Кагоцел® в профилактических целях.
Указанные свойства обосновывают перспективность клинического применения препарата Кагоцел® в терапии герпесвирусной инфекции.
Основные зарегистрированные показания для применения препарата Кагоцел®:
- лечение герпетической инфекции, включая генитальный и рецидивирующий герпес;
- лечение и профилактика гриппа и других острых респираторных вирусных инфекций (ОРВИ).
Представляют интерес результаты многоцентрового когортного открытого контролируемого исследования препарата Кагоцел® при лечении генитального и лабиального герпеса, проведенного Т.И. Долгих и соавт. [4]. Критерии включения – лица обоего пола в возрасте от 18 до 65 лет с первичным эпизодом и рецидивами генитального и лабиального герпеса. Диагноз герпеса устанавливался на следующих основаниях:
- клиническая картина – наличие клинических признаков, субъективных ощущений, локализация воспалительного процесса на гениталиях и гладкой коже;
- данные лабораторных исследований – лабораторные показатели герпесвирусной инфекции (ПЦР), общий анализ крови.
Всего под наблюдением находились 146 пациентов: 63 мужчины и 83 женщины.
По данным ПЦР-исследования, ВПГ-1 был определен у 30 (20,5%) больных, ВПГ-2 – у 49 (33,5%), 1 и 2 типы ВПГ – у 23 (15,8%), ВПГ без определения типа – у 18 (12,3%), отрицательный результат был получен у 6 (4,1%) пациентов, у 20 (13,8%) больных исследований не проводилось.
Больные были разделены на 3 группы. Пациенты I группы получали только Кагоцел® (106 больных: 48 мужчин и 58 женщин), II – Кагоцел® и Ацикловир (10 больных: 4 мужчин и 6 женщин), III – только Ацикловир (30 больных: 12 мужчин, 18 женщин).
Схема лечения Кагоцелом® больных основной группы была следующей: при первичном эпизоде и рецидивах – по 2 табл. 3 раза в сутки в течение 5 дней. Больным III группы при первичном эпизоде и рецидивах назначали по 1 табл. (200 мг) Ацикловира 5 раз в день в течение 5 дней; больные II группы получали одновременное лечение Кагоцелом® и Ацикловиром по указанным схемам. Выраженность клинических признаков – боли, зуда, жжения, эпителизации эрозий, очищения от высыпаний – оценивалась в баллах до лечения, на 5-й день лечения и через 10 дней после его окончания. Сравнительный анализ клинической оценки эффективности лечения показал, что наилучшие результаты получены у больных
I и II групп: эволюция клинических проявлений завершилась через 5,6 и 3,2 дня соответственно, тогда как в III группе этот срок составил 6,4 дня. При наблюдении в течение года после лечения рецидивов не отмечалось у 22,2% пациентов, у 11% был один рецидив, у 38,9% – два рецидива и у остальных – три рецидива. При оценке безопасности Кагоцела® ни у одного больного не было отмечено побочных действий и случаев отмены препарата, а также не наблюдались неблагоприятные или серьезные неблагоприятные явления.
Другое сравнительное рандомизированное клиническое исследование эффективности лечения больных генитальным герпесом с применением Кагоцела® проведено Г.И. Мавровым и соавт. в Институте дерматологии и венерологии АМН Украины [8].
Оно включало 46 больных (24 мужчины и 22 женщины, возраст от 25 до 31 года), страдающих рецидивирующим генитальным герпесом, с давностью заболевания от 1 года до 5 лет. Частота эпизодов высыпаний на гениталиях составляла 8–15 в год.
Рандомизацию проводили с помощью генератора случайных чисел (четное число – основная группа, нечетное – группа сравнения).
В результате было сформировано 2 группы по 23 человека. Кагоцел® получали только пациенты из основной группы по следующей схеме: по 2 табл. 3 раза в сутки в течение 5 дней (на курс 30 табл.).
В качестве этиотропной терапии все пациенты получали Ацикловир по 800 мг 4 раза в сутки.
При обследовании выявлено, что состояние системы ИФН у больных на фоне рецидива заболевания характеризовалось значительными нарушениями. У 37 пациентов до начала лечения наблюдалось резкое снижение титров индуцированного ИФН-α. При этом показатели ИФН-γ находились в пределах нормы у 28 больных. До лечения показатели сывороточного ИФН были повышены у 43 пациентов. У 15 пациентов наблюдалась спонтанная продукция ИФН, которая в норме отсутствует.
В результате комбинированной терапии (Кагоцел® в сочетании с Ацикловиром) отмечались постепенная нормализация показателей ИФН-статуса и улучшение клинической картины заболевания. Показатели индуцированных ИФН-α и ИФН-γ нормализовались у 20 пациентов из основной группы (n = 23). Нормализация показателей ИФН-статуса соответствовала улучшению клинической картины заболевания у большинства больных.
У данных пациентов также сократилась продолжительность рецидива с 6,4 ± 2,3 суток (в группе сравнения) до 3,5 ± 1,8 суток (в основной группе). Частота рецидивов на протяжении 6 месяцев снизилась с 6,1 ± 2,2 до 2,2 ± 1,5 в основной группе, до 3,1 ± 2 в группе сравнения.
Таким образом, в результате лечения Кагоцелом® в сочетании с Ацикловиром продолжительность течения рецидива в среднем сокращалась с 5–8 до 3–4 суток, что подтверждалось нормализацией показателей ИФН-статуса к моменту окончания рецидива. Была показана хорошая переносимость Кагоцела® и обоснована целесообразность его включения в комплексную терапию рецидивирующего генитального герпеса.
Клинико-иммунологическая эффективность препарата Кагоцел® также подтверждается в проспективном когортном рандомизированном исследовании, проведенном Т.И. Долгих и соавт. в Омской государственной медицинской академии [5], в которое были включены 23 пациента (18 женщин и 5 мужчин) в возрасте от 17 до 49 лет с верифицированным диагнозом герпетической инфекции с проявлением лабиального (8 пациентов) и генитального (15 пациентов) герпеса и давностью заболевания от 1 года до 14 лет.
Кагоцел® назначали пациентам по 2 табл. 3 раза в день в течение 5 дней.
Подтверждение активности инфекционного процесса с уточнением этиологической расшифровки проводилось на основе наличия специфического IgA к ВПГ 1 и
2 типов и результатов прямых методов исследований лейкоцитарной взвеси и/или соскобов из очагов инфекции: «ранние» белки ВПГ-1 и ВПГ-2 выявляли в реакции иммунофлюоресценции, а ДНК – методом ПЦР.
Содержание ИФН-α и ИФН-γ (спонтанного и стимулированного фитогемагглютинином), а также компонентов комплемента С3 и С4 оценивали до назначения иммунотропной терапии и в динамике через 10 и 30 дней.
Оценка эффективности препарата показала улучшение состояния у 87,5% пациентов. Через 10 дней после лечения Кагоцелом® отмечено уменьшение клинических проявлений: болевой синдром купирован у 98% пациентов, зуд и жжение сохранялись лишь у 6% пациентов с проявлениями генитального герпеса, отек и гиперемия имели место у 4% пациентов. В 98% случаев значительно уменьшилась кратность рецидивов (0–2 раза в год вместо 3–12 раз), а длительность обострения сократилась до 3–8 дней (до лечения – 8–14 дней).
На 10-й день после проведения терапии Кагоцелом® у всех пациентов при исследовании лейкоцитарной взвеси ДНК и ранние белки вируса не определялись, что свидетельствовало о прекращении его репликации.
Установлено, что через 30 суток после окончания терапии Кагоцелом® статистически значимо изменяются все изученные показатели иммунного статуса. Продукция ИФН-α по сравнению с исходными данными возросла с 2,5 (0,6; 3,6) до 5,27 (3,25; 7,13) пг/мл, т.е. в 2,1 раза. Отмечено увеличение содержания спонтанного ИФН-γ с 21,9 (18,1; 28,1) до 33,48 (27,30; 46,15) пг/мл, а уровень стимулированного ИФН-γ увеличился с 450,5 (279,4; 740,6) до 848,34 (663,38; 1345,7) пг/мл, т.е. в 1,5 и 1,9 раза соответственно.
На основании проведенных исследований установлено следующее:
- препарат Кагоцел® в виде монотерапии является эффективным средством для лечения поражений, вызванных ВПГ;
- применение Кагоцела® прерывает развитие клинических проявлений герпесвирусной инфекции и позволяет снизить частоту рецидивов в 3–4 раза;
- Кагоцел® хорошо переносится пациентами, побочных явлений терапии препаратом не отмечалось.
Особо отметить следует уменьшение числа рецидивов ПГ у пациентов, получивших курс терапии препаратом Кагоцел®. Таким образом, Кагоцел® целесообразно использовать не только в качестве средства, купирующего обострение ВПГ, но и в целях профилактики заболевания, что значительно улучшает качество жизни больных, страдающих рецидивирующим простым герпесом.
Умеренная стоимость, хорошая переносимость препарата наряду с его клинико-иммунологической эффективностью (прямое противовирусное действие, повышение неспецифической и специфической резистентности организма) позволяют рекомендовать Кагоцел® для лечения и профилактики рецидивов простого герпеса.
1. Куле Ж.П. Основные тенденции в эпидемиологии вирусных инфекций папилломы человека (ВПЧ), простого герпеса 2 (ВПГ-2) и гепатита В во Франции // Вестник дерматовенерологии. 2000. № 6. С. 59–60.
2. Герпес: неизвестная эпидемия (патогенез, диагностика, клиника, лечение) / Под ред. Л.Н. Хахалина. Смоленск: Фармаграфикс, 1997. С. 162.
3. Баринский И.Ф., Шубладзе А.К., Каспаров А.А., Гребенюк В.Н. Герпес: этиология, диагностика и лечение. М., 1986.
4. Долгих Т.И., Масюкова С.А., Петренко Л.А. и др. Эффективность и переносимость препарата Кагоцел при лечении герпетической инфекции // Медлайн-экспресс. 2007. № 2. С. 34–36.
5. Долгих Т.И., Минакова Е.Ю., Запарий Н.С. Клиникоиммунологическая оценка эффективности применения Кагоцела при лечении пациентов с рецидивирующей герпетической инфекцией // Рос. журн. кож. и вен. бол. (Прилож.: Герпес). 2010. № 1. С. 15–18.
6. Ершов Ф.И., Киселев О.И. Интерфероны и их индукторы (от молекул до лекарств). М.: ГЭОТАР-Медиа, 2005. C. 356.
7. Европейские стандарты диагностики и лечения заболеваний, передаваемых половым путем / Под ред. К. Рэдклифа, В.П. Адаскевича. М.: Мед. литература, 2006. C. 264.
8. Мавров Г.И., Чинов Г.П., Нагорный А.Е. Эффективность лечения больных генитальным герпесом с применением индуктора эндогенных интерферонов Кагоцела // Рос. журн. кож. и вен. бол. (Прилож.: Герпес). 2007. № 1. С. 30–32.
9. Коломиец А.Г., Малевич Ю.К., Коломиец Н.Д. Вирус простого герпеса и его роль в патологии человека. Минск, 1986.
10. Масюкова С.А., Гладько В.В., Устинов М.В., Егорова Ю.С. Кагоцел в лечении генитального герпеса // Рос. журн. кож. и вен. бол. (Прилож.: Герпес). 2006. № 2. С. 48–52.
11. Оспельникова Т.П., Полонский В.О., Наровлянский А.Н. и др. Эффективность препарата Кагоцел при хроническом рецидивирующем генитальном герпесе // Медлайн-экспресс. 2006. № 2–3. С. 39–41.
Новости на тему
17.08.2022 01:00:00
18.09.2014
Отправить статью по электронной почте
Ваш адрес электронной почты:
Адрес электронной почты получателя:
Разделите несколько адресов электронной почты запятой
Сообщение(не обязательно)
Не более 1500 символов
Анти спам:
Для предотвращения спама, пожалуйста, введите в поле слово, которое видите ниже.
Обновить код
* адреса предоставленные Вами будут использоваться только для отправки электронной почты.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.