Препараты алендроновой кислоты в лечении остеопороза
- Аннотация
- Статья
- Ссылки

Остеопороз (ОП) – прогрессирующее системное заболевание скелета, характеризующееся снижением массы кости и нарушением структуры (микроархитектоники) костной ткани, приводящее к увеличению хрупкости кости и риску возникновения переломов [1]. ОП относится к числу наиболее распространенных заболеваний, являясь одной из главных причин переломов шейки бедра и тел позвонков, а следовательно, инвалидизации больных. По данным ВОЗ, среди неинфекционных заболеваний ОП занимает четвертое по частоте место после болезней сердечно-сосудистой системы, онкологической патологии и сахарного диабета. В России, по данным НИИР РАМН, частота ОП и остеопении у женщин старше 50 лет составляет 34% в поясничном отделе позвоночника и 43% в шейке бедренной кости; у мужчин – 27% и 44% соответственно (работа выполнена в рамках Европейской программы изучения остеопороза позвоночника – EVOS) [2]. При обследовании другой крупной когорты больных – 2155 женщин в возрасте 55 лет и старше, наблюдавшихся в поликлинике Центрального округа г. Москвы, – частота ОП в поясничном отделе позвоночника составила 29,8% [3]. Данные по частоте переломов тоже неутешительны: около 40% женщин и 13% мужчин европеоидной расы в возрасте 50 лет и старше имеют, по крайней мере, один клинически значимый перелом [4]. А тот факт, что переломы костей при ОП возникают даже вследствие небольшой травмы, например, падения с высоты собственного роста или подъема тяжестей, делают ОП важной социально-экономической проблемой.
Учитывая вышесказанное, лечение ОП должно быть направлено прежде всего на снижение риска переломов скелета. На сегодняшний день существует достаточно большой спектр лекарственных средств для лечения данного заболевания. Но наиболее эффективными препаратами, бесспорно, являются бисфосфонаты [5–7].
Несмотря на то что история бисфосфонатов начинается с XIX века, в медицине они применяются относительно недавно, а первоначально их использовали для смягчения воды в ирригационных системах. В дальнейшем, благодаря открытию их способности предотвращать растворение гидроксиапатита, были предприняты попытки применения бисфосфонатов для лечения нарушений костного метаболизма (болезни Педжета и гиперкальциемии опухолевого генеза). Это произошло лишь в 1960-е гг., а реальный механизм действия бисфосфонатов был продемонстрирован совсем недавно – в 1990-е гг. – на примере алендроната [8].
Бисфосфонаты являются синтетическими аналогами пирофосфатов костного матрикса, которые устойчивы к расщеплению ферментами. Основной механизм действия всех бисфосфонатов направлен на ингибирование костной резорбции путем подавления активности остеокластов, что приводит к увеличению костной массы. Алендронат относится ко второму поколению бисфосфонатов, содержащих в своей химической структуре один атом азота. Эти азотсодержащие бисфосфонаты, вошедшие в медицинскую практику в конце 80-х гг. ХХ века, оказывают более активное антирезорбтивное действие по сравнению с препаратами первого поколения (клодронат, этидронат). Это обусловлено особенностью метаболизма бисфосфонатов I поколения, которые метаболизируются с образованием соединений – аналогов АТФ. Эти соединения накапливаются в остеокластах и нарушают их функцию. Аминобисфосфонаты имеют принципиально иной механизм действия: сами они не метаболизируются, но вмешиваются в процесс обмена мевалоната (путем ингибирования фермента фарнезил-пирофосфатазы), нарушая тем самым дифференцировку предшественников остеокластов, а также стимулируя апоптоз зрелых клеток. Проникая в костную ткань, бисфосфонаты создают высокую концентрацию в лакунах резорбции и уменьшают их глубину (как было показано в исследованиях in vitro).
Кроме того, бисфосфонаты способствуют увеличению количества остеобластов в губчатой и кортикальной кости, а также снижению секреции остеобластами остеокласт-стимулирующего фактора.
Все вышеперечисленное вместе способствует восстановлению объема кости и повышению ее прочности, а следовательно, снижению риска переломов. Эффективность алендроната в отношении всех видов переломов подтверждена большим числом длительных клинических исследований. Было проведено несколько крупных многоцентровых рандомизированных плацебоконтролируемых исследований по изучению эффективности алендроната при ОП:
- исследование FOSIT, включающее 153 центра в 34 странах-участницах и 1908 женщин постменопаузального возраста с ОП, длительность исследования 1 год [9];
- исследование FIT, включающее 11 центров США и 3658 женщин в постменопаузе, длительность 3 года [10];
- исследование FLEX – 10-летнее наблюдение пациентов, продолжавших получать 5 мг и 10 мг алендроната либо переведенных в группу плацебо после 5 лет терапии алендронатом [11].
Во всех исследованиях ежедневный прием 10 мг алендроната показал высокую эффективность, увеличивая минеральную плотность кости (МПК) в шейке бедра и позвоночнике (уровень доказательности А) и достоверно снижая частоту переломов в позвоночнике, шейке бедренной кости и предплечье.
По данным исследования FLEX, у пациентов, переведенных на плацебо после 5 лет терапии алендронатом, отмечалось снижение МПК в проксимальных отделах бедра (-2,4%; 95% ДИ (-2,9)–(-1,8)%; р < 0,001) и в поясничном отделе позвоночника (-3,7%; 95% ДИ (-4,5)–(-3,0)%; р < 0,001), однако значения МПК не возвращались к исходному уровню, а риск периферических переломов достоверно между группами не различался.
В дальнейшем были опубликованы данные об эффективности терапии алендронатом по сравнению с плацебо в сочетании с препаратами кальция и витамина D. Так, по данным Кохрановского систематического обзора [12], анализирующего результаты 11 РКИ (12 068 женщин), проведенных за период с 1966 по 2007 г., было отмечено значимое снижение абсолютного риска переломов позвонков (на 6%), шейки бедренной кости (на 1%) и периферических переломов (на 2%) у больных, получавших терапию алендронатом (уровень доказательности А).
Таким образом, использование алендроната остается актуальным по сегодняшний день, по мнению многих авторов, препарат является «золотым стандартом» в лечении ОП. Дальнейшее направление в использовании алендроновой кислоты связано с разработкой пролонгированных препаратов, создающих возможность интермиттирующего введения, что является более рациональным как с медицинской точки зрения, так и по соображениям комплаентности.
В нескольких рандомизированных плацебоконтролируемых исследованиях было продемонстрировано, что прием алендроната один раз в неделю в дозе 70 мг терапевтически эквивалентен ежедневной дозе препарата 10 мг. Кроме того, для данной формы препарата отмечалась лучшая переносимость, в частности, меньшая частота нежелательных явлений со стороны верхних отделов желудочно-кишечного тракта [13–17].
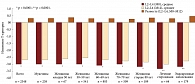
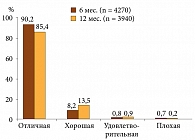
Постмаркетинговое неинтервенционное исследование Осталона (алендронат натрия тригидрат, 1 таблетка которого содержит 91,35 мг, что соответствует содержанию 70 мг алендроновой кислоты) длительностью 12 месяцев (апрель 2006 г. – июнь 2007 г.), проведенное в 294 центрах по лечению остеопороза в Венгрии и включающее 4360 пациентов с остеопорозом, показало хорошую эффективность и переносимость препарата (рис. 1–3).
Именно эти преимущества были учтены при создании препарата Осталон® Кальций-Д, который представляет собой комбинацию таблеток, содержащих алендроновую кислоту в дозе 70 мг (№ 4), и таблеток, содержащих колекальциферол – активную форму витамина D – 400 МЕ (10 мкг) и кальция карбонат с содержанием 600 мг ионизированного кальция (№ 28). Подобная форма выпуска является очень удобной для пациентов, поскольку включает полный набор препаратов, необходимых для лечения ОП в течение месяца, и, следовательно, способствует повышению комплаентности.
Следует отметить, что биодоступность колекальциферола в комбинации с алендроновой кислотой сходна с его биодоступностью при изолированном приеме. Биодоступность алендроновой кислоты при приеме натощак (за 2 часа до еды) составляет 0,64%, T1/2 – 72 часа, конечное T1/2 (выведение из костной ткани) – более 10 лет.
Показаниями к применению препарата Осталон® Кальций-Д являются:
- остеопороз у женщин в постменопаузе (снижение риска развития переломов, в т.ч. переломов бедренной кости и компрессионных переломов тел позвонков);
- остеопороз у мужчин (снижение риска развития переломов);
- остеопороз, вызванный длительным приемом глюкокортикостероидов.
Дозировка препарата традиционна: таблетки, содержащие алендроновую кислоту, назначают по 70 мг 1 раз в неделю. Таблетки, содержащие комбинацию «колекальциферол + кальция карбонат», назначают по 1 шт. ежедневно, не ранее чем через 3 ч после приема алендроновой кислоты. Наличие в составе Осталон® Кальций-Д витамина D3 (колекальциферола) является бесспорным преимуществом препарата. Витамин D является основным регулятором гомеостаза кальция и фосфора в организме человека и необходим для нормальной минерализации костей. Витамин D усиливает всасывание ионов кальция и фосфора в тонком кишечнике и снижает их выделение почками. Известно, что ионы кальция всасываются в основном в проксимальной части тонкого кишечника, при этом только 10% всасывается пассивно, а подавляющая часть кальция – 90% – путем активного механизма, контролируемого витамином D. В свою очередь, витамин D3 поступает с пищей растительного происхождения, а также образуется в коже из витамина D2 под действием ультрафиолетовых лучей. Однако поступающий с пищей витамин D всасывается только на 50%, а небольшое количество солнечных дней в большинстве стран Европы и северных областях и средней полосе России приводит к его дефициту. По данным немецких исследователей (N. Breijawi и соавт.) [18], у 84,7% обследованных авторами пациентов с ОП и остеоартрозом имелся дефицит витамина D3.
Таким образом, очевидно, что пациентам с ОП необходимо дополнительное поступление витамина D3, который подвергается в организме дальнейшему превращению: в печени – в 25-гидроксиколекальциферол и далее в почках – в активную форму 1,25-дигидроксиколекальциферол.
Дальнейшие исследования показали, что снижение уровня 1,25-дигидроксивитамина D может приводить не только к нарушению минерального обмена, но и к развитию миопатии, проявляющейся в слабости проксимальных мышц, изменению походки, трудностям при вставании с постели и со стула. H.A. Bischoff и соавт. [19] в 1999 г. показали, что у пожилых людей (старше 65 лет) наблюдается обратная корреляция между концентрацией 1,25-дигидроксивитамина D в сыворотке крови и силой разгибания в коленном суставе. Позднее этими же авторами была выявлена ассоциация между нормальным уровнем витамина D и более высокой мышечной силой рук, лучшей способностью вставать со стула и меньшим риском падений [20]. Это еще раз подтверждает целесообразность применения препаратов витамина D у больных ОП с целью оптимизации нервно-мышечной функции и профилактики падений, в большинстве случаев приводящих к переломам.
Недавнее исследование S.H. Scharla и соавт. [21] описывает эффекты витамина D (альфакальцидола) на метаболизм кости, уровень цитокинов, силу мышц и выраженность боли у пожилых пациентов с ревматоидным артритом и остеопенией. При анализе результатов было обнаружено, что в группе больных, принимавших 1 мкг альфакальцидола + 500 мг кальция ежедневно, значительно снижалось содержание маркера костной резорбции (NTX) в моче. Кроме того, прием альфакальцидола сопровождался достоверным снижением уровня ФНО-α. Данный факт подтверждает предварительные данные, опубликованные G. Hein и P. Oelzner, отметивших снижение уровня ФНО-α и ИЛ-6 у больных ревматоидным артритом [22]. В работе S.H. Scharla и соавт. подтверждено увеличение мышечной силы у пациентов, принимавших альфакальцидол, а также отмечено улучшение суммарного показателя боли, что может быть объяснено снижением содержания ФНО-α (коррелирующего с выраженностью боли) и улучшением мышечной функции.
Таким образом, препарат кальция и витамина D, входящий в состав Осталон® Кальций-Д, дополняет действие алендроновой кислоты, повышая эффективность препарата.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.