Радиологические исследования почек у детей
- Аннотация
- Статья
- Ссылки
- English
Введение
Диагноз любого заболевания во многом зависит от возможностей применяемых методов визуализации патологии. Диагностическая радиология кардинально изменила врачебную тактику. Ранее в качестве радиологического золотого стандарта в детской нефрологии рассматривались экскреторная урография и микционная цистоуретрография. Сегодня они дополняются ультразвуковыми и изотопными исследованиями, компьютерной томографией (КТ) и магнитно-резонансной томографией (МРТ) [1, 2].
В детской нефрологии чаще всего радиологические исследования проводятся при инфекции мочевыводящих путей и объемных образованиях в брюшной полости. Показаниями к проведению этих исследований также являются врожденные пороки, травма, артериальная гипертензия, ряд других заболеваний внутренних органов, влияющих на функцию и морфологию мочевыводящей системы.
Методические проблемы
Хотя диагностические возможности многих интервенционных методик при ряде патологических состояний практически одинаковы, нередко их выбор у детей определяется несколько иными критериями, чем у взрослых. Цель и задачи диагностического поиска устанавливаются клиницистом и специалистом по диагностической радиологии. Выбор методик и очередность их применения обусловлены не только потенциальным диагнозом, но и возрастом пациента. Радиологические исследования требуют строгих показаний и соответствия всем требованиям безопасности. Очень часто гонады оказываются вне зоны анатомического интереса, доза облучения сводится к минимуму. Ребенок, неадекватно реагирующий на исследование, должен быть иммобилизован вплоть до применения седации. Максимум диагностической информации необходимо получать при минимуме материальных затрат, числа исследований и дискомфорта.
Экскреторная урография
Экскреторная урография часто единственное и завершающее исследование мочевыводящей системы [3]. Экскреторная урография показана после получения ультразвуковых заключений об аномалиях почек, уролитиазе, минимальной (без разрыва) и изолированной травме почки, недержании мочи (при подозрении на экстравезикальную эктопию мочеточника).
Рентгенологу необходимо ознакомиться с анамнезом, клинической картиной, результатами инструментальных и лабораторных исследований, убедиться в отсутствии реакций на контрастные препараты в ходе предыдущих исследований, иметь четкое представление о состоянии водно-электролитного баланса.
Противопоказаниями к экскреторной урографии являются тяжелая дегидратация и шок, а также беременность (исключать у девочек-подростков).
Гломерулярная фильтрация у новорожденного в первые три-четыре дня жизни едва достигает 20% показателей взрослого, к четвертому-пятому дню – 30%, к десятому – 50%. Визуализация почек затруднена, экскреторная урография у новорожденных до двухнедельного возраста нерациональна. У детей раннего и младшего возраста никакой подготовки не требуется. У детей более старшего возраста иногда выполняется очищение толстого кишечника.
Ионные контрастные препараты гиперосмолярны, поэтому перед выполнением экскреторной урографии перерыв в приеме жидкости не может превышать три-четыре часа. Перед исследованием необходимо корригировать любое обезвоживание. Грудное кормление необходимо завершить за три-четыре часа до исследования. Этот интервал исключает обезвоживание и в то же время гарантирует освобождение желудка. Последнее снижает риск аспирации при возможной рвоте. Современные неионные препараты обычно не вызывают рвоты, характеризуются меньшим количеством побочных эффектов, улучшают визуализацию собирательной системы. Их осмолярность ниже (600–700 мОсм/л), чем ионных. В случае попадания препарата в окружающие ткани повреждающий эффект минимален. Однако стоимость неионных препаратов в 10–20 раз выше, чем ионных. На наш взгляд, неионные препараты следует применять у детей грудного возраста, пациентов с повышенной проницаемостью сосудов, в ходе поднаркозного исследования, на фоне критических состояний (гемодинамическая и дыхательная нестабильность, шок, дегидратация), а также если ранее имели место реакции на контрастные препараты. Кроме того, эти препараты целесообразно использовать:
- при атопии;
- астме;
- выполнении ангиографии;
- аритмии;
- врожденных пороках сердца синего типа;
- наличии катетера в центральной вене;
- диабете;
- гемолитическом кризе;
- нефротическом синдроме;
- почечной недостаточности;
- кистозных почках;
- состоянии после трансплантации (стволовых клеток, почек, сердца и т.д.).
Все контрастные средства являются гипертоническими относительно крови, поэтому перед внутривенной инъекцией надо убедиться в адекватной гидратации пациента.
Единого мнения о дозе контрастного препарата нет. Исходя из собственного опыта, рекомендуем ионный препарат в дозе 2 мл/кг массы тела, но не более 4 мл/кг. Неионный контрастный препарат можно вводить в дозе 1–2 мл/кг массы тела.
Микционная цистоуретрография
Микционная цистоуретрография выявляет анатомические особенности мочевого пузыря, уретры, наличие/отсутствие везикоуретрального рефлюкса. Показаниями к ее проведению являются инфекция мочевыводящих путей, уретроэктазия или уретропиелокаликоэктазия (на основании данных ультразвукового исследования (УЗИ)), аноректальные мальформации, синдром «чернослива», миктурия и анурия у новорожденных, неонатальный асцит, энурез. Иногда микционная цистоуретрография выполняется как часть экскреторной урографии. В таком варианте исследование более физиологично, нет риска развития катетер-ассоциированных инфекций и раздражения мочевого пузыря. Но в этом случае можно не обнаружить минимальный рефлюкс. Особой подготовки не требуется. Перед катетеризацией следует убедиться в отсутствии внешних повреждений (гипоспадия, фимоз, баланит, спайки половых губ), которые могут затруднить выполнение исследования. У подростков катетеризацию должен проводить исследователь того же пола.
Сцинтиграфия
Сцинтиграфия с технецием 99m (Tc99m) – идеальная изотопная методика для детского возраста. Общая и локальная дозы радиации низкие, а время полураспада составляет шесть часов. Скорость выведения используемого носителя изотопа (диэтилентриаминпентауксусная кислота (ДТПУК)) определяется гломерулярной фильтрацией, не зависит от тубулярной секреции или абсорбции. ДТПУК характеризуется высокой аффинностью к коре почек. Сцинтиграфия показана в целях диагностики псевдоопухоли почки, аномалий ее положения, артериальной гипертензии, инфекции мочевыводящих путей и везикоуретерального рефлюкса. Расширение верхних мочевыводящих путей существенно затрудняет дифференциальную диагностику наличия/отсутствия обструкции [4]. Ответ на вопрос дает ренография на основе фуросемида. Фуросемид (Лазикс) назначают внутривенно в дозе 1–2 мг/кг через 30 минут после введения изотопа. Снимки делают через две, четыре, шесть, восемь, десять и 20 минут после введения фуросемида. Изучают как сцинтиграммы, так и гистограммы (активность/время).
Компьютерная томография
Компьютерная томография – высокодостоверный метод выявления патологии почек. По сравнению с экскреторной урографией КТ позволяет получить пространственное изображение почек независимо от их функции. Применение контраста повышает точность диагностики. КТ в отличие от УЗИ не зависит от газов или костных структур, точнее передает функциональные и анатомические особенности почек. КТ часто используется в дополнение к экскреторной урографии или УЗИ, когда требуется уточнить диагноз или выявить состояние окружающих тканей, наличие метастазов.
Магнитно-резонансная томография
Магнитно-резонансная томография особенно показана при диагностике опухолей почек и надпочечников.
Ангиография
Ангиография почек абсолютно показана при подозрении на стеноз почечной артерии или внутрипочечных ветвей, при травматическом повреждении сосудистой ножки, псевдоаневризме, артериовенозной фистуле. В настоящее время ангиография дополняется интервенционной ангиографией, позволяющей транслюминально стентировать стенозы. После операции пациент должен длительно получать блокаторы ангиотензинпревращающего фермента, снижающие риск рестенозирования.
Ультразвуковое исследование
Ультразвуковое исследование – первый и нередко завершающий этап диагностического поиска в детской уронефрологии. Методика основана на различии импеданса здоровых и патологически измененных тканей. В настоящее время используются аппараты УЗИ, работающие в режиме КТ или МРТ и создающие трехмерное изображение. Показаниями к проведению УЗИ являются объемные образования брюшной полости, инфекция мочевых путей, высокий риск аномалий почек и опухолей, обструктивная уропатия, неонатальный асцит и анасарка, «немые почки», лейкозная или лимфоматозная инфильтрация почек, локализация почек для биопсии, контроль трансплантата, опухоли и воспалительные заболевания таза и т.д. УЗИ предоставляет достоверную информацию о структуре почки. В норме кора почки выглядит как очень нежная тонкая эхоструктура, в то время как эхогенность мозгового вещества выше. Объективизация оценки плотности паренхимы почки достигается сравнением ее плотности с плотностью печени или селезенки. У новорожденных, особенно недоношенных, за счет небольшого числа клубочков и относительно большей доли паренхимы эхогенность почки несколько выше, чем у детей более старшего возраста. В норме эхогенность почки ниже, чем эхогенность паренхимы здоровой печени (первая степень эхогенности). В случае патологии эхогенность почки приближается к эхогенности паренхимы печени (вторая степень), превышает ее (третья степень) или даже соответствует эхогенности чашечно-лоханочной системы (четвертая степень эхогенности, фиброзированная почка, как правило, «рентгенологически немая»). Стенки чашечек и лоханки состоят в основном из достаточно плотной соединительной ткани. Поэтому плотность чашечно-лоханочной системы, по данным УЗИ, при гломерулонефритах или интерстициальных нефритах, салиурии не меняется. Все заключения о повышении плотности чашечно-лоханочной системы, к сожалению, полностью субъективны и не должны интерпретироваться клиницистами.
Дуплексная допплерография
Для определения васкуляризации почек применяется дуплексная допплерография, во многих случаях заменяющая ангиографию. Почечные артерии наилучшим образом сканируются в поперечной проекции с использованием в качестве маркеров верхней мезентериальной артерии и почечной вены. Скорость допплеровской волны и индекс резистентности определяют при подозрении на стеноз основной почечной артерии или ее ветвей. Индекс резистентности трансплантата используется для оценки его жизнеспособности: повышение индекса свидетельствует об отторжении.
Клинические аспекты
Варианты изображения здоровой почки
Фетальная дольчатость почки считается ее возрастной особенностью. Почка – дольчатый орган, состоящий из семи передних и семи задних сегментов (долей), разделенных тонкими перегородками соединительной ткани. Иногда фиброзный тяж, ограничивающий передние и задние доли, визуализируется как внутрипочечная перегородка. В местах соприкосновения долей на поверхности почки возникает небольшое вдавление, что придает почке плода и новорожденного фестончатый вид. Наблюдая подобную картину, врач может заподозрить рубцевание почки при хроническом атрофическом пиелонефрите. Но в противоположность пиелонефритным рубцам точки естественного втяжения проецируются в пространство между чашечками, а не на чашечки, общие размеры почки не изменены, сами чашечки не деформированы.
При экскреторной урографии аберрантный сосочек пирамидки проецируется в просвет чашечки или лоханки. В этом случае сосочек пирамидки выглядит как круглый или овальный дефект наполнения. Но при многоосевом просвечивании, а также по результатам УЗИ он хорошо дифференцируется от опухоли, камня, тромба, некроза верхушки пирамидки, кистозного пиелита.
Псевдоопухоли почки
Хорошо известным симулятором опухоли почки является гипертрофия столбиков Бертини. В норме столбик (септа) Бертини представляет собой кортикальную ткань между пирамидками почки. При локальной гипертрофии столбик Бертини вдается в собирательную систему, обычно между чашечками верхней и средней третей почки. При экскреторной урографии плотность гипертрофированного столбика Бертини выше плотности мозгового вещества почки и соответствует плотности коркового слоя.
Компенсаторная гипертрофия здоровой почки развивается у пациентов с односторонним поражением противоположной почки. Это наблюдается при нефрэктомии, агенезии, гипоплазии. Компенсаторная гипертрофия не должна восприниматься как неоплазия. Иногда при уменьшенной почке противоположная здоровая почка воспринимается исследователем как увеличенная, что приводит к абсолютно необоснованному длительному и утомительному диагностическому поиску. Причина ошибки – субъективизация, нежелание исследователя пользоваться объективными показателями (номограммами).
Воспалительная псевдоопухоль почки (инфекционная нефрония) выглядит как внутрипочечная масса, нарушающая или деформирующая чашечно-лоханочную систему. В начальном периоде формирования очаг воспаления, по данным УЗИ, может быть гипоэхогенным или смешанной эхогенности, впоследствии – гиперэхогенным. Почка увеличивается в размерах, стирается граница между корковым и мозговым веществом, общая эхогенность увеличивается. Экскреторная урография наряду с увеличением почки демонстрирует слабое заполнение чашечек и лоханки. Воспалительная (инфекционная) псевдоопухоль наблюдается при флегмоне почки, карбункуле, ксантогранулематозном пиелонефрите, остром пиелонефрите, крайне редко при одностороннем гломерулонефрите. Диагноз проясняют общая интоксикация, лихорадка, боль в пояснице, мочевой синдром. При необходимости выполняется КТ или МРТ.
Врожденные аномалии почек
Двусторонняя агенезия почек встречается редко. Аномалия чаще регистрируется у плода мужского пола, обычно мертворожденного. Длительность жизни новорожденного с такой патологией не превышает нескольких дней. В подавляющем большинстве случаев отмечается маловодие. У плода с отсутствующими почками обнаруживаются характерные признаки синдрома Поттера (большие низко расположенные ушные раковины с дефицитом хряща, гипертелоризм, эпикант, микрогнатия, гипоплазия легкого, нередко с пневмотораксом и пневмомедиастинумом). Почечные артерии отсутствуют. Мочеточники могут отсутствовать, Льетодиев треугольник не выражен, мочевой пузырь и мочеиспускательный канал гипоплазированы. Часты пороки гениталий и желудочно-кишечного тракта. Анурия у новорожденного служит показанием к немедленному радиологическому исследованию. По данным УЗИ, ткань почек не обнаруживается, почечные артерии не выявляются. При сцинтиграфии не обнаруживается функционирующая почечная паренхима. По результатам умбиликальной аортографии, почечные артерии не визуализируются. Условием успешной реализации последней методики и получения достоверных результатов является достаточное заполнение аорты контрастом. Двусторонняя агенезия почек несовместима с жизнью.
Односторонняя агенезия почки встречается достаточно часто (1:500–1:1000 живорожденных). Почечная артерия отсутствует, но надпочечник сохранен, а у новорожденных может быть гипертрофирован. Увеличенный надпочечник иногда ошибочно принимают за почку. Ипсилатеральный мочеточник и соответствующая сторона Льетодиева треугольника отсутствуют. Единственная противоположная почка развивается нормально, компенсаторно гипертрофируется. Ребенок растет и развивается нормально, хотя возможны сопутствующие аномалии половых органов. Односторонняя агенезия почки выявляется, как правило, случайно. Однако заболевание единственной почки (рефлюкс, пиелонефрит, нефрит, травма, камни) крайне опасно. Следует отметить, что камни в единственной почке формируются чаще, чем у детей с обеими почками. Односторонняя агенезия хорошо выявляется при всех вариантах радиологических исследований. В случае левосторонней агенезии селезеночный изгиб толстой кишки занимает почечное ложе.
Гипоплазия почки – частое состояние, протекающее с уменьшением размеров почки.
Простая гипоплазия – врожденное уменьшение почки без признаков дисплазии (данное утверждение не разделяется многими авторами). Число долек почки уменьшено, что, по данным радиологических исследований, проявляется уменьшением числа чашечек. Гипопластичная почка может быть эктопичной или мальротированной и предрасположена к рецидивирующей инфекции.
Сегментарная гипоплазия – частичная односторонняя гипоплазия почки. Ее сочетание с артериальной гипертензией известно как синдром Аска – Упмарка. Почка уменьшена в размерах, основная почечная артерия сужена, число чашечек уменьшено. На контуре почки видно втяжение, паренхима в этом месте истончена, от лоханки вглубь почки по направлению к поверхностному втяжению тянется отросток. Отличить на основании данных радиологических исследований частичную гипоплазию почки от пиелонефритического рубцевания невозможно.
Олигонефроническая гипоплазия – редкая форма двухсторонней гипоплазии с очень маленькими почками с одной-двумя чашечками. Число нефронов резко уменьшено, они расширены и гипертрофированы. В ранней фазе почечной недостаточности, по данным экскреторной урографии, визуализируется неразвитая собирательная система.
Дисплазия почек характеризуется дезорганизацией паренхимы с нарушением развития и незрелостью нефронов и канальцев. Гистологическая картина нормальна для плода, но атипична для зрелого новорожденного. Дисплазия может поражать всю почку или ее часть. Дисплазия почки неизменно сочетается с аномалиями мочеточника или нижних мочевыводящих путей. Радиологические исследования позволяют не только различить гипоплазию и дисплазию, но и выявить сопутствующие пороки.
Эктопия почки – атипичное положение почки без ее смещения на противоположную сторону или слияния с другой почкой. Эктопия почки может сочетаться с полиренией (дополнительными почками). Последнее является частью так называемого реномаммарного синдрома: почки располагаются по маммарной (среднеключичной) линии. Гипертелоризм сосков сочетается с латерально расположенными почками, дополнительные соски – с дополнительными почками. При эктопии почка крайне редко смещается вверх, в грудную полость. Обычно при эктопии она располагается в поясничной области, подвздошной, в тазу, пресакральном пространстве. Длина мочеточника соответствует расстоянию от фактического положения почки до мочевого пузыря. Это кардинальное отличие от птоза почки, когда длина мочеточника соответствует расстоянию от гипотетического поясничного положения почки до мочевого пузыря. Поперечная эктопия – расположение почки на противоположной стороне брюшной полости. Такая почка располагается ниже аутохтонной, обычно они сливаются, образуя подковообразную почку, L-образную и т.д.
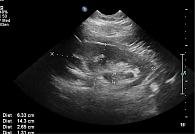
Врожденный мегакаликоз – необструктивное расширение чашечек, сочетающееся с гипоплазией пирамидок. Последнее является радиологическим отличием врожденного мегакаликоза от обструктивного гидронефроза. Пирамидки хорошо дифференцируются, кортико-медуллярная граница визуализируется, толщина коры почки не изменена. Мозговой слой почки несколько истончен. Сосочки пирамидок плоские. Почки больше возрастных размеров, сохраняется плодная дольчатость. Число чашечек увеличено, чашечки полигональны. По данным экскреторной урографии, нефрографическая фаза выражена, но мочеточники и мочевой пузырь контрастируются позже, так как контраст задерживается в расширенных чашечках. Врожденный мегакаликоз относительно благоприятное состояние, функции почек не нарушаются, может отмечаться некоторое ограничение их концентрационной способности, склонность к уролитиазу или гематурии. В отсутствие инфекции, мочекаменной болезни, гематурии лечения не требуется. Картина глубокого расщепления чашечно-лоханочной системы представлена на рис. 1, тотальной гидронефротической трансформации почки – на рис. 2.
Кистозная болезнь почек часто сочетается с кистами других органов. Существует несколько классификаций кистозной болезни:
- поликистоз почек и печени детского типа (тип I по Поттеру, а/р): новорожденных, инфантильный, ювенильный (эктазия почечных канальцев с гепатофиброзом);
- поликистоз почек и печени взрослого типа (тип III по Поттеру, а/д);
- мультикистозная дисплазия почек (тип II по Поттеру);
- фокальная и сегментарная дисплазия;
- кистозная дисплазия в сочетании с обструкцией нижних мочевыводящих путей (тип IV по Поттеру);
- кортикальные кисты (простые кисты, мультилокулярные кисты, гломерулокистоз);
- синдромы, ассоциированные с кистозной болезнью (синдромы Цельвегера, Конради, Меккеля, Тернера, туберозный склероз, болезнь Гиппеля – Линдау, многие трисомии);
- тубулярная эктазия;
- ювенильный нефронофтиз;
- солитарные кисты;
- парапельвикальные кисты;
- псевдокисты (посттравматические, туберкулезные, неопластические, эхинококковые).
Приобретенные состояния
Этот термин достаточно условный. Его применяют, когда речь идет о патологии почек. Даже в явно приобретенных состояниях (пиелонефрит, постстрептококковый нефрит) велика роль генетической составляющей.
Острый пиелонефрит у детей, особенно младшего возраста, может протекать с неспецифическими симптомами (лихорадка, общее недомогание, боль в животе). Детей с пиелонефритом обычно обследуют после купирования воспаления. Если радиологическое исследование направлено на исключение абсцесса, методом выбора является УЗИ. На ранних этапах острого пиелонефрита регистрируются увеличение размеров почки и снижение ее эхогенности. У некоторых детей повышается эхогенность и стираются границы между корковым и мозговым веществом почки. Экскреторная урограмма при первичном пиелонефрите не изменена. Функция почек достоверно выявляется при использовании радионуклидных методик. При хроническом пиелонефрите определяются повышение плотности почек, истончение паренхимы, наличие втяжений. Абсцесс почки и перинефральный абсцесс хорошо выявляются эхографически. Неконтрастная допплерография позволяет с высокой степенью достоверности оценить состояние сосудов почки при острых и хронических процессах [5].
При нефротическом синдроме почка существенно увеличивается в размерах, приобретает округлую форму.
Нефрокальциноз нечасто встречается у детей, определяется как отложение кальция в паренхиме почек. Депозиты кальция находят в канальцах, эпителии канальцев или в интерстициальной ткани. Причин развития нефрокальциноза несколько [6]:
- идиопатические;
- гиперкальциурия, гиперкальциемия (аминоацидурия, синдром Бартера, гиперпаратиреоидизм, гипервитаминоз D, гиперурикемия, применение диуретиков, длительная иммобилизация, полное парентеральное питание, идиопатическая гиперкальциемия (синдром Вильямса), синдром Кушинга, оксалоз, остеопороз, несовершенный остеогенез, саркоидоз, тубулярный ацидоз, цистинурия);
- некроз коры почек;
- некроз сосочка пирамидки;
- врожденный нефрит;
- хронический пиелонефрит;
- туберкулез;
- губчатая почка;
- отравление тяжелыми металлами;
- проживание в высокогорье;
- опухоль Вильмса.
Одна из самых частых причин нефрокальциноза – длительная терапия мочегонными средствами на фоне бронхолегочной дисплазии или врожденных пороков сердца. На обзорной рентгенограмме кальцинаты визуализируются как вкрапления, часто сгруппированные, обычно двухсторонние, в паренхиме почки. УЗИ значительно более чувствительно в диагностике нефрокальциноза. Нефрокальциноз нередко сочетается с уролитиазом.
Уролитиаз – отложение кальция в собирательной системе почки и дистальных отделах мочевыводящего тракта. В современных условиях самой частой причиной уролитиаза является хроническая инфекция, вызванная бактериями рода Proteus. Другими причинами являются хронические воспалительные заболевания толстого кишечника и метаболические нарушения. УЗИ недостаточно информативно для выявления кальцинатов в мочеточнике, поэтому предпочтение отдают экскреторной урографии.
Нефробластома, опухоль Вильмса – эмбриональная опухоль, состоящая из эпителиальных, бластных и стромальных элементов. Часто (75%) встречается у детей в возрасте от года до пяти лет. На ее долю в структуре опухолей почек в этом возрасте приходится 97%. В подавляющем большинстве случаев неоплазма обнаруживается спорадически, но в 1% случаев носит семейный характер. В 5% случаев опухоль поражает обе почки, а у 15% больных сочетается с хромосомной патологией, церебральным гигантизмом, гемигипертрофией, спорадической несемейной аниридией, синдромом Видемана – Беквита, гамартомами, нейрофиброматозом и другими аномалиями. Опухоль длительное время растет бессимптомно, хотя описаны случаи острой манифестации опухоли после минимальных травм.
При экскреторной урографии у детей с нефробластомой отмечаются нарушение формы, размеров и расположения почек, изменение чашечно-лоханочной системы и мочеточников. Исключение составляет так называемая «немая почка». Феномен свидетельствует либо о поражении средних сегментов почки со сдавлением мочеточника или почечной вены, либо о прорастании сосудистой ножки внеорганной забрюшинной нейробластомой. Эти случаи снижают значимость экскреторной урографии в дифференциальной диагностике нефробластомы.
УЗИ и КТ позволяют более точно определить анатомо-топографические и в какой-то степени морфологические характеристики нефробластомы [7]. Опухоль выглядит как солитарная масса преимущественно неправильной формы (95,2%) с преобладанием гиподенситивных очагов. Кальцинаты обнаруживаются редко. В области опухолевого узла контур почки выпуклый, нередко выявляется экзофитная зона с фрагментарно выраженной капсулой. При внутривенном контрастном усилении во всех случаях негомогенность усиливается. Фокальные участки пониженной плотности ограничиваются более резко выраженной линией демаркации, отделяющей опухоль от нормальной резидуальной почечной ткани. Бугристость контуров почки свидетельствует о выходе опухоли за пределы органа. Но четкость контуров говорит в пользу сохранности капсулы, что в отсутствие метастазов указывает на вторую стадию заболевания. Третья и четвертая стадии опухолевого процесса проявляются нечеткостью контуров почки, бугристостью, то есть прорастанием собственной капсулы. Наряду с этим возможны инфильтрация околопочечной клетчатки в виде ее уплотнения, прорастание в прилежащие органы (надпочечники, поджелудочную железу, селезенку, печень, диафрагму, стенку кишки). Редко поражается нижняя полая вена (прорастание и метастатический тромбоз), что клинически проявляется выраженной гематурией и отеками ног.
Наиболее часто при нефробластоме поражаются регионарные лимфатические узлы. Точность экскреторной урографии в диагностике нефробластомы составляет 79,6%, что уступает точности УЗИ (89,9%), КТ (91,9%) и тем более ангиографии (97,6%). Экскреторная рентгенография наряду с УЗИ может использоваться как скрининг-метод [8].
Травма почки – самое частое последствие тупой травмы живота. Выделяют минимальную травму почки (контузия почки без разрыва капсулы или повреждения чашечно-лоханочной системы, 25% всех травм почки), большую травму (нарушение капсулы или нарушение чашечно-лоханочной системы, 50% всех травм почки), критическую травму (фрагментация почки, отрыв почки от сосудистой ножки или тромбоз сосудов, 25% травм почки). Результаты обзорной рентгенограммы неспецифичны. Могут обнаруживаться стушеванность тени m. Ileopsoas, переломы костей таза и другие сопутствующие травмы. Эхография более информативна, регистрируются нарушение архитектоники почки, жидкость в брюшной полости. Разрыв почки выглядит как неправильный дефект низкой эхогенности. Эхогенность свежей гематомы может быть ниже эхогенности паренхимы почки. Подкапсулярные гематомы, лентовидные или овальные, изменяют контур почки.
Заключение
Радиологические исследования почек требуют оптимального выбора методик, нередко их комплексного использования, а также участия клинициста и радиолога-диагноста.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Финансирование. Гранты, благодарности – неприменимо.
A.Zh. Dosimov, PhD, G.V. Tereshchenko, PhD, V.M. Delyagin, PhD, Prof., I.A. Ismailova
Dmitry Rogachev National Medical Research Center of Pediatric Hematology, Oncology and Immunology
Marat Ospanov West Kazakhstan Medical University
Contact person: Vasily M. Delyagin, delyagin-doktor@yandex.ru
A critical review of the capabilities of various methods of visualizing the kidneys in children of different ages with various pathologies is presented. Comparison of methods and discussion of their diagnostic significance allows us to formulate proposals for organizing the examination.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.