Неалкогольная жировая болезнь печени и сахарный диабет 2 типа в практике врача-эндокринолога
- Аннотация
- Статья
- Ссылки
- English
Подход к лечению включает диетотерапию и физические нагрузки, изменение поведения и фармакотерапию с учетом как этиопатогенетических факторов, так и фоновых заболеваний. Фармакотерапия НАЖБП должна быть направлена на коррекцию инсулинорезистентности, улучшение функции печени и снижение риска развития ассоциированных заболеваний.
Для уменьшения выраженности стеатоза при НАЖБП необходимо снизить массу тела не менее чем на 5% от первоначальной. Диетические рекомендации должны быть направлены на уменьшение калорийности пищи. В то же время на фоне низкокалорийной диеты с существенным ограничением жиров значительно возрастает риск образования желчных камней. Для профилактики желчнокаменной болезни можно рекомендовать препараты урсодезоксихолевой кислоты (Урсофальк).
Результаты исследований продемонстрировали, что у пациентов с НАЖБП прием урсодезоксихолевой кислоты способствует уменьшению выраженности стеатоза, липотоксичности и, по некоторым данным, фиброза печени.
Многосторонний подход к ведению пациентов с НАЖБП и СД 2 типа с применением урсодезоксихолевой кислоты может быть рекомендован при всех формах НАЖБП.
Эффективной мерой предупреждения развития НАЖБП и СД 2 типа является коррекция массы тела на фоне модификации образа жизни.
Подход к лечению включает диетотерапию и физические нагрузки, изменение поведения и фармакотерапию с учетом как этиопатогенетических факторов, так и фоновых заболеваний. Фармакотерапия НАЖБП должна быть направлена на коррекцию инсулинорезистентности, улучшение функции печени и снижение риска развития ассоциированных заболеваний.
Для уменьшения выраженности стеатоза при НАЖБП необходимо снизить массу тела не менее чем на 5% от первоначальной. Диетические рекомендации должны быть направлены на уменьшение калорийности пищи. В то же время на фоне низкокалорийной диеты с существенным ограничением жиров значительно возрастает риск образования желчных камней. Для профилактики желчнокаменной болезни можно рекомендовать препараты урсодезоксихолевой кислоты (Урсофальк).
Результаты исследований продемонстрировали, что у пациентов с НАЖБП прием урсодезоксихолевой кислоты способствует уменьшению выраженности стеатоза, липотоксичности и, по некоторым данным, фиброза печени.
Многосторонний подход к ведению пациентов с НАЖБП и СД 2 типа с применением урсодезоксихолевой кислоты может быть рекомендован при всех формах НАЖБП.
Эффективной мерой предупреждения развития НАЖБП и СД 2 типа является коррекция массы тела на фоне модификации образа жизни.
В настоящее время получены убедительные данные о том, что сочетание неалкогольной жировой болезни печени (НАЖБП) и сахарного диабета (СД) 2 типа представляет серьезную проблему для современного здравоохранения и негативно влияет на прогноз данных заболеваний.
На современном этапе продемонстрировано, что между НАЖБП и СД 2 типа существует двунаправленная ассоциация патофизиологических, эпидемиологических и клинических характеристик [1–3].
Согласно данным общенационального регистра, на начало 2021 г. по сравнению с 2000 г. количество пациентов с СД увеличилось вдвое и составило почти 4,8 млн, более 3% населения России. Из них более 4,4 млн страдали СД 2 типа [4].
Известно, что у пациентов с СД 2 типа инсулинорезистентность (ИР), дисфункция жировой ткани и липотоксичность могут привести к развитию НАЖБП.
НАЖБП представляет собой хроническое заболевание метаболического генеза у лиц с отсутствием экзогенных факторов токсического поражения печени, обусловленное накоплением липидов в составляющих печеночную дольку клеточных элементах, морфологически доказанным стеатозом, стеатогепатитом, фиброзом, циррозом или аденокарциномой [5].
Распространенность НАЖБП при СД 2 типа составляет от 70 до 100% [5]. Стеатоз печени выявляется у подавляющего большинства больных СД. Так, по некоторым данным, частота сочетания НАЖБП с СД 2 типа у пациентов старше 50 лет достигает примерно 70% [6].
С учетом тесной связи СД 2 типа и НАЖБП некоторые эксперты полагают, что НАЖБП можно рассматривать как одно из осложнений СД [3, 7, 8].
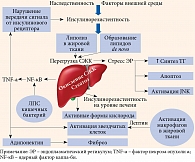
Следует отметить общие патогенетические факторы, которые лежат в основе развития НАЖБП и СД 2 типа. Так, одной из основных причин развития СД 2 типа и НАЖБП является ИР. В соответствии с одной из современных теорий, избыточное накопление свободных жирных кислот (СЖК) и триглицеридов (ТГ) при НАЖБП приводит к повреждению сигнальных путей инсулина и развитию ИР, что в свою очередь способствует постепенному нарушению секреции инсулина, а в дальнейшем – манифестации СД 2 типа [9, 10].
Нередко встречаемая при ожирении активация симпатоадреналовой системы усиливает липолиз в жировой ткани с высвобождением повышенного количества СЖК, одновременно в печени снижается скорость их окисления. Усиленный приток СЖК к печени и замедленное их окисление способствуют избыточному накоплению ТГ в гепатоцитах и секреции большего количества липопротеинов очень низкой плотности [5, 11].
Накопленные на сегодняшний день данные позволяют считать одним из основных звеньев патогенеза изменение профиля гормонов жировой ткани – регуляторов жирового обмена: адипонектина, грелина и др. [11].
Не вызывает сомнений, что немаловажную роль в патогенезе НАЖБП играют дисфункция и воспаление жировой ткани.
Последние данные свидетельствуют о том, что процессы, происходящие в тонкой кишке, также вовлечены в развитие патологического процесса [10].
Кишечная микрофлора опосредованно за счет проникновения липополисахаридов (ЛПС) грамотрицательных бактерий в портальный кровоток активирует через толл-подобный рецептор 4 неспецифический иммунный ответ, что влечет за собой развитие воспаления и активацию продукции фиброзного матрикса [11].
Опубликованные результаты ряда исследований указывают на роль наследственной предрасположенности к развитию неалкогольного стеатогепатита (НАСГ) у пациентов с НАЖБП, а также к более стремительному темпу прогрессирования фиброза печени. Продемонстрировано значение полиморфизма генов адипонутрина (PNPLA3) и белков, участвующих в обмене липидов, инсулина, оксидативного стресса (например, циклооксигеназы 2) [1, 10, 11].
Основными причинами развития НАЖБП при СД 2 типа признаны дисфункция жировой ткани, ИР и липотоксичность.
В настоящее время доказана и продемонстрирована корреляция между показателями ИР и признаками поражения печени: уровнем инсулина сыворотки крови и наличием признаков цитолиза [12].
Так, ИР клеток печени сопровождается снижением синтеза гликогена, активацией гликогенолиза и глюконеогенеза. Физиологическая реакция печени на гиперинсулинемию проявляется в снижении продукции глюкозы. В течение долгого времени ИР компенсируется нефизиологической гиперинсулинемией. Истощение данного механизма приводит к гиперпродукции глюкозы и в дальнейшем к развитию СД 2 типа [13]. Согласно данным статистики, НАЖБП диагностируют у 100% лиц с абдоминальным ожирением и метаболическим синдромом [5].
Фиброз печени развивается у 15–20% больных стеатозом и может трансформироваться в цирроз, а при более длительном течении или воздействии повреждающих факторов – в гепатоцеллюлярную карциному. В то же время признаки НАЖБП могут быть выявлены у 10–15% больных без клинических проявлений метаболического синдрома [5].
Согласно эпидемиологическим данным, НАЖБП ассоциирована с увеличенным риском развития СД 2 типа, при этом лечение НАЖБП уменьшает риск возникновения диабета. Сахарный диабет 2 типа ухудшает течение НАЖБП и удваивает риск ее прогрессирования до выраженного фиброза, цирроза и гепатоцеллюлярной карциномы. И наоборот, НАЖБП вносит вклад в метаболическую декомпенсацию СД 2 типа [1].
В ряде исследований установлено, что печень секретирует молекулы, способные воздействовать на метаболизм глюкозы при НАЖБП. Вероятно, белково-секреторная функция гепатоцитов при НАЖБП нарушается с развитием стеатоза, и продукция гепатокинов связана с развитием воспаления и ИР [14]. Гепатокины – белки, которые оказывают воздействие на метаболический процесс при помощи аутокринного, паракринного и эндокринного сигналингов [13–15]. Следовательно, данные нарушения могут приводить к манифестации СД.
Представляет интерес фетуин В как гепатокин, который обладает эндокринной функцией за пределами печени. Он неблагоприятно воздействует на чувствительность клеток к инсулину.
Материалы исследования, в котором анализировались 168 гепатокинов, 32 из которых секретировались гепатоцитами, пораженными при НАЖБП, продемонстрировали повышение уровня фетуина В у пациентов с НАЖБП и СД 2 типа [14–17]. Еще в одной работе выявлено, что гепатокин фетуин В способствовал нарушению толерантности к глюкозе и был повышен у пациентов с СД 2 типа и НАЖБП с фиброзом [14].
Следовательно, данные исследований указывают на стойкую патофизиологическую связь между CД 2 типа и НАЖБП.
Основные патогенетические звенья НАЖБП представлены на рис. 1.
Необходимо отметить, что у большинства лиц клинические проявления НАЖБП отсутствуют или слабо выражены. В реальной клинической практике к врачам обращаются пациенты с жалобами, которые обусловлены коморбидными, ассоциируемыми с НАЖБП заболеваниями, например с артериальной гипертензией, ишемической болезнью сердца, заболеваниями периферических сосудов, ожирением, СД 2 типа, фибромиалгиями, и тогда НАЖБП становится диагностической находкой [5].
Наиболее ранними критериями повреждения печени при СД 2 типа являются повышение уровней аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), щелочной фосфатазы, гамма-глутамилтрансферазы (ГГТ) в плазме крови. Отмечено, что показатели АЛТ в сыворотке крови коррелируют с ИР и снижением чувствительности к инсулину клеток печени по сравнению с концентрацией АСТ и ГГТ [18].
В российских клинических рекомендациях указано, что важным критерием диагностики НАЖБП является наличие избыточного содержания жира в печени по данным инструментальных и/или морфологических исследований [5].
Инструментальные методы исследования (компьютерная томография и ультразвуковое исследование) позволяют диагностировать гепатомегалию, косвенно оценить наличие стеатоза печени, обнаружить признаки портальной гипертензии.
В то же время неинвазивный метод на основе ультразвука (транзиентная эластография) предоставляет возможность одновременно оценивать степень стеатоза и фиброза печени, измеряющий параметр затухания и жесткость печени, коррелирующие со стадией ее фиброза [19].
На современном этапе в клиническую практику внедрено несколько диагностических панелей для определения активности фиброгенеза (FIB-4, FibroMax, NAFLD fibrosis score (Non-Alcoholic Fatty Liver Disease Fibrosis Score, NFS), ВАRD и др.). Наибольшую диагностическую точность в рандомизированных исследованиях продемонстрировала NAFLD fibrosis score [5, 11, 20].
Оценка фиброза по NFS осуществляется с применением шести показателей: возраста, индекса массы тела, глюкозы плазмы, подсчета количества тромбоцитов и соотношения АСТ/АЛТ. Параметр NFS менее -1,455 имеет 90%-ную чувствительность для исключения выраженного фиброза, более 0,675 обладает 97%-ной специфичностью для выявления выраженного фиброза [20].
Подход к лечению включает диетотерапию и физические нагрузки, изменение поведения и фармакотерапию с учетом как этиопатогенетических факторов, так и фоновых заболеваний. В случае развития НАЖБП на фоне ожирения и СД 2 типа наиболее эффективным признано постепенное снижение массы тела вследствие модификации образа жизни (гипокалорийной диеты и умеренных физических нагрузок). Пациентам с НАЖБП противопоказаны полностью вегетарианский рацион, низкоуглеводные диеты и голодание.
Для уменьшения выраженности стеатоза при НАЖБП необходимо снижение массы тела не менее чем на 5% от первоначальной. В то же время для устранения воспалительных и некротических изменений в печени при стеатогепатите требуется снизить массу тела не менее чем на 10% от исходной [5].
В реальной клинической практике нередко можно столкнуться с такой проблемой, как низкая приверженность долгосрочным диетическим рекомендациям, которые способствуют снижению массы тела. Поэтому в последнее время значительное внимание уделяется повышению переносимости диет. В рационе регулярно должны присутствовать продукты, содержащие клетчатку, что позволит достичь чувства насыщения при меньшей общей суточной калорийности пищи [21, 22].
Клинически значимое снижение массы тела, а также нормализация или устойчивость показателей углеводного обмена способствуют положительной динамике как клинических, так и лабораторных показателей, характеризуются снижением индекса гистологической активности и степени фиброза печени [5].
Фармакотерапия НАЖБП должна быть направлена на коррекцию ИР, улучшение функции печени и снижение риска развития ассоциированных заболеваний.
С учетом накопленных доказательств ведущей роли ИР в этиопатогенезе НАЖБП и СД 2 типа представляется обоснованным применение инсулиносенситайзеров – лекарственных средств, повышающих чувствительность клеток к инсулину (бигуаниды, тиазолидиндионы) [5, 10, 11].
Основной механизм действия бигуанидов (метформина) заключается в повышении чувствительности инсулинзависимых тканей к инсулину за счет активации в них киназы циклического аденозинмонофосфата и, следовательно, подавлении глюконеогенеза и увеличении утилизации глюкозы мышечной тканью. Помимо воздействия на углеводный обмен метформин способен приводить к снижению аккумуляции ТГ в печени и ассоциированного с ожирением хронического воспаления в жировой ткани [23, 24].
Тиазолидиндионы (пиоглитазон) показаны для лечения морфологически подтвержденного НАСГ. Однако эффективность и безопасность данного пиоглитазона при длительной терапии не доказаны [5, 11]. Долгосрочное применение препарата может способствовать возникновению широкого спектра побочных эффектов. Пиоглитазон снижает ИР в периферических тканях и в тканях печени, способствует уменьшению продукции глюкозы в печени [5, 11]. Применение пиоглитазона у пациентов с НАЖБП связано с целым рядом метаболических изменений, включая повышение чувствительности жировой, мышечной и печеночной тканей к инсулину, уменьшение уровня ТГ, повышение экспрессии транспортеров глюкозы [25].
Метаанализ результатов четырех исследований в отношении пациентов с НАЖБП и предиабетом/СД 2 типа, опубликованный J. Lian и соавт. в 2021 г., продемонстрировал, что применение пиоглитазона способствовало значимому регрессу стеатоза печени и степени воспаления, однако не оказывало достоверного влияния на фиброз [26].
Следует подчеркнуть, что препараты из группы инсулиносенситайзеров не рекомендуется назначать в отсутствие установленных нарушений углеводного обмена (предиабета и СД) [27].
В то же время известно, что витамин Е (токоферол) в дозе 800 мг/сут оказывает положительное влияние на цитолиз, стеатоз и воспаление. Назначение витамина Е (токоферола) обоснованно при сочетании НАЖБП и СД, при НАЖБП без НАСГ и фиброза, при подозрении на НАСГ, но без гистологического подтверждения, а также при исходе НАЖБП в цирроз печени [5].
Важно также отметить роль агонистов рецепторов глюкагоноподобного пептида 1 (арГПП-1). Агонисты рецепторов ГПП-1 в первую очередь применяются у больных СД 2 типа с избыточной массой тела и ожирением в качестве сахароснижающей терапии. Установлено, что арГПП-1 задерживают опорожнение желудка, что ускоряет возникновение чувства насыщения и снижает постпрандиальные колебания глюкозы плазмы [28]. В исследованиях продемонстрирована эффективность арГПП-1 у пациентов с НАЖБП как с СД 2 типа, так и без СД в уменьшении массы тела, а также содержания жира в печени и активности печеночных трансаминаз, печеночной плотности [12, 28, 29].
Заслуживают внимания данные и об ингибиторах натрий-глюкозного котранспортера 2 (ипраглифлозине). Так, у пациентов с СД 2 типа на фоне их приема уменьшались значения индекса стеатоза печени [30, 31].
Параллельно с представленной ранее базисной терапией рекомендуется проводить коррекцию дисбиотических изменений.
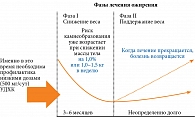
При применении низкокалорийной диеты с существенным ограничением жиров значительно возрастает риск образования желчных камней. Так, при снижении веса на 1,0–1,5 кг/нед повышается риск развития желчнокаменной болезни (рис. 2).
Для профилактики желчнокаменной болезни возможно применение препаратов урсодезоксихолевой кислоты (УДХК).
Результаты клинических и экспериментальных исследований продемонстрировали различные эффекты УДХК: гепатопротективный, антиоксидантный, цитопротективный, антифибротический, апоптознормализующий. Препараты УДХК способны оптимизировать углеводный и липидный обмен [32–35].
Данные метаанализов, представленные A. Sánchez-García и соавт. (2018 г.) и L. Simental-Mendía и соавт. (2019 г.), свидетельствуют, что использование УДХК значимо способствовало нормализации показателей углеводного обмена (глюкозы плазмы, гликированного гемоглобина (HbA1c) и инсулина) и снижению общего холестерина [35, 36]. Показан эффект УДХК, применяемой в разных дозах от шести недель до двух лет, на гликемические параметры.
Метаанализ результатов семи исследований с применением восьми групп лечения УДХК продемонстрировал значительное снижение уровня глюкозы плазмы натощак – -3,30 ммоль/л при 95%-ном доверительном интервале (ДИ) -6,36– -0,24 (р = 0,034; I2 = 28,95%).
Метаанализ результатов двух групп лечения показал значительное уменьшение концентрации HbA1c – -0,41% (95% ДИ -0,81– -0,01; р = 0,042; I2 = 0%). Метаанализ данных четырех групп лечения продемонстрировал существенное снижение уровня инсулина в плазме – средневзвешенная разница -1,50 мг/дл (95% ДИ -2,81– -0,19; р = 0,025; I2 = 67,90%). Установлено, что УДХК значительно снижала концентрацию глюкозы плазмы натощак, HbA1c и инсулина, что свидетельствовало о ее положительном влиянии на гомеостаз глюкозы [35].
Доказано, что желчные кислоты, включая УДХК, служат сигнальными молекулами с системными эндокринными функциями. Они регулируют собственную энтерогепатическую циркуляцию, а также гомеостаз глюкозы, ТГ и энергии [1].
В нескольких исследованиях показано уменьшение ИР под влиянием УДХК [36].
В других исследованиях продемонстрировано, что у пациентов с НАЖБП прием УДХК способствовал уменьшению выраженности стеатоза, эффектов липотоксичности и, по некоторым данным, фиброза печени.
УДКХ способствуют нормализации обмена липидов, уменьшению ИР, что в свою очередь направлено на снижение толщины комплекса «интима – медиа» [1, 37, 38].
Получены данные о возможности УДХК влиять на метаболизм желчных кислот и уровень липидов у людей [38].
Представляют интерес данные, подтверждающие способность УДХК улучшать чувствительность клеток к инсулину, связанную со стеатозом печени у мышей, находившихся на рационе с высоким содержанием жира [39].
В другой экспериментальной работе, в которой проводилось скармливание УДКХ мышам, страдавшим ожирением, анализировали уровни желчных кислот в сыворотке, печени, эпидермисе и бурой жировой ткани [40]. Прием УДКХ сопровождался достоверным ростом ее конъюгатов (тауроурсодезоксихолевой кислоты и др.) и полиненасыщенных жирных кислот, снижением концентрации свободных жирных кислот [40].
Еще в одном исследовании установлено, что комбинация УДХК и ситаглиптина обусловливает более выраженное снижение уровня HbA1c, чем монотерапия УДХК или ситаглиптином. В исследование были включены пациенты с СД 2 типа (уровень HbA1c ≥ 7,0%) и хронической болезнью печени (НАЖБП). Первой группе исходно была назначена только УДХК в дозе 900 мг в течение 12 недель с последующим включением в терапию ситаглиптина в дозе 50 мг на 12 недель. Вторая группа сначала получала монотерапию ситаглиптином в дозе 50 мг в течение 12 недель, после чего к терапии была добавлена УДХК в дозе 900 мг на срок 12 недель. Первоначальные характеристики исследуемых групп были сходными. Снижение уровня HbA1c с 7,0 ± 0,3 до 6,4 ± 0,5% (р = 0,01) выявлено в первой группе. Данный показатель уменьшился еще больше после добавления ситаглиптина – с 6,4 ± 0,5 до 6,0 ± 0,4% (р < 0,01). Таким образом, применение УДХК в виде монотерапии уже приводило к статистически достоверному снижению уровня HbA1c в среднем на 0,6%. Их комбинация способствовала более выраженному снижению показателя [41].
Согласно современным руководствам, УДХК может быть рекомендована при всех формах НАЖБП, в том числе на стадии НАСГ и в сочетании с другими диффузными заболеваниями печени [5]. Эффективность УДХК доказана в лечении НАЖБП, в частности НАСГ [5]. Выявлено, что прием УДХК в дозе 15–30 мг/кг массы тела ежедневно в течение 24–48 недель приводил к достоверному снижению активности печеночных трансаминаз [42].
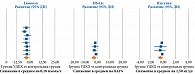
Безопасность применения УДХК у пациентов с СД 2 типа, а также тенденция к снижению уровня HbA1c на 0,5% вследствие лечения НАСГ были продемонстрированы при проведении метаанализа (рис. 3) [41].
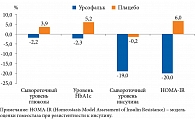
Дополнительные эффекты высоких доз (25–30 мг/кг) УДХК при НАСГ выявлены в другой работе. В частности, показано улучшение показателей углеводного обмена при нарушении толерантности к глюкозе и СД 2 типа (рис. 4) [43].
На фармацевтическом рынке представлено достаточное количество препаратов УДХК. Референтным препаратом УДХК в странах Европы (EU Harmonised Birth Dates, related Data Lock Points, allocated P-RMSs, 2009), а также в России является Урсофальк.
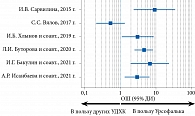
Преимущество Урсофалька перед другими препаратами УДХК, представленными в Российской Федерации, в отношении эффективности продемонстрировано в недавнем метаанализе, проведенном Ю.А. Кучерявым и соавт. (2022 г.). Ученые оценили динамику растворения билиарного сладжа в различных исследованиях (рис. 5).
Так, при применении референтного для РФ препарата Урсофальк обобщенная частота растворения билиарного сладжа в течение трех месяцев терапии составила 64,826% (95% ДИ 49,242–78,941), тогда как при использовании других препаратов УДХК – 39,187% (95% ДИ 17,520–63,390). Урсофальк оказался эффективнее других препаратов УДХК (отношение шансов (ОШ) 3,183 (95% ДИ 1,495–6,777)) [44]. Аналогичная тенденция сохранялась при оценке эффективности шестимесячного курса терапии (ОШ 4,614 (95% ДИ 2,881–7,388)). Так, обобщенная частота растворения билиарного сладжа в группах Урсофалька составила 88,381% (95% ДИ 80,890–94,198), в группах других препаратов УДХК – 65,978% (95% ДИ 60,125–71,491).
Урсофальк выпускается в двух формах: капсулы по 250 мг и таблетки по 500 мг. При назначении высоких доз удобнее применять таблетки по 500 мг.
Для профилактики образования желчных конкрементов Урсофальк назначают в дозе 8–10 мг/кг/сут (вся доза однократно на ночь) в течение одного – трех месяцев.
При неалкогольном стеатогепатите УДХК (Урсофальк) применяется в дозе 10–15 мг/кг/сут в два-три приема. Длительность терапии составляет 6–12 месяцев и более.
В заключение необходимо отметить, что, поскольку связующим патогенетическим звеном СД 2 типа и НАЖБП является ИР, коморбидность диктует многофакторный подход к лечению пациентов с данными патологиями.
Прием УДХК может быть рекомендован при всех формах НАЖБП, особенно с признаками вне- и внутрипеченочного холестаза, сердечно-сосудистой патологии, признаках НАСГ [45].
Эффективными мерами предупреждения развития НАЖБП и СД 2 типа являются коррекция массы тела, изменение пищевого поведения, физическая активность.
N.A. Petunina, Corresponding member of the RASci., MD, PhD, Prof., M.E. Telnova, PhD, E.V. Goncharova, PhD, N.S. Martirosyan, PhD, I.A. Kuzina, A.O. Shchetinina, PhD
I.M. Sechenov First Moscow State Medical University
Contact person: Milena Е. Теlnova, milena.telnova@mail.ru
At present, convincing data have been obtained that demonstrate that the combination of non-alcoholic fatty liver disease (NAFLD) and type 2 diabetes mellitus (DM) poses a serious problem for modern healthcare and negatively affects the prognosis of these diseases. The prevalence of NAFLD in type 2 diabetes is from 70 to 100%. Liver steatosis is detected in the vast majority of people with diabetes. The main causes of the development of NAFLD in type 2 diabetes are adipose tissue dysfunction, insulin resistance and lipotoxicity.
The approach to treatment includes diet therapy and physical activity, behavior change and pharmacotherapy, taking into account both etiopathogenetic factors and background diseases. Pharmacotherapy of NAFLD should be aimed at correcting insulin resistance, improving liver function and reducing the risk of associated diseases.
To reduce the severity of steatosis in NAFLD, it is necessary to reduce body weight by at least 5% of the original. Dietary recommendations should be aimed at reducing the calorie content of food. At the same time, against the background of the low-calorie diet with the significant restriction of fats, the risk of gallstones formation increases significantly. For the prevention of cholelithiasis, ursodeoxycholic acid (Ursofalk) preparations can be recommended.
The results of the studies have demonstrated that in patients with NAFLD, taking ursodeoxycholic acid helps to reduce the severity of steatosis, lipotoxicity and, according to some data, liver fibrosis.
A multi-pronged approach to the management of patients with NAFLD and type 2 diabetes with the use of ursodeoxycholic acid can be recommended for all forms of NAFLD.
An effective measure to prevent the development of NAFLD and type 2 diabetes is the correction of body weight against the background of lifestyle modification.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.