Отечно-асцитический синдром: практический алгоритм
- Аннотация
- Статья
- Ссылки
- English






1. Общие положения
Каждый пункт рекомендаций базируется на данных рандомизированных клинических исследований и имеет соответствующий уровень доказательности (табл. 1–3).
Отметим, что при определении степени рекомендации нет прямой связи между уровнем доказательности данных и степенью рекомендации. Например, отсутствие доказательств высокого уровня не исключает возможность дать рекомендации уровня А, если имеется богатый клинический опыт и достигнут консенсус. При определении степени рекомендаций качество научных доказательств, лежащих в их основе, является важным фактором, но его необходимо соотнести с преимуществами и недостатками, полезностью и стоимостью.
Данные рекомендации разработаны для применения у взрослых пациентов (старше 18 лет), у которых развитие отечно-асцитического синдрома связано с циррозом печени.
1.1. Определение асцита
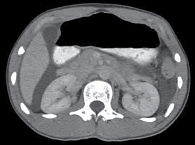
Асцит – патологическое скопление жидкости в брюшной полости (рис. 1).
Самая распространенная причина развития асцита – цирроз печени (81% случаев) [3], далее следуют онкологические заболевания, затем смешанные причины, как правило цирроз печени с трансформацией в гепатоцеллюлярную карциному (ГЦК). Такие причины асцита, как сердечная недостаточность, туберкулез, заболевания поджелудочной железы, не превышают по частоте встречаемости 5% (рис. 2).
1.2. Классификация причин асцита по системам и органам
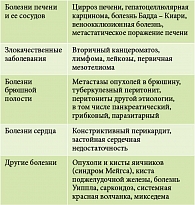
Если асцит рассматривать в отношении конкретных органов, доминировать будут печень и ее сосуды – до 90% всех причин развития асцита (табл. 4).
Как видно из представленных данных, несмотря на то что подавляющее большинство случаев асцита развивается на фоне патологии печени, существует ряд заболеваний, требующих дифференциальной диагностики.
1.3. Медико-социальная значимость асцита
Вопрос развития отечно-асцитического синдрома стоит остро. Дело в том, что данное осложнение цирроза печени развивается у 60% пациентов в течение десяти лет с момента выявления компенсированного цирроза печени [4, 5] и является маркером неблагоприятного исхода: в течение первого года от момента появления асцита доля летального исхода составляет 40%, пятилетняя выживаемость не превышает 50% [1, 5, 6].
1.4. Клиническая классификация асцита
В практическом применении наиболее удобна классификация, разработанная в 2003 г. IAC (International Ascitic Club). В ней учтены выраженность асцита и терапевтические мероприятия в зависимости от его степени (табл. 5).
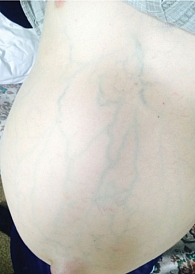
Так, асцит 1-й степени визуально не диагностируется. К способам его определения можно отнести сонографические и/или лучевые методы исследования. Такой асцит не требует назначения терапии. Асцит 2-й степени может быть определен методами перкуссии и, как правило, сопровождается явлениями флуктуации. Терапевтическая тактика при данном варианте асцита включает ограничение потребления соли с пищей, назначение адекватной диуретической терапии. Асцит 3-й степени обычно характеризуется наличием напряженной передней брюшной стенки (рис. 3), требует проведения объемных парацентезов, ограничения потребления соли с пищей, назначения адекватной диуретической терапии.
2. Методы диагностики асцита
Основными жалобами пациентов с циррозом печени при наличии асцита являются увеличение живота в объеме, увеличение веса, отеки ног и т.п. При физикальном осмотре можно верифицировать наличие асцита перкуторным методом, в положении лежа и стоя.
Инструментальными методами, подтверждающими наличие асцита, могут служить ультразвуковое исследование, магнитно-резонансная и компьютерная томография.
Основными специфическими методами диагностики пациентов с асцитом считаются проведение диагностического парацентеза с анализом асцитической жидкости, сопоставление лабораторных результатов диагностики асцитической жидкости и сыворотки.
2.1. Диагностический парацентез: общие положения
(А1) Диагностический парацентез должен быть проведен всем больным:
-
при впервые выявленном асците;
-
при асците 2–3-й степени;
-
при наличии признаков ухудшения общего состояния больного и/или осложнений цирроза печени.
2.2. Диагностический парацентез: частные вопросы
Осложнения при циррозе печени, требующие проведения диагностического парацентеза:
-
прогрессирование печеночной энцефалопатии (ПЭ);
-
наличие признаков кровотечения из варикозно расширенных вен (пищевода, желудка, прямой кишки);
-
признаки системной воспалительной реакции (лихорадка, озноб, лейкоцитоз, сдвиг лейкоцитарной формулы влево, повышение уровня С-реактивного белка, увеличение скорости оседания эритроцитов, положительный результат прокальцитонинового теста, положительный рост культуры сыворотки);
-
признаки развития гепаторенального синдрома (ГРС).
2.3. Диагностика спонтанного бактериального перитонита
(А1) При проведении диагностического парацентеза должна быть осуществлена диагностика на предмет исключения спонтанного бактериального перитонита (СБП). СБП устанавливается при наличии следующих критериев:
-
абсолютное число нейтрофильных лейкоцитов > 250/мм3;
-
определение положительного роста культуры при посеве асцитической жидкости;
-
снижение уровня белка в асцитической жидкости < 15 г/л.
По результатам исследования выделяют несколько вариантов асцита:
-
I – классический культуропозитивный нейтрофильный вариант СБП;
-
II – культуронегативный нейтрофильный асцит;
-
III – культуропозитивный низконейтрофильный.
Специалисты обсуждают наличие еще одного варианта СБП – культуронегативного низконейтрофильного. Такой вариант можно рассматривать как предстадию СБП.
2.4. Дифференциальная диагностика асцита
(А2) Проведение дифференциальной диагностики асцита включает определение:
-
цвета асцитической жидкости (желтый, красный, молочный, темно-коричневый);
-
наличия атипичных клеток (в 55% случаев встречаются при ГЦК, в 22% – при метастатическом поражении печени);
-
сывороточно-асцитического градиента (исследование альбумина сыворотки/альбумина асцита; значение показателя ≥ 1,1 является подтверждением связи асцита с портальной гипертензией, чувствительность метода 80%);
-
глюкозы (дифференциальная диагностика с перфорацией полого органа, онкопатологией);
-
амилазы (асцитически/сывороточный градиент > 0,4 свидетельствует в пользу панкреатического генеза асцита, наличия перфорации полого органа);
-
билирубина (дифференциальная диагностика с перфорацией билиарного тракта);
-
триглицеридов (травма лимфатического протока);
-
лактатдегидрогеназы (дифференциальная диагностика с воспалительным процессом в брюшной полости, онкопатологией).
3. Лечение пациентов с циррозом печени при наличии асцита
3.1. (В1) Наличие асцита 2–3-й степени требует обсуждения хирургической тактики
Все пациенты с асцитом 2–3-й степени рассматриваются для проведения трансъюгулярного шунтирования (transjugular intrahepatic portosystemic shunt – TIPS) как метода хирургического симптоматического лечения. Донорская или ортотопическая трансплантация – радикальный метод лечения пациентов данной категории. Поскольку асцит резко ухудшает прогноз, следует объективно оценивать состояние больного и предпринимаемые консервативные методы лечения. При неэффективности терапии пациент должен получать лечение в условиях палаты/отделения интенсивной терапии, а также быть поставлен в лист ожидания трансплантации печени.
3.2. (В1) Ограничение потребления соли
У пациентов с циррозом печени, осложненным асцитом, ограничивают потребление соли до 6,9 г/сут. Данное количество рассматривается в качестве эквивалента неупотребления соли как нутритивного компонента.
3.3. Терапия, которая должна быть назначена пациенту с циррозом печени, осложненным асцитом
3.3.1. Адекватная диуретическая терапия
При подборе схемы диуретической терапии должны быть учтены степень асцита, наличие признаков диуретико-ассоциированных осложнений.
3.3.2. Адекватная антибиотикотерапия
Профилактически антибиотики должны быть назначены всем пациентам с асцитом при отсутствии признаков СБП и пациентам с купированными признаками СБП. Препаратом выбора является норфлоксацин 400 мг/сут. Альтернативными препаратами считаются ципрофлоксацин 750 мг 1 раз/нед или ко-тримоксазол (сульфаметоксазол 800 мг/сут + триметоприм 160 мг/сут).
В случае подтверждения СБП эмпирическая антибиотикотерапия назначается незамедлительно. Препаратами выбора являются цефалоспорины третьего и четвертого поколения в дозе 4 г/сут с обязательным проведением повторного диагностического парацентеза через 48 часов и на пятые сутки применения антибиотиков с целью контроля эффективности антибиотикотерапии. При неэффективности применяемых препаратов антибиотик меняют в соответствии с принятыми терапевтическими канонами.
В случае низкого содержания белка в асцитической жидкости (< 15 г/л) данное состояние расценивается как фактор риска развития СБП, что требует применения норфлоксацина 400 мг/сут.
3.3.3. Нормализация кишечной флоры
Назначаются препараты лактулозы (суспензия 10–15 мл три раза в сутки) и пробиотики согласно инструкции.
3.3.4. Альбумин – основной препарат патогенетической терапии при асците
У пациентов с асцитом показано применение инфузий альбумина при снижении показателя сывороточного альбумина ниже порогового значения (< 35 г/л). Режим дозировки инфузии альбумина зависит от сопутствующих факторов и осложнений (табл. 6) [1].
3.3.5. Коррекция нутритивного статуса
Применяется комплекс препаратов нутритивной поддержки энтерально и парентерально. Основным методом коррекции нутритивного статуса является применение растворов разветвленных аминокислот в дозе 1,2 г/кг/сут и обеспечение высокой калорийности пищи – не менее 40–45 ккал/кг массы тела. Общая калорийность должна покрываться потреблением белка в дозе 1,2–1,5 г/кг/сут. Жиры и углеводы назначаются в соотношении 1:1 из доли небелковой калорийности [6–8]. Качество и правила назначения углеводов должны полностью соответствовать требованиям преимущественного усвоения белка [8, 9]. К обязательным компонентам нутритивной поддержки относятся минералы, водо- и жирорастворимые витамины, которые также рекомендованы для ежедневного применения.
При развитии энцефалопатии должна быть скорректирована калорийность пищи до 35–40 ккал/кг в расчете на идеальную массу тела (I A1) при условии сохранения соотношения жиров и углеводов 1:1. Суммарное потребление белка и применение разветвленных аминокислот должно остаться прежним (I A1).
3.3.6. Препараты для коррекции печеночной энцефалопатии
Нелеченая ПЭ является одной из основных причин смерти больных циррозом печени и причиной резкого снижения качества жизни (вплоть до утраты способности к самообслуживанию). Приобретая характер постоянного прогрессирования, ПЭ становится частой причиной многократных госпитализаций таких пациентов в течение года. Как показывает практика, развитие даже минимальной ПЭ существенно ухудшает прогноз заболевания. Именно поэтому пациенты с циррозом печени относятся к группе повышенного риска развития тяжелой энцефалопатии (2-я степень и более), что еще больше увеличивает риск летального исхода.
(II В1) В соответствии с последними рекомендациями AASLD/EASL при первоначальном лечении ПЭ целесообразно применять препараты лактулозы. Однако следует учесть, что эффективность применения сиропа per os и per rectum заявлена в небольших исследованиях, что в настоящее время широко дискутируется и подвергается критике. Основным принципом применения лактулозы считается регулярный прием сиропа per os в небольших количествах, рассчитанных индивидуально (в среднем по 25 мл два раза в сутки), до достижения мягкого стула два-три раза в сутки [10, 11].
(I B2) При развитии тяжелой ПЭ единственным препаратом выбора считается Л-орнитин-Л-аспартат (Гепа-Мерц). Основной точкой приложения данного препарата является воздействие на один из патогенетических факторов развития энцефалопатии – увеличение аммиака сыворотки. В многочисленных клинических исследованиях продемонстрированы достоверные данные снижения уровня аммиака в сыворотке при использовании препарата Л-орнитин-Л-аспартат (L-Ornithine-L-Aspartate, LOLA) по сравнению с постоянным приростом такового в группе плацебо [12–14]. На основании достоверной эффективности использования LOLA внутривенно препараты данной группы также рекомендованы к применению в последних документах AASLD/EASL (2014) [10].
В настоящее время рекомендуемая доза LOLA – 20–40 г/сут в разведении раствором NaCl 0,9% 200,0–400,0. Применяется медленно внутривенно капельно с переходом на дальнейшее использование LOLA в гранулах 6 г три раза в сутки не менее двух недель [15]. Игнорирование применения LOLA в гранулах в амбулаторном режиме для лечения минимальной энцефалопатии и после курса внутривенных инфузий обычно приводит к более тяжелому рецидиву ПЭ и частым госпитализациям [13, 14, 16, 17].
Критерием эффективности применения LOLA служит достоверное снижение уровня аммиака сыворотки, повышение качества жизни [12, 13, 15]. Кроме того, применение LOLA важно с фармакоэкономической точки зрения. Так, в группе больных, получавших LOLA, отмечено уменьшение длительности пребывания в стационаре на 40% [18].
Отметим, что симптоматическое лечение ПЭ сегодня сводится к комплексному применению препаратов лактулозы, LOLA и пробиотиков. Профилактическое лечение предполагает применение рифаксимина и лактулозы (I A1). Альтернативными препаратами (II B2) являются неомицин и метронидазол [10].
3.3.7. Сопутствующая терапия, которая должна быть отменена у пациента с циррозом печени, осложненным асцитом
В основе декомпенсации основного заболевания на фоне приема нижеперечисленных препаратов лежат три основных механизма – нефротоксичность, гепатотоксичность, дисциркуляторные нарушения. Пациентам с асцитом рекомендовано воздержаться от применения препаратов данных фармакологических групп:
-
нестероидные противовоспалительные препараты;
-
ингибиторы ангиотензинпревращающего фермента;
-
антагонисты ангиотензина II;
-
альфа-1-адреноблокаторы;
-
аминогликозиды.
3.3.8. Диуретическая терапия: правила назначения и коррекции
(В1) Цель диуретической терапии – купирование асцита на минимальной дозе диуретических препаратов.
Асцит 2-й степени, выявленный впервые
3.3.8.1. (А1) Первая линия диуретической терапии – назначение спиронолактона:
-
начальная доза – 100 мг/сут на три приема;
-
пошаговое увеличение на 100 мг один раз в неделю;
-
максимальная доза – 400 мг/сут.
3.3.8.2. (А1) Оценка эффективности включает:
-
измерение массы тела один раз в неделю;
-
контрольное исследование электролитов сыворотки.
3.3.8.3. (А1) Признаки эффективности диуретической терапии первой линии:
-
положительный диурез;
-
снижение массы тела > 2 кг в течение недели, но < 3,5 кг при наличии только асцита;
-
снижение массы тела > 2 кг в течение недели, но < 7 кг при наличии асцита и периферических отеков.
3.3.8.4. (А1) Признаки неэффективности диуретической терапии первой линии:
-
снижение массы тела < 2 кг в течение недели;
-
развитие диуретико-ассоциированного осложнения – гиперкалиемии (калий сыворотки > 6 ммоль/л).
При неэффективности первой линии терапии показано применение второй линии диуретической терапии.
3.3.8.5. (А1) Вторая линия диуретической терапии – добавление к максимальной дозе спиронолактона (400 мг/сут) препарата фуросемид:
-
начальная доза фуросемида – 40 мг утром;
-
пошаговое увеличение дозы фуросемида на 40 мг один раз в неделю;
-
максимальная доза фуросемида – 160 мг/сут.
3.3.8.6. (А1) Признаки эффективности диуретической терапии второй линии:
-
положительный диурез;
-
снижение массы тела > 2 кг в течение недели, но < 3,5 кг при наличии только асцита;
-
снижение массы тела > 2 кг в течение недели, но < 7 кг при наличии асцита и периферических отеков.
3.3.8.7. (А1) Мониторинг лабораторных показателей не реже одного раза в неделю в течение первого месяца:
-
сыворотка: клинический анализ, натрий, калий, мочевина, креатинин, билирубин общий, международное нормализованное отношение (МНО), альбумин;
-
моча: клинический анализ, определение суточной экскреции натрия, белка.
Асцит 2-й степени, выявленный повторно
3.3.8.8. (А1) Назначение комбинированной диуретической терапии – спиронолактон + фуросемид:
-
начальная доза спиронолактона 100 мг/сут на три приема + фуросемид 40 мг/сут однократно утром;
-
пошаговое увеличение спиронолактона на 100 мг и фуросемида на 40 мг один раз в неделю;
-
максимальная доза спиронолактона – 400 мг/сут и фуросемида – 160 мг/сут.
3.3.8.9. Признаки неэффективности диуретической терапии:
-
снижение массы тела < 2 кг в течение недели;
-
развитие диуретико-ассоциированных осложнений.
3.3.8.10. Признаки эффективности диуретической терапии:
-
положительный диурез;
-
снижение массы тела > 2 кг в течение недели, но < 3,5 кг при наличии только асцита;
-
снижение массы тела > 2 кг в течение недели, но < 7 кг при наличии асцита и периферических отеков.
3.3.8.11. (А1) Мониторинг лабораторных показателей не реже одного раза в неделю в течение первого месяца:
-
сыворотка: клинический анализ, натрий, калий, мочевина, креатинин, билирубин общий, МНО, альбумин;
-
моча: клинический анализ, определение суточной экскреции натрия, белка.
3.3.8.12. (А1) Первая линия терапии:
-
одноэтапный лечебный парацентез большим объемом (> 5 л) при условии показателя МНО < 1,5, тромбоцитов > 40 000/мкл;
-
обязательное условие: замещение альбумином (8 г альбумина/1 л эвакуированной асцитической жидкости);
-
доза диуретиков в день проведения одноэтапного лечебного парацентеза должна быть минимальной, в дальнейшем корректируется в зависимости от степени асцита.
Асцит 3-й степени
3.3.8.13. (В1) Цель диуретической терапии – купирование асцита на минимальной дозе диуретических препаратов.
3.3.9. Диуретическая терапия: правила отмены
-
Диуретическая терапия верошпироном должна быть прекращена при повышении калия сыворотки > 6 ммоль/л.
-
Диуретическая терапия фуросемидом должна быть прекращена при снижении калия сыворотки < 3 ммоль/л.
-
Все препараты диуретической терапии должны быть отменены:
-
при снижении сывороточного натрия < 120 ммоль/л;
-
развитии признаков ГРС;
-
прогрессировании ПЭ;
-
развитии тяжелых судорог.
3.3.10. Понятие рефрактерного асцита
По данным, опубликованным в рекомендациях EASL [1], достигнут международный консенсус в определении состояния «рефрактерный асцит». В настоящее время под термином «рефрактерный асцит» принято понимать невозможность разрешить или предотвратить ранний рецидив асцита из-за низкого ответа на предпринимаемые терапевтические меры (снижение потребления соли, назначение диуретической терапии) или в случае развития диуретико-ассоциированных осложнений на фоне приема адекватной дозы мочегонных препаратов.
Рефрактерный асцит должен отвечать нескольким критериям:
-
длительность: не менее одной недели применения комбинации максимальных доз спиронолактона (400 мг/сут) и фуросемида (160 мг/сут);
-
недостаточность ответа на диуретическую терапию: снижение массы тела < 0,8 кг за четыре дня;
-
ранний рецидив асцита: появление асцита 2–3-й степени на фоне диуретической терапии в течение четырех недель.
Диуретико-ассоциированные осложнения:
-
ГРС;
-
ПЭ;
-
гипонатриемия (снижение уровня сывороточного натрия на 10 ммоль/л от исходного показателя или абсолютное значение натрия < 125 ммоль/л);
-
гипо/гиперкалиемия (при условии снижения уровня сывороточного калия < 3 ммоль/л или повышения > 6 ммоль/л).
Заключение
Асцит – практически неминуемое осложнение при естественном течении цирроза печени. Это указывает на неблагоприятный прогноз основного заболевания. Медико-социальная значимость асцита очевидна в силу высокой вероятности летального исхода у пациентов с циррозом печени. Именно поэтому в основу разработки национального руководства по ведению больных с этим заболеванием легли принципы доказательной медицины, предусматривающие наиболее эффективные методы диагностики и лечения. В течение последних лет cтановление практических рекомендаций для врачей претерпело множество правок, и данные, приведенные в этой статье, сводят воедино принципы дифференциальной диагностики, правила назначения терапии, критерии эффективности применяемого лечения и вопросы, связанные с неэффективностью консервативных мероприятий. Учитывая существующие реалии, врачам, курирующим пациентов с декомпенсированными заболеваниями печени, видимо, следует решать вопрос о постановке больного в лист ожидания трансплантации в РФ сразу после диагностирования первого эпизода асцита.
I.G. Bakulin, A.A. Varlamicheva
Moscow Clinical Research and Practical Center of the Moscow Healthcare Department
Moscow State University of Food Production
Contact person: Igor Gennadyevich Bakulin, igbakulin@yandex.ru
The article presents summarized data of practical guidelines for general practitioners, gastroenterologists, hepatologists based on recommendations proposed by EASL (European Association for the Study of the Liver, 2010), AASLD (American Association for the Study of Liver Diseases, 2009) as well as results of large-scale clinical trials.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.