Принципы современной фармакотерапии аллергического ринита: эффективность, безопасность, надежность
- Аннотация
- Статья
- Ссылки
- English
Аллергический ринит (АР) – заболевание, которое характеризуется IgE-опосредованным воспалением слизистой оболочки полости носа под действием аллергенов и наличием ежедневно проявляющихся хотя бы двух из следующих симптомов: заложенность носа, ринорея, чихание, зуд в полости носа. АР часто сочетается с другими аллергическими заболеваниями, такими как аллергический риноконъюнктивит (РК), атопический дерматит, бронхиальная астма (БА) [1, 2]. Сочетание назальных и глазных симптомов при АР отмечают до 90% пациентов [3]. В связи с этим АР является междисциплинарной проблемой для аллергологов, оториноларингологов и офтальмологов, так как часть пациентов с глазными симптомами обращаются за помощью с проявлениями РК. В последние годы повсеместно наблюдается рост распространенности аллергических заболеваний (АЗ), в структуре которых одно из ведущих мест занимает АР. Согласно данным Европейской академии аллергологии и клинической иммунологии (EAACI), в Европе зарегистрировано около 150 млн пациентов с аллергическими заболеваниями, что составляет около 20% населения. По прогнозам ВОЗ, к 2025 г. АЗ будет поражена большая часть населения мира. Распространенность АР среди всех АЗ в разных странах мира составляет 4–32%, в России – 10–24% [4]. Чаще всего заболевание дебютирует в детском возрасте. АР часто ассоциирован с БА, которая выявляется у 15–38% пациентов с АР [5, 6]. В то же время 55–85% пациентов с БА отмечают симптомы АР [7]. Общая распространенность персистирующего АР в Европе – 22,7% [8]. Большинство пациентов, обращающихся к специалистам, страдают АР тяжелой степени. С увеличением продолжительности анамнеза АР и его тяжести увеличивается количество сопутствующих заболеваний [9]. Частота встречаемости пациентов с АР в практике ЛОР-врача составляет 15–20% от всех обращений. Гистамин, действуя на клеточные рецепторы и вызывая дилатацию сосудов и усиление проницаемости их эпителия и гиперсекрецию, приводит к выраженному отеку слизистой оболочки и блокированию соустий пазух носа и слуховой трубы. При персистирующих аллергических процессах доказано формирование хронического очага воспаления [1]. Таким образом, формируется несколько предпосылок для развития инфекционного патологического процесса в ЛОР-органах.
Как правило, пациенты с симптомами аллергического или инфекционного ринита не обращаются за медицинской помощью в первые сутки, если нет выраженного ухудшения самочувствия и лихорадки, а начинают терапию заболевания самостоятельно. Для купирования ринореи и заложенности носа чаще всего применяются деконгестанты, которые благодаря безрецептурному статусу являются легкодоступной для населения группой препаратов. Но с их применением связано большое количество осложнений в амбулаторной практике, поэтому протоколами терапии введены ограничения на их использование не более семи дней подряд [1].
В связи с высокой частотой встречаемости гистамин-зависимых назальных симптомов очевидно, что для лечения больных АР необходимы препараты с высоким профилем безопасности, при этом позволяющие быстро и эффективно купировать симптомы.
В схемах терапии АР используются разные классы медикаментов, например топические антигистаминные и глюкокортикостероидные (ГКС) средства, у каждого из них есть свои преимущества [1]. В клинической практике, как правило, на первый план выходит потребность в одновременном контроле над симптомами и скорости развития эффекта, поэтому в терапии АР используют азеластина гидрохлорид.
Азеластина гидрохлорид является эффективным антигистаминным средством второго поколения местного действия для лечения симптомов аллергического ринита. Это высокоаффинный антагонист H1-гистаминовых рецепторов со структурными и химическими отличиями (производное фталазинона), благодаря которым он выделяется среди имеющихся в настоящее время антигистаминных препаратов [10]. Кроме того, азеластина гидрохлорид обладает мембраностабилизирующими и противовоспалительными свойствами, снижая концентрацию лейкотриенов, кининов и фактора активации тромбоцитов in vitro и in vivo, а также миграцию воспалительных клеток у пациентов с АР [11]. Азеластина гидрохлорид показал гораздо более быстрое начало действия (15 минут при использовании в виде назального спрея и до трех минут при использовании в виде глазных капель) среди доступных в настоящее время препаратов для лечения АР [12]. Действие азеластина длится не менее 12 часов, что позволяет применять его один или два раза в день [13]. Азеластина гидрохлорид обладает доказанной эффективностью в лечении как аллергического, так и неаллергического ринита, а также РК.
Азеластина гидрохлорид подавляет активацию тучных клеток и высвобождение интерлейкина (IL) 6, триптазы и гистамина [14]. Он также способствует снижению количества медиаторов дегрануляции тучных клеток в назальной лаважной жидкости пациентов с АР, таких как лейкотриены, которые участвуют в поздней фазе аллергического ответа [15, 16]. Возможно, это происходит за счет снижения выработки лейкотриена (LT)B4 синтазы и LTC4, ингибирования фосфолипазы A2 и LTC4 [17]. Лейкотриены инициируют расширение сосудов, повышение их проницаемости и отек, что приводит к заложенности носа, выработке слизи и активации воспалительных клеток [18]. Концентрация субстанции Р и брадикинина, которые образуются в биологических жидкостях и тканях во время воспаления, также снижается под воздействием азеластина [19, 20]. Эти агенты связаны с симптомами АР – носовым зудом и чиханием, но могут также способствовать появлению неаллергических симптомов. Другие противовоспалительные свойства молекулы азеластина запускают ингибирование высвобождения фактора некроза опухоли альфа (TNFα) [21, 22], снижение выработки гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF), а также снижение количества ряда воспалительных цитокинов, включая IL-1β, IL-6, IL-4 и IL-8. Эти цитокины закрепляют воспалительную реакцию [23, 24]. Наконец, у пациентов с сезонным аллергическим ринитом (САР) назальный спрей, содержащий азеластин, снижает количество нейтрофилов и эозинофилов и уменьшает экспрессию молекул межклеточной адгезии-1 на поверхности эпителиальных клеток носа как в ранней, так и в поздней фазе аллергической реакции [25]. Он также уменьшает продукцию свободных радикалов человеческими эозинофилами и нейтрофилами и приток кальция, индуцированный фактором, активирующим тромбоциты, in vitro [26].
Препараты местного действия с входящими в их состав антигистаминными молекулами имеют преимущества перед системной терапией. Во-первых, при использовании назального спрея лекарство может быть доставлено непосредственно к месту аллергического воспаления. Во-вторых, более высокие концентрации антигистаминного препарата по сравнению с пероральным должны усиливать противоаллергическое и потенциальное противовоспалительное действие этого средства. В-третьих, доза 0,28 мг при интраназальном применении имеет более быстрое начало действия, чем при пероральном приеме. Преимущества топического использования молекулы азеластина (после интраназального применения системная биодоступность составляет 40%, Vd – 14,5 л/кг по сравнению с олопатадином – 57%) обусловливают меньший риск системных побочных эффектов и лекарственных взаимодействий [27].
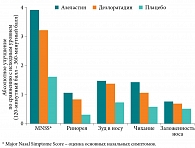
Клинические исследования, проводимые среди пациентов с АР, показали, что азеластина гидрохлорид демонстрирует более высокую эффективность и более быстрое начало действия по сравнению с пероральными антигистаминными препаратами [32, 33]. Азеластин является сильнодействующим веществом с высокой эффективностью в лечении пациентов с АР, которые не ответили на ранее проводимую терапию пероральными антигистаминными средствами [34]. Кроме того, он значительно уменьшает заложенность носа, которая является особенно тяжелым симптомом для людей, страдающих АР. В отличие от олопатадина при применении спрея, содержащего азеластин, создаются очень низкие концентрации препарата в плазме крови, что способствует снижению частоты нарушений сна у пациентов [27, 37]. В результате исследования [35] установлена более высокая эффективность азеластина в форме назального спрея по сравнению с таблетками дезлоратадина у пациентов с САР (рис. 1).
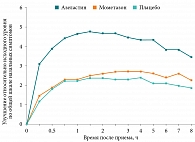
Помимо антигистаминных препаратов для лечения АР используют интраназальные глюкокортикостероиды (ИГКС), стабилизаторы мембран тучных клеток, сосудосуживающие препараты, антихолинергические препараты. Поскольку ГКС и кромоны влияют на патофизиологические аспекты АР, их расценивают как базисную терапию [1]. При сравнении эффективности назального спрея, содержащего азеластина гидрохлорид, и ИГКС мометазона фуроата было выявлено преимущество первого в снижении симптоматики САР и круглогодичного аллергического ринита (КАР). Через 15 минут после введения пациентам спрея с азеластином было продемонстрировано значительное снижение TNSS от исходного уровня на 29,5% по сравнению с 12,3% при использовании плацебо (p < 0,001) и, наоборот, ИГКС мометазона фуроат существенно не снижал TNSS по сравнению с плацебо в любой временной точке (p ≥ 0,09). Это значительное превосходство действующего вещества азеластин над плацебо сохранялось в каждой временной точке в течение восьмичасового воздействия аллергена [30] (рис. 2).
Таким образом, быстрое начало действия препарата является важным и ожидаемым элементом терапии. Комбинация азеластина и мометазона дает возможность получения положительных эффектов двух действующих веществ и оправдана для использования при ожидании определенной скорости наступления эффекта. Однако использование двух препаратов (двух флаконов) может быть затруднительным для пациентов, поэтому фиксированная комбинация азеластина гидрохлорида (140 мкг) и мометазона фуроата (50 мкг) в одном препарате значительно облегчает их использование, а также повышает эффективность лечения за счет правильного применения.
В России представлена запатентованная фиксированная комбинация мометазона и азеластина – спрей назальный дозированный Момат Рино Адванс (Др. Редди’с Лабораторис – компания, осуществляющая продвижение препарата на территории РФ), продемонстрировавший бÓльшую эффективность, чем любой из этих компонентов, используемый по отдельности, и эта комбинация может принести пользу пациентам с трудно поддающимися лечению САР и КАР. Это было подтверждено результатами нашего исследования [31] на учебных базах кафедры оториноларингологии Московского государственного медико-стоматологического университета им. А.И. Евдокимова в 2016–2017 гг. В исследовании сопоставляли результаты монотерапии пациентов топическими глюкокортикостероидами и результаты комбинированной терапии, состоящей из топических ГКС совместно с интраназальными антигистаминными препаратами.
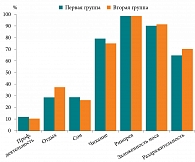
Под наблюдением было 105 пациентов с диагнозом «круглогодичный аллергический ринит». Из них 52 пациентам был назначен мометазон (первая группа), а 53 – мометазон в комбинации с азеластином (вторая группа). В обе группы входили комплаентные пациенты в возрасте от 18 до 55 лет. Группы были сопоставимы по полу, возрасту, основному диагнозу и сопутствующей патологии. Оценивалось состояние здоровья по опроснику, который пациенты заполняли на первичном и повторном визитах у врача-оториноларинголога (после курса лечения по две дозы два раза в день в течение одного месяца) в амбулаторно-поликлинических условиях. Опросник включал оценку следующих симптомов: чихания, заложенности носа, ринореи, раздражительности, профессиональной деятельности, отдыха, сна. Состояние пациентов оценивали по пятибалльной шкале, где 1 – не беспокоит, а 5 – очень сильно беспокоит. По данным опросника, в обеих группах результаты были практически сопоставимы. Все пациенты отмечали выраженную заложенность носа, чихание, ринорею, что в свою очередь приводило к раздражительности, снижению концентрации и работоспособности. Наши пациенты отмечали дискомфорт также в период свободного времяпрепровождения, во время занятий спортом, а также выраженное нарушение сна (большинство пациентов отмечали пробуждение во время сна в связи с выраженной заложенностью носа и затруднением носового дыхания) (рис. 3).
Все включенные в исследование пациенты прошли терапию до конца. Ни у кого из участников не были выявлены критерии исключения. На завершающем этапе пациенты повторно заполнили опросники для выявления оценки проведенного лечения.
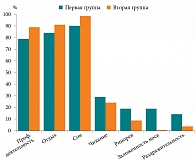
Результаты исследования выявили положительную динамику при использовании ИГКС, но все же более выраженное преимущество отмечено при лечении мометазоном в комбинации с азеластином, что выражалось в уменьшении проявления симптомов уже на четвертый день использования препарата. Повышался уровень трудоспособности (как при профессиональной деятельности, так и во время отдыха), улучшалось качество сна (пациенты отмечали, что сон не прерывался, а утром при пробуждении носовое дыхание сохранялось). Таким образом, оказывалось положительное влияние на психоэмоциональную сферу (рис. 4).
Данное исследование показало более высокую эффективность мометазона в комбинации с азеластином по всем вышеперечисленным показателям (из 53 пациентов у половины комплаентность составила более 96%, а положительная динамика состояния – у 100% участников).
Добавление к терапии интраназальным мометазоном антигистаминного препарата оправдано при среднетяжелом и тяжелом течении АР, что связано с отсроченным эффектом кортикостероида при необходимости быстрого купирования симптоматики. В РФ зарегистрирован препарат Момат Рино Адванс, представляющий собой назальный дозированный спрей, в состав которого входит фиксированная комбинация азеластина гидрохлорида 140 мкг и мометазона фуроата 50 мкг. В нем соединены представители разных классов, отличающиеся по механизму действия, которые позволяют воздействовать на разные звенья патогенеза АР и эффективно купировать симптомы заболевания, значительно ухудшающие качество жизни пациентов. Препарат показан для курсового приема, а также для использования в режиме «по требованию». Момат Рино Адванс помогает не только эффективно и быстро купировать симптомы аллергического ринита и РК, но также действует на очаг хронического аллергического воспаления.
Комбинация активных веществ дает врачу дополнительную возможность для индивидуального подбора терапии и решения вопросов, связанных с купированием назальных и глазных симптомов, со скоростью наступления эффекта, а также с приверженностью пациентов назначенной терапии. В настоящее время не подлежит сомнению тот факт, что в ряде случаев неудачи терапии связаны с низким комплаенсом пациентов. При этом использование фиксированной комбинации мометазона фуроата, золотого стандарта среди топических ГКС, с азеластина гидрохлоридом (Момат Рино Адванс) не только повышает приверженность пациентов лечению в связи с удобством применения и быстротой наступления эффекта, но и соответствует международным и российским протоколам терапии [1, 2]. ![]()
Конфликт интересов
Материал подготовлен при информационной поддержке компании Др. Редди’с Лабораторис.
A.Yu. Ovchinnikov, PhD, Prof., N.A. Miroshnichenko, PhD, Prof., N.P. Jimsheleishvili, Yu.O. Nikolaeva, PhD
A.I. Yevdokimov Moscow State University of Medicine and Dentistry
Contact person: Andrey Yu. Ovchinnikov, lorent1@mail.ru
The wide prevalence of allergic rhinitis (AR) makes it one of the urgent problems not only of modern allergology, but also of other medical specialties. The multiple symptoms of this disease significantly affects the quality of life of patients and their performance, which imposes additional requirements on medicines in terms of the speed of action and the ability to stop not only clinical manifestations, but also the focus of chronic persistent allergic inflammation. The use of the fixed combination of mometasone furoate with azelastine hydrochloride not only increases patients' adherence to treatment due to the ease of use and the speed of the onset of the effect, but also complies with international and Russian protocols of step therapy of allergic rhinitis.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.