Дифференциальная диагностика когнитивных нарушений
- Аннотация
- Статья
- Ссылки
- English

Введение
Когнитивные нарушения представляют собой одно из наиболее распространенных в клинической практике неврологических расстройств, особенно среди пациентов пожилого возраста. Согласно эпидемиологическим данным, не менее 5% лиц пожилого возраста страдают деменцией, причем в старших возрастных группах этот показатель прогрессивно возрастает [1, 2]. Кроме того, у 3–24% лиц старше 60 лет выявляются когнитивные нарушения, выходящие за пределы возрастной нормы, но не вызывающие зависимости от посторонней помощи [1, 2]. Согласно общепринятой классификации, подобные когнитивные нарушения определяются как «легкие» или «умеренные» [3].
В последние годы особое внимание уделяется так называемым субъективным когнитивным нарушениям, когда жалобы на снижение когнитивных функций не подтверждаются результатами объективных тестов. Лонгитудинальные наблюдения свидетельствуют, что значительный процент «субъективных» когнитивных нарушений со временем трансформируется в деменцию или легкие и умеренные когнитивные нарушения. Поэтому данный синдром часто знаменует собой начальные стадии деменции [4]. Исследований распространенности «субъективных» когнитивных нарушений не проводилось, но можно обоснованно предположить, что они не уступают по частоте встречаемости «объективным» (легким и умеренным) когнитивным нарушениям.
Оценка когнитивных функций пациента представляет собой неотъемлемую составляющую клинического исследования неврологического статуса. Количественные и качественные особенности обнаруженных когнитивных нарушений играют немаловажную роль в синдромальной, топической, нозологической, дифференциальной диагностике заболеваний нервной системы. На практике наиболее частыми причинами когнитивных нарушений, в особенности среди пожилых пациентов, являются болезнь Альцгеймера, цереброваскулярные заболевания и сочетание болезни Альцгеймера с цереброваскулярным заболеванием [1, 2].
Болезнь Альцгеймера – одно из наиболее распространенных нейродегенеративных заболеваний и самая частая причина деменции в пожилом возрасте. Это заболевание отвечает не менее чем за 40% выраженных когнитивных расстройств в пожилом возрасте [5]. В основе патогенеза болезни Альцгеймера лежит накопление в паренхиме головного мозга патологического нейротоксического белка – бета-амилоида, что ведет к постепенному повреждению и гибели нейронов. Результатом данного процесса становится прогрессирующая церебральная атрофия, максимально выраженная в височно-теменных отделах головного мозга.
Цереброваскулярные заболевания – вторая по частоте причина когнитивных нарушений, которая определяется по меньшей мере в 10–15% случаев [5]. К цереброваскулярным заболеваниям, согласно общепринятой классификации, относятся инсульт и хроническая недостаточность мозгового кровообращения (дисциркуляторная энцефалопатия). Когнитивные нарушения, развившиеся вследствие указанных заболеваний, принято обозначать как сосудистые когнитивные нарушения.
Проведение дифференциальной диагностики между болезнью Альцгеймера и сосудистыми когнитивными нарушениями имеет большое значение для выбора наиболее адекватной тактики ведения пациентов, прогноза и консультирования родственников. Дифференциальный диагноз базируется на количественных и качественных особенностях когнитивных расстройств, анализе другой неврологической симптоматики и данных нейровизуализации.
Важно подчеркнуть, что наличие сердечно-сосудистых заболеваний в анамнезе само по себе не может рассматриваться как неоспоримое доказательство исключительно сосудистой природы когнитивных нарушений. В настоящее время установлено, что артериальная гипертензия, гиперлипидемия, сахарный диабет и другие патологические состояния, которые традиционно трактуются как сосудистые факторы риска, повышают вероятность развития не только сосудистых когнитивных нарушений, но и болезни Альцгеймера [6, 7]. Согласно международным наблюдениям, даже деменция, впервые манифестировавшая после острого нарушения мозгового кровообращения, в ряде случаев связана с декомпенсацией болезни Альцгеймера, которая до инсульта была бессимптомной [8, 9].
Особенности когнитивных нарушений при болезни Альцгеймера и цереброваскулярных заболеваниях
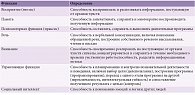
Согласно DSM-V, к когнитивным функциям относятся внимание, память, праксис, гнозис, речь, управляющие функции и социальный интеллект (табл. 1) [10].
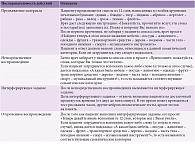
Для дифференциальной диагностики между болезнью Альцгеймера и сосудистыми когнитивными нарушениями исключительно важно провести нейропсихологический анализ мнестических расстройств, для чего используют специальные методики, облегчающие запоминание и воспроизведение (например, тест «12 слов», табл. 2) [11].
Нарушения памяти встречаются при обоих заболеваниях, однако имеют принципиальные различия. Выраженные и прогрессирующие нарушения памяти – самый ранний и важный для клинической диагностики симптом болезни Альцгеймера. Как правило, он появляется еще до других когнитивных расстройств, то есть до развития деменции. В первую очередь страдают запоминание текущих событий и воспоминания о недавнем прошлом, в то время как отдаленные события жизни сохраняются в памяти вплоть до стадии выраженной деменции (закон Рибо). Кроме того, болезни Альцгеймера свойствен такой дисмнестический симптом, как посторонние вплетения при воспроизведении (конфабуляции) [12–14].
Нарушения памяти при сосудистых когнитивных нарушениях выражены в значительно меньшей степени, чем при болезни Альцгеймера, и носят стационарный или малопрогредиентный характер. Преимущественно страдает оперативная память: пациент не может припомнить, что куда положил, забывает, что нужно сделать, не может усвоить новые алгоритмы деятельности (например, как пользоваться новым сотовым телефоном). В то же время нарушения памяти не распространяются на текущие события, отсутствует присущая болезни Альцгеймера преимущественная уязвимость воспоминаний о недавнем прошлом по сравнению с отдаленными событиями [15–18].
Большое значение для дифференциальной диагностики имеет также анализ речевого статуса пациента. При сосудистых когнитивных нарушениях, в отсутствие инсультов в анамнезе с типичной локализацией патологического очага, дисфазия не наблюдается. Нарушения речи могут быть представлены дизартрией и диспросодией, связанной с наличием псевдобульбарного паралича и/или амиостатическим синдромом [15–18].
При болезни Альцгеймера, наоборот, прогрессирующая дисфазия – типичный когнитивный симптом, который присутствует в подавляющем большинстве случаев. На начальных стадиях болезни Альцгеймера дисфазия представлена недостаточностью номинативной функции речи: пациент не может правильно назвать демонстрируемый предмет, часто вместо названия говорит предназначение предмета (например, «то, чем пишут» вместо «ручка»). В дальнейшем изменяется речевая продукция: из нее исчезает большинство существительных, что делает речь малосодержательной. Может частично страдать понимание обращенной речи. Наиболее быстро речевые нарушения прогрессируют при пресенильных формах болезни Альцгеймера, хотя и у пожилых пациентов практически всегда можно обнаружить дисфазию различной степени выраженности [12–14].
Нарушения внимания и управляющей функции (планирование и контроль) в большей степени присущи сосудистым когнитивным нарушениям [15–18]. Обычно данные нарушения развиваются раньше других и достаточно выражены уже на стадии умеренных когнитивных расстройств. Весьма характерно снижение темпа познавательной деятельности: на любую интеллектуальную активность затрачивается больше времени, чем в норме, пациенты быстрее устают и отвлекаются от начатого дела. Другой ранний когнитивный симптом – снижение интеллектуальной гибкости: пациенты испытывают нерешительность и подчас непреодолимые трудности при необходимости смены привычной парадигмы деятельности. Из-за этого пожилые люди с сосудистыми когнитивными нарушениями становятся более консервативными и осторожными, с подозрением и нежеланием относятся к любым переменам привычного уклада жизни.
При болезни Альцгеймера внимание и управляющие функции длительное время остаются относительно сохранными. В небольшой степени они могут нарушаться у пациентов более пожилого возраста и обычно уже на стадии деменции [12–14]. В нейропсихологии для оценки внимания и управляющих функций используются тесты, в которых оценивают время выполнения задания. В качестве примера такого теста, который, по мнению международного научного сообщества, весьма чувствителен к самым ранним проявлениям сосудистых когнитивных нарушений, можно привести тест цифр и букв (табл. 3) [11].
Нарушения зрительно-пространственного гнозиса и праксиса присущи и болезни Альцгеймера, и сосудистым когнитивным нарушениям, поэтому не могут служить надежным дифференциально-диагностическим признаком. Могут возникать проблемы при рисовании трехмерных геометрических фигур (например, кубика) или расположения стрелок на циферблате часов на заданное время (тест рисования часов). Однако при сосудистых когнитивных нарушениях пространственные расстройства достаточно редко приводят к трудностям ориентирования на местности, в то время как при болезни Альцгеймера это почти облигатный когнитивный симптом. Поэтому у пациентов с болезнью Альцгеймера раньше возникают сложности с ориентированием в малознакомых местах, позже у них нарушается способность путешествовать по хорошо знакомым маршрутам [12–18].
Другие нарушения гнозиса и праксиса (проблемы с узнаванием предметов, знакомых лиц, идеаторная, идеомоторная и кинетическая апраксия) проявляются при болезни Альцгеймера достаточно поздно, на стадии развернутой деменции и поэтому тоже не могут служить надежным ориентиром в дифференциальной диагностике.
Как при болезни Альцгеймера, так и при цереброваскулярном заболевании так называемый социальный интеллект нарушается не сразу. Следует отметить, что на стадии развернутой деменции проведение нейропсихологического тестирования и интерпретация его результатов крайне затруднительны из-за общей выраженности когнитивных нарушений, трудностей коммуникации с пациентом, снижения его мотивации.
Неврологический статус
Важнейшая отличительная особенность болезни Альцгеймера – отсутствие на стадии легкой и умеренной деменции первичных двигательных, сенсорных и тазовых нарушений. В неврологическом статусе не обнаруживается какой-либо очаговой симптоматики. Однако как у здоровых пожилых людей, так и у пациентов с болезнью Альцгеймера иногда могут присутствовать умеренный хоботковый рефлекс, легкая гипомимия и гипокинезия. Приблизительно в 10% случаев гипомимия и гипокинезия могут достигать клинической значимости и сопровождаться повышением мышечного тонуса. Предполагается, что речь идет об особом морфологическом варианте болезни Альцгеймера, при котором наряду с типичными для основного заболевания признаками имеются также тельца Леви. В нейропсихологическом статусе таких пациентов помимо типичных когнитивных симптомов определяются более выраженные нарушения внимания и управляющих функций (планирования и контроля). Возможно, в таких случаях могут сочетаться два нейродегенеративных заболевания – болезнь Альцгеймера и деменция с тельцами Леви [12, 19, 20].
На поздних стадиях болезни Альцгеймера в неврологическом статусе появляются так называемые примитивные рефлексы: хватательные, орального автоматизма, феномен противодержания. Характерны миоклонии, иногда наблюдаются генерализованные тонико-клонические эпилептические припадки. Ослабляется контроль над тазовыми органами. В последнюю очередь нарушается самостоятельная ходьба [12, 21, 22].
Напротив, при сосудистых когнитивных нарушениях на фоне цереброваскулярных заболеваний очаговая неврологическая симптоматика формируется достаточно рано, обычно еще на стадии умеренных когнитивных нарушений. Совсем недавно пристальное внимание уделялось так называемой микросимптоматике: симметричному повышению сухожильных рефлексов, оживлению хоботкового рефлекса, незначительному постурально-кинетическому тремору при выполнении координаторных проб и т.д. Между тем вышеперечисленные симптомы представляют собой весьма распространенный вариант нормы и часто встречаются не только при сосудистых когнитивных нарушениях, но и при болезни Альцгеймера, а также у здоровых пожилых людей. Следовательно, так называемая микросимптоматика не может рассматриваться в качестве аргумента в пользу сосудистой этиологии когнитивных нарушений. Существенно большее значение имеют специфические нарушения походки, псевдобульбарный синдром (не только рефлексы орального автоматизма!) и раннее развитие тазовых нарушений.
Хроническая недостаточность мозгового кровообращения, как известно, приводит к формированию диффузных изменений белого вещества (лейкоареозу). Поражение белого вещества влечет за собой нарушение связей между корковыми и подкорковыми отделами головного мозга, включая мозжечок. В результате одной из первых страдает система постурального контроля. Изменяется походка пациентов: укорачивается шаг и увеличивается база ходьбы (лобная дисбазия) [23]. Имеют место падения, которые чаще всего возникают в начале ходьбы, при поворотах и остановках. По данным международных исследований, риск падений в пожилом возрасте достоверно коррелирует с выраженностью лейкоареоза [24].
Пациенты с лобной дисбазией обычно жалуются на головокружение, которое носит несистемный характер и описывается как чувство неустойчивости и пошатывания во время ходьбы. В то же самое время системное (вестибулярное) головокружение хронической недостаточности мозгового кровообращения не свойственно [25].
Лобная дисбазия – достаточно ранний неврологический симптом хронического цереброваскулярного заболевания. Позже, как правило, на стадии сосудистой деменции, присоединяется псевдобульбарный синдром, обычно в сочетании с асимметричным пирамидным тетрасиндромом и тазовыми нарушениями по центральному типу. Следует подчеркнуть, что о псевдобульбарном синдроме правомерно говорить при наличии наряду с рефлексами орального автоматизма дизартрии и дисфонии, реже дисфагии, а также насильственного плача или смеха. Сочетание псевдобульбарного синдрома и пирамидного тетрапареза свидетельствует о поражении моста, который наряду с подкорковыми базальными ядрами и внутренней капсулой представляет собой типичную локализацию гипертензивных лакунарных инфарктов [12, 23, 26].
Нейровизуализация
Неоспоримо доказывает сосудистое поражение головного мозга наличие церебральных инфарктов при структурной нейровизуализации – компьютерной рентгеновской или магнитно-резонансной томографии головного мозга. При этом обнаруженные в ходе нейровизуализации инфаркты мозга не всегда свидетельствуют об инсультах в анамнезе. В настоящее время установлено, что на каждый инсульт приходится не менее четырех-пяти «немых» инфарктов, которые развиваются без клинических симптомов острого нарушения мозгового кровообращения [27]. Обычно «немые» инфаркты небольшие по величине, соответствуют критериям лакунарного инфаркта (не более 10–15 мм в диаметре). Причина формирования «немых» лакунарных инфарктов – микроангиопатия при артериальной гипертензии, сахарном диабете, реже церебральной амилоидной ангиопатии, системных васкулитах и др. В типичных случаях поражение головного мозга локализуется в области подкорковых базальных ганглиев и глубинных отделах белого вещества, поскольку данные структуры кровоснабжаются пенетрантными артериями небольшого калибра, особенно уязвимыми при заболеваниях с микроангиопатией.
Другим признаком сосудистого поражения головного мозга являются диффузные изменения белого вещества головного мозга – лейкоареоз. Лейкоареоз гиперинтенсивен на Т2-взвешенных изображениях с подавлением сигнала от свободной воды (так называемый FLAIR-режим), в то время как последствия церебральных инфарктов в данном режиме нейровизуализации изоинтенсивны. В отличие от инфарктов головного мозга лейкоареоз не абсолютно специфичен для цереброваскулярного заболевания. Аналогичные изменения белого вещества могут наблюдаться при нейродегенеративных, демиелинизирующих, дисметаболических заболеваниях, хронических цефалгических синдромах, нормальном старении. Поэтому дифференциально-диагностическое значение лейкоареоза относительно. Как проявление сосудистого заболевания данный феномен может расцениваться лишь при соответствующем анамнезе, одновременном наличии инфарктов мозга, характерных клинических симптомах [16, 23, 26, 28].
Инфаркты мозга и лейкоареоз свидетельствуют в пользу наличия сосудистого поражения головного мозга, но при этом не доказывают, что все имеющиеся когнитивные расстройства связаны с цереброваскулярным заболеванием. Следует иметь в виду высокий процент коморбидных состояний, когда цереброваскулярное заболевание сочетается с нейродегенеративным процессом. Окончательное суждение о природе когнитивных нарушений в таких случаях делается на основании анализа всей совокупности имеющихся клинических и параклинических данных, включая особенности когнитивных нарушений (см. выше).
К нейровизуализационным признакам болезни Альцгеймера относится церебральная атрофия, которая максимально выражена в височно-теменных отделах головного мозга. Наиболее специфичны атрофические изменения в медиальных отделах височной доли, в том числе в гиппокампе. Дополнительное наличие легкого или умеренного лейкоареоза, особенно возле задних рогов боковых желудочков, не противоречит диагнозу [12, 29, 30].
Проблема смешанной деменции
Обычно о смешанной деменции (или смешанных когнитивных нарушениях) говорят при наличии сочетанного сосудистого и дегенеративного поражения головного мозга. Однако данный термин остается слишком неопределенным и поэтому его лучше избегать. Как известно, коморбидность в пожилом возрасте является скорее правилом, чем исключением, поэтому велика вероятность сочетания не только дегенеративного и цереброваскулярного патологического процесса, но и двух дегенеративных заболеваний (например, болезни Альцгеймера и деменции с тельцами Леви, о чем уже говорилось выше). В этой связи, с нашей точки зрения, более корректен диагноз «болезнь Альцгеймера с цереброваскулярным заболеванием».
По данным клинико-морфологических сопоставлений, выполненных на рубеже ХХ и ХХI веков, в 48–77% случаев деменций в пожилом возрасте определяется сочетание патологоанатомических признаков болезни Альцгеймера и цереброваскулярного заболевания [20, 31, 32]. Однако не во всех указанных случаях можно говорить о смешанной природе когнитивных нарушений. Болезнь Альцгеймера, как и цереброваскулярное заболевание, длительное время остается бессимптомной. Поэтому наличие морфологических изменений не обязательно свидетельствует об их связи с клиническими проявлениями. Для обоснованного суждения о комплексной этиологии когнитивных нарушений необходимо наличие не только морфологических и/или нейровизуализационных, но и клинических признаков двух заболеваний [33]. В таком случае одновременно наблюдаются прогрессирующие в соответствии с законом Рибо нарушения памяти, дисфазические расстройства и угнетение управляющих функций, внимания, нарушения походки с расстройствами равновесия, падениями и другие характерные неврологические симптомы. При указанном диагностическом подходе обычно до 15% деменций в пожилом возрасте признаются «смешанными» [5]. Сочетанная цереброваскулярная и нейродегенеративная патология чаще встречается в пожилом и особенно старческом возрасте (после 75 лет). Напротив, «чистые» сосудистые или нейродегенеративные расстройства наблюдаются у более молодых пациентов.
Основные подходы к ведению пациентов с сосудистыми и дегенеративными когнитивными нарушениями
При болезни Альцгеймера с синдромом выраженных нейрокогнитивных нарушений (деменцией) показаны ингибиторы ацетилхолинэстеразы (донепезил, ривастигмин, галантамин) и/или мемантин. На фоне применения данных препаратов достоверно улучшаются память и другие когнитивные функции, пациенты становятся более самостоятельными в повседневной жизни, уменьшается нагрузка на родственников, осуществляющих уход. Высказывается мнение о целесообразности максимально ранней нейротрансмиттерной терапии, хотя данные о ее эффективности на стадии недементных когнитивных нарушений противоречивы. К сожалению, ацетилхолинергическая терапия или мемантин не могут остановить прогрессирование патологического процесса при болезни Альцгеймера, но могут несколько его замедлить. В настоящее время активно разрабатываются новые подходы к патогенетической терапии болезни Альцгеймера, направленные на то, чтобы предотвратить накопление в мозге амилоидного белка или уменьшить его нейротоксический эффект. Подобная терапия теоретически могла бы надолго остановить прогрессирование нейродегенеративных когнитивных нарушений [29, 30].
При преимущественно сосудистой природе когнитивных нарушений в первую очередь необходимо лечить базисное сосудистое заболевание – артериальную гипертензию, церебральный атеросклероз, гиперлипидемию, сахарный диабет и др. В настоящее время накоплено достаточно подтверждений тому, что своевременная и корректная антигипертензивная терапия достоверно уменьшает риск развития деменции в пожилом возрасте [34]. Менее определена роль антитромбоцитарной и гиполипидемической терапии [35, 36]. Однако антитромбоцитарные и гиполипидемические препараты по соответствующим показаниям должны назначаться для профилактики повторных острых нарушений мозгового кровообращения. Безусловно, рекомендованы немедикаментозные методы (оптимизация питания и образа жизни, умственная и физическая активность), которые, как было продемонстрировано в исследовании FINGER, замедляют прогрессирование нарушений внимания и управляющих функций, то есть тех когнитивных расстройств, которые обычно вызываются цереброваскулярным заболеванием [37].
Имеется положительный опыт использования ингибиторов ацетилхолинэстеразы и мемантина на стадии сосудистой деменции, однако терапевтический эффект этих препаратов несколько меньше того, который они оказывают при болезни Альцгеймера [38].
Несмотря на значительные различия патогенеза и клинических проявлений, наряду с приведенными выше особенностями существуют общие подходы к терапии болезни Альцгеймера и сосудистых когнитивных нарушений. И в том, и в другом случае показаны нейрометаболические препараты с нейропротективными свойствами. К числу таких препаратов относится Актовегин®.
Актовегин® представляет собой производное крови молодых телят, которое содержит несинтетические биологически активные соединения. Препарат оказывает антиишемический, антиоксидантный и инсулиноподобный эффект. В экспериментальных условиях Актовегин® продемонстрировал способность уменьшать нейротоксическое действие церебрального амилоидного белка и препятствовать процессам перекисного окисления липидов [39].
Недавно с помощью методов капилляроскопии и лазерной допплероскопии было продемонстрировано благоприятное влияние препарата на эндотелиальную функцию, которую в настоящее время большинство экспертов рассматривают в качестве основного механизма формирования лейкоареоза при хронической недостаточности мозгового кровообращения. При этом увеличение капиллярной перфузии ассоциировалось с регрессом выраженности сосудистых когнитивных нарушений [40]. Таким образом, Актовегин® исходя из своего механизма действия имеет точки приложения как при болезни Альцгеймера, так и при цереброваскулярных заболеваниях.
Клиническая эффективность препарата Актовегин® при когнитивных нарушениях как сосудистой, так и нейродегенеративной этиологии подтверждается результатами многочисленных международных и отечественных исследований и многолетним опытом практического применения.
В. Херрманн и соавт. оценивали эффективность препарата Актовегин® в дозе 250 мл 20%-ного раствора внутривенно капельно в течение четырех недель по сравнению с плацебо у пациентов с сосудистой деменцией и деменцией при болезни Альцгеймера [41]. Актовегин® способствовал достоверному улучшению когнитивных функций и повышению самостоятельности пациентов в повседневной жизни. Улучшение когнитивных функций на фоне терапии препаратом Актовегин® у пациентов с деменцией легкой или умеренной степени различной этиологии наблюдали также S. Kanowski и соавт. [42].
Актовегин® может применяться как при деменциях, так и при когнитивных нарушениях, не вызывающих дезадаптации в повседневной жизни (легких или умеренных когнитивных нарушениях). В работе B. Saletu и соавт. препарат Актовегин® назначался в виде внутривенных вливаний пожилым пациентам с недементными когнитивными нарушениями различной этиологии. Уже через две недели от начала приема было отмечено достоверное улучшение памяти, внимания и других когнитивных функций. Одновременно наблюдались нормализация биоэлектрической активности головного мозга по данным электроэнцефалографии и увеличение амплитуды когнитивного вызванного потенциала Р300 [43].
Аналогичные результаты были получены в работе W.D. Oswald и соавт. Пациенты с недементными когнитивными нарушениями сосудистой и предположительно нейродегенеративной природы принимали Актовегин® перорально в дозе 400 мг три раза в день в течение восьми недель. На фоне лечения отмечался достоверный регресс выраженности когнитивных и других нервно-психических расстройств органической природы [44].
В исследование В. Янсена и Г. Брукнера вошли пациенты с недементными сосудистыми когнитивными нарушениями. В течение 12 недель они принимали препарат Актовегин® перорально по 1200 и 1800 мг/сут. Прием препарата в указанных режимах способствовал достоверному улучшению когнитивных функций при сопоставимом терапевтическом эффекте, что свидетельствует о нецелесообразности повышения дозы до 1800 мг/сут [45].
В нашей стране недавно было завершено два небольших исследования эффективности препарата Актовегин® при умеренных когнитивных нарушениях сосудистой этиологии. О.Д. Остроумова и соавт. применяли Актовегин® в дозе 2000 мг внутривенно в течение первых семи дней и далее перорально по 1200 мг/сут в течение 11 недель у пациентов с умеренными когнитивными нарушениями на фоне артериальной гипертензии второй и третьей стадии [46]. У пациентов достоверно улучшались память, внимание и самочувствие. В работе С.И. Гаврилова и соавт. было показано достоверное улучшение когнитивных функций и общего клинического статуса в целом на фоне внутримышечного введения препарата Актовегин® в течение 28 дней пациентам с умеренными сосудистыми когнитивными нарушениями [47].
Во всех исследованиях отмечается благоприятный профиль безопасности и переносимости препарата Актовегин®, в том числе у пожилых лиц с сопутствующими хроническими сердечно-сосудистыми заболеваниями.
Заключение
Стратегия ведения пациентов с когнитивными нарушениями во многом определяется этиологией и выраженностью имеющихся расстройств. Однако во всех случаях можно применять нейропротективные препараты, влияющие на универсальные конечные механизмы повреждения нейронов. Использование таких препаратов, как Актовегин®, способствует регрессу когнитивных и других нервно-психических расстройств, позволяет пациентам с цереброваскулярными расстройствами и нейродегенеративными заболеваниями быть более самостоятельными.
V.V. Zakharov
I.M. Sechenov First Moscow State Medical University
Contact person: Vladimir Vladimirovich Zakharov, zakharovenator@gmail.com
Alzheimer’s disease and cerebrovascular diseases represent the most common causes of cognitive impairments. Differential diagnosis between vascular and neurodegenerative cognitive impairments is based on neuropsychological, neurological features as well as neurovisualization data. During Alzheimer's disease, memory impairment dominates, but no focal neurological symptoms are documented, with typical atrophy mainly of temporal and parietal brain regions. In case of cerebrovascular disease there are attention deficit, impaired executive functions; neurologically, pseudobulbar palsy and impaired walking, and neuroimaging analysis reveals cerebral infarctions and leukoaraiosis. In many cases, especially in elderly patients, signs of both vascular and neurodegenerative cerebral injury are observed. Certain differences in patient management exist depending on the cause of cognitive impairments. However, during both neurodegenerative and vascular cognitive impairments, neurometabolic drugs with neuroprotective effect are used.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.