Применение устекинумаба у больных псориатическим артритом: клинические примеры
- Аннотация
- Статья
- Ссылки
- English
В статье рассмотрены примеры применения устекинумаба у пациентов с псориатическим артритом. На фоне такого лечения отмечалась положительная динамика симптомов заболевания.
В статье рассмотрены примеры применения устекинумаба у пациентов с псориатическим артритом. На фоне такого лечения отмечалась положительная динамика симптомов заболевания.
Введение
Псориатический артрит (ПсА) – гетерогенное хроническое воспалительное заболевание с широким спектром клинических проявлений и различными особенностями течения [1]. Известно, что при ПсА в воспалительный процесс вовлекается не только опорно-двигательный аппарат (суставы, энтезисы, синовиальные оболочки сухожилий, позвоночник), но и кожа, ногтевые пластины, кишечник, органы зрения [2–4]. Кроме того, у больных ПсА или псориазом (Пс) повышен риск развития ожирения, инсулинорезистентности, сахарного диабета 2 типа, метаболического синдрома, артериальной гипертензии, гиперлипидемии, сердечно-сосудистых заболеваний [5].
За последние три десятилетия терапия ПсА стала значительно эффективнее благодаря изучению патогенеза заболевания и использованию биотехнологий для создания новых лекарственных средств.
В настоящее время для лечения ПсА применяются:
- нестероидные противовоспалительные препараты (НПВП); глюкокортикостероиды (ГКС);
- базисные противовоспалительные препараты (БПВП);
- таргетные синтетические базисные противовоспалительные препараты; генно-инженерные биологические препараты (ГИБП).
Целью терапии является подавление прогрессирования деструктивных повреждений и улучшение качества жизни больных [1, 6, 7].
В связи с тем что у части больных ПсА наблюдается непереносимость или неэффективность терапии БПВП и ГИБП, например ингибиторами фактора некроза опухоли (ФНО) альфа, возникает потребность в препаратах с другим механизмом действия. К таким препаратам относится устекинумаб.
Устекинумаб представляет собой человеческие моноклональные антитела к интерлейкинам (ИЛ) 12 и 23 (ИЛ-12/23р40). По своей структуре он относится к иммуноглобулинам класса G1 (IgG1). За счет связывания субъединицы p40 ИЛ-12 и ИЛ-23 устекинумаб препятствует их взаимодействию с рецепторами ИЛ-12Rß1, расположенными на естественных клетках-киллерах и T-лимфоцитах. За счет этого не формируются опосредованные ИЛ-12 и ИЛ-23 сигналы и ассоциированные с этим созревание, а также экспансия клеток Th1 и Th17. Устекинумаб снижает индуцированную ИЛ-12 и ИЛ-23 экспрессию клеточных поверхностных маркеров, которые отвечают за миграцию, активацию, выброс цитокинов. Кроме того, препарат модулирует вызываемую указанными ИЛ секрецию про- и противовоспалительных цитокинов. В результате прерывается аномальный цитокиновый каскад, лежащий в основе патогенеза Пс и ПсА [8].
Эффективность и безопасность устекинумаба при Пс и ПсА хорошо изучены в международных многоцентровых рандомизированных плацебоконтролируемых клинических исследованиях [9–18].
Необходимо отметить, что устекинумаб находит все более широкое применение в терапии Пс и ПсА в мире в целом и в Российской Федерации в частности.
Ниже представлены примеры применения устекинумаба в реальной клинической практике.
Клинический случай 1
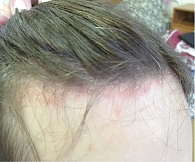
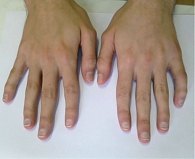
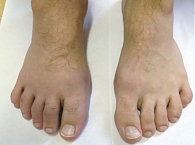
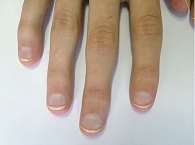
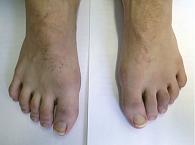
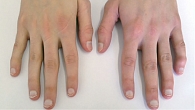
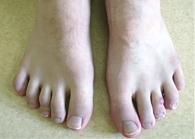
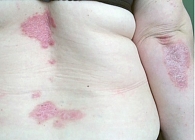
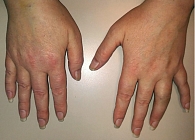
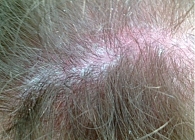
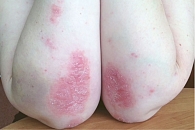
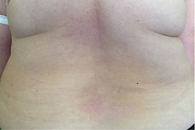
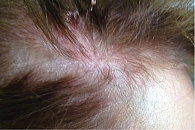
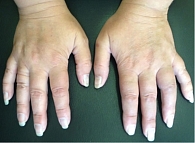
Пациент Ж., 23 года. Наблюдается по поводу ПсА. Проявления заболевания классические: артрит, дактилит, боль в нижней части спины воспалительного ритма, плантарный фасциит слева (рис. 1–5). Псориаз впервые выявлен три месяца назад. Площадь поражения кожи (Body Surface Are – BSA) – 3%. Симптомы ПсА появились два месяца назад. Помимо Пс наблюдалась псориатическая ониходистрофия (рис. 5). Число болезненных суставов (ЧБС) – 13, число припухших суставов (ЧПС) – 13, индекс активности заболевания (Disease Activity Score – DAS/DAS 28) – 5,47/4,85 балла.
Начато лечение метотрексатом. Препарат вводился подкожно в дозе 10 мг в неделю с последующим повышением дозы до 25 мг в неделю. Кроме того, больной получал НПВП и ГКС. Последний препарат вводился однократно внутрь сустава.
Через три месяца терапии метотрексатом в дозе 25 мг у больного сохранялись дактилиты правой стопы, артрит плюснефаланговых суставов правой стопы, развился дактилит третьего пальца левой стопы (рис. 6), правого лучезапястного сустава, проксимального межфалангового сустава второго пальца правой кисти. ЧПС – 10, скорость оседания эритроцитов (СОЭ) – 54 мм/ч (по Вестергрену), уровень С-реактивного белка (СРБ) – 26,8 мг/л, активность ПсА умеренная – 4,68 балла по DAS 28 и 5,1 балла по DAS.
Из-за недостаточного эффекта метотрексата в схему лечения был добавлен устекинумаб. Препарат вводили подкожно в дозе 45 мг. На фоне такой терапии состояние больного улучшилось. Через четыре недели после второй инъекции устекинумаба клинико-лабораторная активность заболевания снизилась до состояния ремиссии: BSA – 0%, ЧПС – 0, СОЭ – 3 мм/ч (по Вестергрену), уровень СРБ – 1,3 мг/л, DAS 28 – 0,77 балла, DAS – 0,36 балла (рис. 7–10).
Через четыре недели после третьей инъекции устекинумаба в дозе 45 мг пациент был переведен на монотерапию. Метотрексат был отменен из-за развития острой фолликулярной ангины с лимфаденитом. Несмотря на отмену метотрексата, ремиссия сохранялась: ЧВС – 0, DAS – 0,32 балла, DAS 28 – 0,53 балла, СОЭ – 2 мм/ч, уровень СРБ – 0,8 мг/л, BSA – 0%. Кроме того, исчезла болезненность в области прикрепления плантарной фасции к левой пяточной кости.
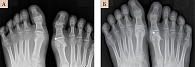
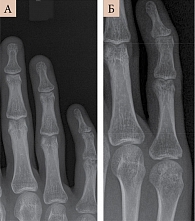
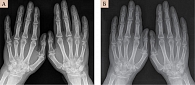
Через 12 месяцев комбинированной и монотерапии рент-генологического прогрессирования ПсА не наблюдалось (рис. 11 и 12). До лечения, согласно результатам рентгенографии стоп, асимметричные изменения: выраженный околосуставной остеопороз справа, сужение щелей. Множественные кистовидные просветления костной ткани в головках плюсневых костей справа. Нечеткость контура первой плюсневой головки правой стопы – эрозия (рис. 11А). Через 12 месяцев лечения ухудшения состояния не наблюдалось (рис. 11Б). Согласно рентгенограмме левой кисти, до начала лечения – сужение щелей многих суставов, эрозии проксимального межфалангового и пястно-фалангового суставов пятого пальца (рис. 12А), через 12 месяцев лечения новых эрозий не обнаружено (рис. 12Б).
Таким образом, у больного Ж. устекинумаб в сочетании с метотрексатом и в виде монотерапии оказался высокоэффективным. Достигнута ремиссия ПсА, регресс Пс до полного исчезновения, купированы дактилиты и энтезит.
Клинический случай 2
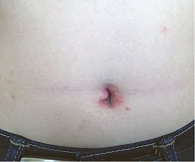
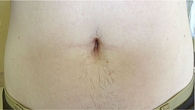
Пациентка М., 52 года. Наблюдается по поводу ПсА и Пс. Длительность заболеваний – шесть и девять месяцев соответственно. Помимо ПсА выявлены признаки метаболического синдрома, такие как резистентность к инсулину, абдоминальное ожирение (индекс массы тела (ИМТ) – 31,5 кг/м2), артериальная гипертензия, дис-липидемия.
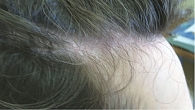
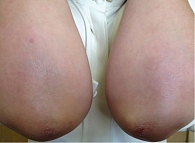
Активность ПсА умеренная: ЧБС – 8, ЧПС – 6, СОЭ – 18 мм/ч (по Вестергрену), уровень СРБ – 16 мг/л, DAS 28 – 4,7 балла, DAS – 3,77 балла. Тяжесть Пс оценивалась как среднетяжелая: BSA – 10%, индекс тяжести псориаза и его распространенности (Psoriasis Area and Severity Index – PASI) – 8,7 балла (рис. 13–16).
Назначен метотрексат в виде подкожных инъекций в дозе 15 мг один раз в неделю и НПВП. Через три месяца лечения доза метотрексата была снижена из-за повышения уровня печеночных трансаминаз в два раза относительно верхней границы нормы. Кроме того, сохранялась клинико-лабораторная активность ПсА: ЧБС – 6, ЧПС – 4, СОЭ – 22 мм/ч (по Вестергрену), уровень СРБ – 11,3 мг/л, DAS 28 – 4,35 балла, DAS – 2,83 балла, BSA – 7,5%, PASI – 4 балла.
Из-за наличия неблагоприятных факторов прогноза (полиартрит, эрозии суставов, повышение СОЭ/СРБ), недостаточной эффективности/плохой переносимости терапии пациентке М. был назначен устекинумаб подкожно в дозе 45 мг. Доза метотрексата составляла 10 мг в неделю.
После двух инъекций устекинумаба (на нулевой и четвертой неделях) и перед третьей инъекцией (16-я неделя) отмечено значительное улучшение состояния, снижение активности ПсА и Пс: ЧБС – 0, ЧПС – 0, СОЭ – 20 мм/ч (по Вестергрену), DAS 28 – 2,32 балла, DAS – 1,1 балла, BSA – 0,1% (рис. 17–20).
Через 12 месяцев комбинированной терапии ИМТ не увеличился – 30,5 кг/м2. Кроме того, не отмечалось отрицательной динамики рентгенологических изменений в кистях (рис. 21). До лечения на рентгенограмме пятнистый остеопороз пальцев левой кисти, костные пролиферации на краях суставов, периоститы основной фаланги пятого пальца левой кисти, эрозии проксимального межфалангового сустава четвертого пальца левой кисти, сужение щелей отдельных суставов, через 12 месяцев – состояние не ухудшилось.
Таким образом, у пациентки с ранним ПсА и метаболическим синдромом удалось добиться ремиссии ПсА и значительного регресса Пс после назначения устекинумаба в дозе 45 мг в комбинации с метотрексатом в дозе 10 мг в неделю (подкожное введение). На фоне такого лечения ремиссия сохранялась более года.
Обсуждение результатов лечения
Результаты клинической практики свидетельствуют о положительном влиянии устекинумаба на Пс и основные проявления ПсА: артрит, дактилит, энтезит. Согласно результатам рандомизированных клинических исследований PSUMMIT-1 и -2, на 24-й неделе улучшение симптомов артрита, кожных проявлений Пс, дактилита, энтезита, функциональных способностей у получавших устекинумаб было более выраженным, чем у принимавших плацебо [16, 17]. Эффект лечения сохранялся в течение длительного времени (до 100 недель). При этом эффективность достигалась независимо от сопутствующего приема метотрексата.
У наших пациентов в течение 12 месяцев не наблюдалось рент-генологического прогрессирования деструктивных процессов в суставах. Это согласуется с данными крупных рандомизированных клинических исследований. Комплексный анализ рентгенологических данных исследований PSUMMIT-1 и -2 продемонстрировал значительно меньшее прогрессирование деструктивных процессов в суставах на 24-й неделе у больных ПсА в группе устекинумаба по сравнению с группой плацебо [19]. Клиническая эффективность и сдерживание рентгенологического прогрессирования поддерживались в течение 52 и 100 недель (PSUMMIT-1).
Как отмечалось ранее, у больных Пс и ПсА повышен риск развития сердечно-сосудистых заболеваний. В настоящее время влияние ГИБП на повышение или понижение сердечно-сосудистого риска активно изучается. У пациентов, принимавших устекинумаб, не установлено возрастания риска развития сердечно-сосудистых заболеваний [20]. По мнению авторов исследования, проведенный анализ не установил положительного либо отрицательного влияния устекинумаба на таковой, поэтому для окончательного вывода следует проводить дальнейшие наблюдения.
Заключение
Устекинумаб может быть показан пациентам с ранним ПсА и на более поздних стадиях заболевания при наличии полиартрита (пять и более воспаленных суставов), дактилитов, энтезитов, умеренной или высокой активности воспалительного процесса, среднетяжелого или тяжелого псориаза и/или псориатической ониходистрофии, высоком риске инфекций, наличии сердечно-сосудистых заболеваний, метаболического синдрома, при недостаточной эффективности предшествующей терапии БПВП (метотрексатом или лефлуномидом и сульфасалазином). Кроме того, при плохой переносимости или непереносимости БПВП эффективна монотерапия устекинумабом, так как препарат обладает низкой иммуногенностью.
Наши данные подтверждают, что лечение устекинумабом способствует снижению клинико-лабораторной активности ПсА и Пс и может замедлить деструктивные процессы в пораженных суставах.
Yu.L. Korsakova, PhD, Ye.Yu. Loginova, PhD, T.V. Korotayeva, MD, PhD
V.A. Nasonova Research Institute of Rheumatology
Contact person: Tatiana V. Korotayeva, tatianakorotaeva@gmail.ru
Psoriatic arthritis is a heterogeneous chronic inflammatory disease with a wide range of clinical manifestations and variants of course. For its treatment, non-steroidal anti-inflammatory drugs, glucocorticosteroids, basic anti-inflammatory drugs, targeted synthetic basic anti-inflammatory drugs, genetically engineered biological drugs are used. One of the representatives of the latter is ustekinumab. Ustekinumab – fully human monoclonal antibodies to interleukin 12/23p40 – belonging to the G1 class immunoglobulins.
The article considers the use of ustekinumab in patients with psoriatic arthritis. Positive dynamics of the disease symptoms was noted on the background of such treatment.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.