Результаты первого ретроспективного исследования алоглиптина по сравнению с другими пероральными сахароснижающими препаратами у пациентов с сахарным диабетом 2 типа в России ARRIVAL
- Аннотация
- Статья
- Ссылки
- English
Цель. Целью наблюдательного ретроспективного исследования стал сравнительный анализ влияния алоглиптина и других ССП на уровень гликированного гемоглобина (HbA1c), достижение/удержание гликемических целей и частоту сердечно-сосудистых событий.
Материал и методы. В анализ вошли данные электронных медицинских карт (ЭМК) на основании соглашения о передаче обезличенных данных пациентов с сахарным диабетом 2 типа из 129 медицинских организаций 14 субъектов Российской Федерации. На первом этапе учитывали все ЭМК, соответствующие критериям включения/невключения (n = 90 546), на втором – количественные исходы согласно псевдорандомизации по 28 исходным переменным (n = 71 932). Анализируемые ССП включали алоглиптин, метформин, другие иДПП-4, ингибиторы натрий-глюкозного котранспортера 2 (иНГЛТ-2) и производные сульфонилмочевины (ПСМ).
Результаты. Алоглиптин продемонстрировал максимальную степень снижения гликемии – на 0,5 ммоль/л (р < 0,004). В группе иНГЛТ-2 динамика изменений не достигла статистической значимости, что определило преимущество алоглиптина (p = 0,0002). На фоне алоглиптина отмечалось максимальное снижение уровня HbA1c (-0,8%; р < 0,0001) в отсутствие такового в группах других иДПП-4 и иНГЛТ-2. К окончанию наблюдения доли пациентов с целевым значением HbA1c составили 85% в группе алоглиптина, 63% в группе ПСМ, 67% в группе метформина и 38% в группе иНГЛТ-2. Алоглиптин обеспечивал удержание гликемического контроля чаще, чем другие иДПП-4 (p = 0,01). Отмечено превосходство алоглиптина относительно ПСМ (p = 0,007) и метформина (p = 0,03). При анализе безопасности в группе алоглиптина регистрировалось наименьшее число неблагоприятных событий, включая острые нарушения мозгового кровообращения, острый инфаркт миокарда и другие значимые кардиоваскулярные события. Наибольшее их число было в группе ПСМ. Гипогликемия фиксировалась только в группах ПСМ и метформина.
Выводы. Алоглиптин продемонстрировал преимущество перед другими ССП в отношении влияния на уровень HbA1c, достижение/удержание гликемических целей и кардиобезопасности.
Цель. Целью наблюдательного ретроспективного исследования стал сравнительный анализ влияния алоглиптина и других ССП на уровень гликированного гемоглобина (HbA1c), достижение/удержание гликемических целей и частоту сердечно-сосудистых событий.
Материал и методы. В анализ вошли данные электронных медицинских карт (ЭМК) на основании соглашения о передаче обезличенных данных пациентов с сахарным диабетом 2 типа из 129 медицинских организаций 14 субъектов Российской Федерации. На первом этапе учитывали все ЭМК, соответствующие критериям включения/невключения (n = 90 546), на втором – количественные исходы согласно псевдорандомизации по 28 исходным переменным (n = 71 932). Анализируемые ССП включали алоглиптин, метформин, другие иДПП-4, ингибиторы натрий-глюкозного котранспортера 2 (иНГЛТ-2) и производные сульфонилмочевины (ПСМ).
Результаты. Алоглиптин продемонстрировал максимальную степень снижения гликемии – на 0,5 ммоль/л (р < 0,004). В группе иНГЛТ-2 динамика изменений не достигла статистической значимости, что определило преимущество алоглиптина (p = 0,0002). На фоне алоглиптина отмечалось максимальное снижение уровня HbA1c (-0,8%; р < 0,0001) в отсутствие такового в группах других иДПП-4 и иНГЛТ-2. К окончанию наблюдения доли пациентов с целевым значением HbA1c составили 85% в группе алоглиптина, 63% в группе ПСМ, 67% в группе метформина и 38% в группе иНГЛТ-2. Алоглиптин обеспечивал удержание гликемического контроля чаще, чем другие иДПП-4 (p = 0,01). Отмечено превосходство алоглиптина относительно ПСМ (p = 0,007) и метформина (p = 0,03). При анализе безопасности в группе алоглиптина регистрировалось наименьшее число неблагоприятных событий, включая острые нарушения мозгового кровообращения, острый инфаркт миокарда и другие значимые кардиоваскулярные события. Наибольшее их число было в группе ПСМ. Гипогликемия фиксировалась только в группах ПСМ и метформина.
Выводы. Алоглиптин продемонстрировал преимущество перед другими ССП в отношении влияния на уровень HbA1c, достижение/удержание гликемических целей и кардиобезопасности.


Введение
Сахарный диабет (СД) представляет собой хроническое прогрессирующее заболевание, распространенность которого в мире неуклонно возрастает [1–3]. Согласно данным экспертов Международной диабетической федерации, в 2021 г. СД был диагностирован у 537 млн человек в возрасте от 20 до 79 лет. К 2030 г. глобальное бремя СД может составить 643 млн человек, к 2045 г. – 783 млн. Увеличение продолжительности жизни населения тесно связано с ростом заболеваемости СД 2 типа, частота выявления которого во взрослой популяции составляет 90–95% [1–3]. В России, согласно результатам первого национального эпидемиологического исследования NATION, распространенность СД 2 типа составила 5,4%. При этом у 54% пациентов заболевание было диагностировано впервые [4].
В 2021 г. СД стал причиной 6,7 млн смертей [5]. Эксперты Всемирной организации здравоохранения указывают, что с 2000 по 2019 г. смертность от диабета увеличилась на 3% [3].
Больные СД относятся к группе риска развития сердечно-сосудистых заболеваний (ССЗ). Установлено, что в данной популяции он в два – четыре раза выше, чем в общей популяции [6]. Формирование нестабильных атеросклеротических бляшек, характерное для СД, увеличивает риск развития острого коронарного синдрома, который имеет более пессимистический прогноз у пациентов с диабетом по сравнению с лицами с нормогликемией. Так, смертность при остром коронарном синдроме у больных СД 2 типа в три раза выше [1]. Макроангиопатия становится причиной смерти более 60% страдающих СД 2 типа [6].
Закономерно повышается интерес к сердечно-сосудистой безопасности сахароснижающих препаратов (ССП) [7, 8], прежде всего в отношении гипогликемий как независимого фактора риска возникновения сердечно-сосудистых событий [7, 9]. Именно поэтому в современных рекомендациях Российской ассоциации эндокринологов на старте лечения СД 2 типа предпочтение отдается ССП с низким риском развития гипогликемий [10, 11].
К сахароснижающим препаратам с низким риском гипогликемий относятся ингибиторы дипептидилпептидазы 4 (иДПП-4), или глиптины [1, 7, 9]. Плейотропные эффекты глиптинов определяют их кардиобезопасность. Препараты данной группы могут быть востребованы у пациентов с высоким сердечно-сосудистым риском [1, 2, 9].
Алоглиптин – новый высокоселективный иДПП-4, обеспечивающий значительное снижение постпрандиальной концентрации глюкозы у пациентов с СД 2 типа [9, 12, 13]. Алоглиптин уменьшает гипертрофию миокарда, интерстициальный фиброз и диастолическую дисфункцию, хорошо переносится пациентами, в том числе пожилыми, а также страдающими почечной и/или печеночной недостаточностью [2].
В рамках 26-недельного рандомизированного контролируемого исследования было показано, что у 329 пациентов, не достигших целевых значений гликированного гемоглобина (HbA1c) ≤ 7,0%, монотерапия алоглиптином в дозах 12,5 и 25 мг способствовала его снижению на -0,56 и -0,59% соответственно по сравнению с приемом плацебо (р < 0,001). Положительная динамика отмечалась уже к четвертой неделе лечения (р < 0,001). Уменьшение уровня глюкозы плазмы натощак регистрировалось через неделю и сохранялось на протяжении 26 недель наблюдения [12, 14, 15].
В 2013 г. было завершено многоцентровое рандомизированное двойное слепое исследование EXAMINE, основной целью которого стала оценка сердечно-сосудистого риска, связанного с применением новых ССП у пациентов с СД 2 типа. В исследовании приняло участие 5380 человек из 49 стран. При анализе трехкомпонентной конечной точки больших нежелательных сердечно-сосудистых событий (Major Adverce Cardiovascular Events – MACE), которая включала смертельные исходы от сердечно-сосудистых причин, нефатальный острый инфаркт миокарда (ОИМ) и нефатальный инсульт (острое нарушение мозгового кровообращения (ОНМК)), частота развития событий в группе алоглиптина составила 11,3%, в группе плацебо – 11,8% (р < 0,001) [9, 13, 16, 17].
В рамках крупного постмаркетингового многоцентрового двойного слепого рандомизированного исследования ENDURE анализировались продолжительность сохранения эффекта и безопасность комбинации алоглиптина и метформина по сравнению с комбинацией глипизида и метформина. В исследовании приняли участие 2639 пациентов. Через 104 недели исследования уровень глюкозы плазмы натощак снизился на 0,05 и 0,18 ммоль/л у получавших алоглиптин в дозах 12,5 и 25 мг и увеличился на 0,30 ммоль/л у принимавших глипизид (р < 0,001). Снижение концентрации HbA1c достигло 0,68, 0,72 и 0,59% в группах алоглиптина в дозах 12,5 и 25 мг и глипизида соответственно. Среднее изменение массы тела составило -0,68, -0,89 и +0,95 кг соответственно (р < 0,001). Частота развития подтвержденных MACE – 0,7, 0,9 и 1,3% соответственно [9, 12, 13, 18].
С мая 2016 г. по август 2018 г. на базе 53 российских клинических центров было проведено многоцентровое неинтервенционное проспективное наблюдательное исследование ENTIRE с участием 1399 пациентов с СД 2 типа. Целевых показателей HbA1c < 7,0% достигли 52% получавших алоглиптин в течение шести месяцев. Среднее изменение показателя составило -1,2 ± 1,0% [19]. Дополнительный анализ результатов в рамках проспективного неинтервенционного наблюдательного исследования ENTIRE верифицировал снижение HbA1c более чем на 0,5% у 73,5% больных. Уменьшение массы тела зафиксировано у 76,6% в среднем на 2,6 ± 4,2 кг, а уровня липопротеинов низкой плотности (ЛПНП) – у 74,7%. Снижение артериального давления (АД) отмечено у 59% пациентов. Систолическое артериальное давление (САД) в среднем снизилось на 5,9 ± 0,3 мм рт. ст., диастолическое артериальное давление (ДАД) – на 2,7 ± 0,2 мм рт. ст. [20].
В рамках систематического обзора, проведенного Н.А. Петуниной и соавт., было показано, что у пациентов с СД 2 типа с высокой вероятностью MACE и сохраненной функцией почек алоглиптин снижал риск достижения трехкомпонентных (отношение риска (ОР) 0,81 при 95%-ном доверительном интервале (ДИ) 0,65–0,99) и четырехкомпонентных (ОР 0,82 (95% ДИ 0,65–0,99)) MACE, а также смертей от сердечно-сосудистых причин (ОР 0,61 (95% ДИ 0,41–0,92)) [21]. Трехкомпонентная конечная точка MACE включала оценку частоты летальных исходов от сердечно-сосудистых причин, нефатального ОИМ и нефатального инсульта (ОНМК), четырехкомпонентная – дополнительно оценку частоты госпитализаций по поводу нестабильной стенокардии.
Во всех исследованиях применение алоглиптина характеризовалось благоприятным профилем безопасности и минимальным риском развития гипогликемий [9, 12–15, 18–20].
Таким образом, для алоглиптина была показана высокая эффективность при СД 2 типа, хороший профиль безопасности, в том числе кардиологической, и низкий риск развития гипогликемий.
Хорошие перспективы алоглиптина у коморбидных пациентов с СД 2 типа генерируют проведение исследований в разных субпопуляциях [22, 23].
Целью настоящей публикации стало представление результатов другого неинтервенционного исследования, проводившегося в России для сравнения влияния алоглиптина и других доступных к настоящему времени пероральных ССП на уровень HbA1c, достижение и удержание целевой гликемии, а также на частоту сердечно-сосудистых осложнений.
Материал и методы
Наблюдательное ретроспективное сравнительное исследование эффективности и безопасности алоглиптина и других пероральных ССП у пациентов с СД 2 типа было проведено с использованием электронных медицинских карт (ЭМК).
Материалом исследования стала информация, накопленная на платформе интегральной аналитики к 5 сентября 2022 г. Это были деперсонифицированные ЭМК 10 509 204 пациентов, проходивших обследование и лечение в 129 медицинских организациях 14 субъектов России.
Формирование базы данных из обезличенных электронных медицинских записей, обработку результатов и статистический анализ генерировал внешний провайдер ООО «К-Скай». Для извлечения информации из ЭМК использовали структурированные запросы к базе данных, язык PL/pgSQL, методы NLP, поиск по тексту (регулярные выражения), алгоритмический поиск по условию (параметры лабораторных данных), группировку и агрегацию формализованных данных разных типов (текстовые, численные), парсинг данных (методы сводных таблиц). Обработка результатов базировалась на применении библиотеки языка Python.
Исследование состояло из двух этапов. На первом этапе в анализ включались ЭМК всех пациентов, соответствующих критериям включения/невключения. На втором этапе для устранения систематических различий при анализе количественных исходов в сравниваемых группах применялась псевдорандомизация (propensity score matching) по 28 исходным переменным (табл. 1 и 2).
Время пребывания под наблюдением определялось как количество лет от индексной даты до даты первого возникновения события или до даты окончания наблюдения, в зависимости от того, что произошло раньше.
Обезличенные медицинские записи из лечебно-профилактических медицинских учреждений включались в анализ на основании соглашения о передаче обезличенных данных. Критериями включения записей ЭМК в исследование стали:
- возраст пациента ≥ 18 лет;
- подтвержденный диагноз СД 2 типа;
- факт назначения пероральных ССП.
Из анализа исключались ЭМК пациентов с установленным диагнозом СД 1 типа.
С целью проведения ретроспективного сравнительного анализа эффективности и безопасности алоглиптина и других схем лечения СД 2 типа в условиях реальной клинической практики в России ЭМК были распределены на пять групп в зависимости от типа сахароснижающей терапии: алоглиптин, метформин, иДПП-4, ингибиторы натрий-глюкозного котранспортера 2 (иНГЛТ-2) и производные сульфонилмочевины (ПСМ). Препараты назначались в соответствии с рутинной медицинской практикой. Терапия за время наблюдения не менялась.
В рамках исследования анализировались антропометрические и демографические данные ЭМК пациентов: пол, возраст, вес, индекс массы тела (ИМТ) и окружность талии. Проводились регистрация и анализ сопутствующей терапии: прием антигипертензивных и гиполипидемических средств, антиагрегантов и антикоагулянтов, а также других препаратов, показанных при ССЗ. Анализируемые в рамках проекта клинические и лабораторные/функциональные переменные представлены в табл. 1.
С целью всестороннего анализа эффективности и безопасности алоглиптина по сравнению с таковыми других ССП дополнительно были рассчитаны следующие параметры:
- функциональный класс пациентов;
- удержание гликемического контроля в зависимости от функционального класса пациентов;
- количество ССП в схеме лечения;
- время наблюдения в месяцах;
- время от постановки диагноза СД 2 типа до начала сахароснижающей терапии в месяцах.
Функциональный класс присваивался в зависимости от наличия определенных критериев [11]:
- первый класс – молодой возраст (до 44 лет), отсутствие атеросклеротических сердечно-сосудистых заболеваний (АССЗ);
- второй класс – средний возраст (45–59 лет) и отсутствие АССЗ или молодой возраст и наличие АССЗ;
- третий класс – средний возраст и наличие АССЗ или пожилой возраст (≥ 60 лет), отсутствие АССЗ и функционально независимые;
- четвертый класс – пожилой возраст, наличие АССЗ и функционально независимые;
- пятый класс – пожилой возраст, функционально зависимые.
С целью повышения релевантности данных на втором этапе исследования с помощью методики propensity score matching в соответствии с 28 анализируемыми параметрами были подобраны пары алоглиптин/ССП:
- алоглиптин и другие иДПП-4 – 151 пара пациентов;
- алоглиптин/иНГЛТ-2 – 236 пар;
- алоглиптин/ПСМ – 151 пара;
- алоглиптин/метформин – 151 пара пациентов.
В отношении алоглиптина/иНГЛТ-2 отобрано 26 параметров. Параметры «HbA1c» и «удержание гликемического контроля» не были включены из-за их малого объема в группе иНГЛТ-2.
Количественные показатели представлены в виде среднего арифметического, 95%-ного ДИ, стандартного отклонения, медианы, межквартильного диапазона, минимума и максимума.
По результатам исследования проводилась проверка статистических гипотез. Для проверки в случае нормального распределения количественных признаков использовался t-тест Стьюдента. В отсутствие нормального распределения признака сравнение в независимых выборках осуществляли с использованием непараметрического U-критерия Манна – Уитни. В зависимых выборках применяли критерий Вилкоксона. Для оценки нормальности распределения количественных переменных использовали тест Шапиро – Уилка.
Для оценки справедливости нулевой гипотезы (наличие связи между категориальными признаками) применяли хи-квадрат Пирсона. В случае значений ожидаемого явления менее десяти использовали точный критерий Фишера. Связь между двумя количественными показателями при нормальном распределении устанавливали с помощью критерия корреляции Пирсона, при ненормальном распределении – коэффициента ранговой корреляции Спирмена.
Результаты
Пациенты
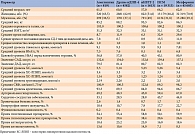
На первом этапе в исследование было включено 7 479 153 медицинских записи ЭМК 90 546 пациентов. Основная выборка состояла из данных 71 932 больных, терапия которых не изменилась за все время наблюдения. Исходные характеристики пациентов основной группы представлены в табл. 2.
В зависимости от индексной сахароснижающей терапии больные были распределены в пять групп (табл. 3).
При подборе методом propensity score matching пар сравнения алоглиптина с группой других иДПП-4 статистически значимые различия регистрировались только в отношении возраста пациентов. Так, средний возраст больных был выше в группе алоглиптина. Подобранные по 26 параметрам группы сравнения алоглиптина и иНГЛТ-2 статистически достоверно различались по времени наблюдения, возрасту, уровню глюкозы в крови, ИМТ, ДАД, скорости клубочковой фильтрации (СКФ), полу, числу пациентов с артериальной гипертензией, ССЗ, гипертрофии левого желудочка и функциональному классу. Исходные уровни глюкозы в крови были достоверно выше в группе иНГЛТ-2, чем в группе алоглиптина, – 9,6 против 9,0 ммоль/л.
Для сравнения группы алоглиптина с группой ПСМ были отобраны пары, сопоставимые по всем 28 оцененным характеристикам. Пары статистически достоверно не различались ни по одному параметру. Отобранные для сравнения групп алоглиптина и метформина пары статистически достоверно различались только по уровню общего холестерина (ХС). Он был выше в группе метформина.
Длительность терапии на первом этапе исследования составила 8,7 (алоглиптин), 11,9 (иДПП-4), 6,3 (иНГЛТ-2), 32,9 (ПСМ) и 29,6 (метформин) месяца. На втором этапе исследования данный показатель был равен 12,7, 14,4, 7,7, 12,6 и 12,4 месяца соответственно.
Исходно в каждой группе ССП применялись в режиме монотерапии. К окончанию наблюдения среднее количество ССП в схеме терапии составило 1,8 (алоглиптин), 2,0 (иДПП-4), 1,7 (иНГЛТ-2) и 1,6 (ПСМ) соответственно. В группе метформина сохранялся режим монотерапии.
Эффективность
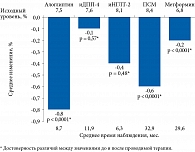
В рамках проведенного исследования алоглиптин продемонстрировал максимальную степень снижения средней гликемии – на 0,5 ммоль/л (р < 0,004) (рис. 1). Следует отметить, что при сравнении группы алоглиптина с группой иНГЛТ-2 было отмечено статистически достоверное различие по уровню глюкозы в крови в пользу исследуемого ССП (p = 0,0002). При этом в группе иНГЛТ-2 динамика показателя не достигла порога статистической значимости.
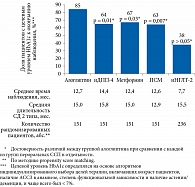
Анализ динамики уровня HbA1c показал, что в группах получавших алоглиптин отмечалось максимальное снижение показателя. Среднее изменение уровня HbA1c относительно исходных значений составило -0,8% (р < 0,0001) (рис. 2). Снижение HbA1c не достигло порога статистической значимости в группах иДПП-4 и иНГЛТ-2. Доля пациентов с целевым уровнем HbA1c к окончанию наблюдения в группе принимавших алоглиптин составила 85% (рис. 3). Наименьшее значение было получено для группы иНГЛТ-2 – 38%. При включении в терапию СД 2 типа ПСМ и метформина доля пациентов с целевым значением HbA1c составила 63 и 67% соответственно.
Удержание гликемического контроля достигалось достоверно чаще в группе алоглиптина по сравнению с группой других иДПП-4 (p = 0,01). Отмечено статистически достоверное различие по количеству пациентов с удержанием гликемического контроля в группах алоглиптина по сравнению с группой ПСМ (p = 0,007) и группой метформина (p = 0,03) в пользу исследуемого ССП.
Безопасность
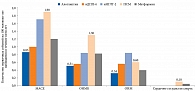
При оценке частоты сердечно-сосудистых событий на фоне терапии разными классами пероральных ССП установлено, что в группе алоглиптина она была наименьшей, включая ОНМК, ОИМ и MACE (рис. 4). Наибольшее число неблагоприятных событий, включая сердечно-сосудистую смерть, смерть от всех причин, ОНМК и MACE, зафиксировано в группе ПСМ. Гипогликемия зафиксирована только в группах ПСМ и метформина.
Обсуждение результатов
Впервые в Российской Федерации было проведено исследование по оценке клинических преимуществ терапии алоглиптином перед другими ССП у пациентов с СД 2 типа в условиях реальной клинической практики на основе анализа большой базы данных ЭМК. Анализ большой популяции пациентов (n = 71 932) из 14 субъектов России, проводившийся с учетом широкого спектра переменных и подбором пар для сравнения по 28 параметрам, обеспечивает высокую репрезентативность полученных результатов.
В ходе исследования подтверждено наличие клинических преимуществ алоглиптина перед другими иДПП-4, ПСМ и метформином в отношении удержания гликемического контроля. В рамках проведенного ретроспективного анализа ЭМК статистически достоверное уменьшение уровня глюкозы в крови отмечалось в группах алоглиптина, иДПП-4, ПСМ и метформина. Отсутствие статистической значимости динамики параметра в группе иНГЛТ-2, вероятно, обусловлено коротким периодом наблюдения (в среднем 6,3 месяца). Наибольшее снижение среднего уровня глюкозы в крови после лечения зафиксировано в группе алоглиптина (на 0,5 ммоль/л), наименьшее – в группе метформина (на 0,14 ммоль/л). В группе алоглиптина также отмечалось наибольшее изменение среднего значения HbA1c – -0,8%. Это соответствует опубликованным ранее результатам клинических исследований.
Адекватно подобрать пары для сравнения групп алоглиптина и иНГЛТ-2 не удалось, поэтому достоверно судить о преимуществах того или иного препарата не представляется возможным.
Отсутствие статистически значимого различия между группой алоглиптина и группами ПСМ и метформина по уровням глюкозы в крови и HbA1c может быть связано с небольшим периодом наблюдения, который в группах сравнения не превышал 14 месяцев, что, скорее всего, недостаточно для выявления статистически значимой разницы в терапевтическом эффекте различных видов сахароснижающей терапии.
Статистически значимых различий по количеству неблагоприятных событий в группах сравнения не выявлено.
Таким образом, ретроспективный анализ ЭМК для оценки распространенности, характеристик пациентов, текущих схем лечения и клинических исходов СД 2 типа в условиях российской реальной клинической практики продемонстрировал ряд преимуществ алоглиптина. Результаты могут быть использованы в качестве научной основы при выборе оптимальных режимов сахароснижающей терапии.
Ограничения
Среди ограничений исследования следует отметить следующие:
небольшое время наблюдения: в группах алоглиптина, иДПП-4, метформина и ПСМ – 12 месяцев, в группе иНГЛТ-2 – около полугода;
недостаточное количество данных по некоторым показателям, в частности при подборе пар во всех группах сравнения из-за недостаточного количества данных не были учтены такие важные параметры, как статус в отношении курения и уровень ХС-ЛПНП, уровень HbA1c и удержание гликемического контроля не были включены в сравнение групп алоглиптина и иНГЛТ-2 из-за их недостаточности в группе иНГЛТ-2, не удалось адекватно подобрать пары сравнения групп алоглиптина и иНГЛТ-2;
в связи с ретроспективным дизайном исследования невозможно точно оценить контроль за соблюдением пациентами рекомендаций.
Заключение
- При терапии алоглиптином отмечалось максимальное абсолютное снижение уровня HbA1c от исходного – на 0,8% (р < 0,0001).
- Терапия алоглиптином обеспечивала наибольшее среднее снижение уровня глюкозы в крови, определяемого в любое время суток (на 0,5 ммоль/л), по сравнению с группами других иДПП-4, иНГЛТ-2, ПСМ и метформина.
- Терапия алоглиптином обеспечивала лучшее удержание гликемического контроля (> 80%) по сравнению с другими иДПП-4, ПСМ и метформином.
- Терапия алоглиптином ассоциировалась с меньшей частотой развития ОНМК, ОИМ и MACE, чем применение иДПП-4, иНГЛТ-2, ПСМ и метформина.
- Случаи развития гипогликемии регистрировались только в группах ПСМ и метформина.
V.V. Fadeev, Corresponding member of the RASci., MD, PhD, Prof.
I.M. Sechenov First Moscow State Medical University
Contact person: Valentin V. Fadeev, walfad@mail.ru
The dipeptidyl peptidase type 4 (iDPP-4) inhibitor alogliptin is a promising hypoglycemic drug (HGD) with a low risk of hypoglycemia and significant cardiac safety.
Purpose. The purpose of this observational retrospective trial was to compare the effects of alogliptin and other HGDs on glycated hemoglobin (HbA1c), achievement/maintenance of glycemic targets, and incidence of cardiovascular events.
Material and methods. The analysis included data from electronic medical records (EMR; based on the Anonymous Data Transfer Agreement) of patients with type 2 diabetes mellitus from 129 medical organizations in 14 constituent departments of the Russian Federation. The first part were included all EMRs (n = 90 546) that met the inclusion/exclusion criteria; at the second one were analyzed quantitative outcomes according to pseudo-randomization for 28 initial variables (n = 71 932). There were analyzed alogliptin, metformin, iDPP-4, sodium-dependent glucose transporter type 2 inhibitors (iSGLT-2), and sulfonylurea derivatives (SUMs).
Results. The maximal glycemic reduction were 0.5 mmol/l (p < 0.004) on alogliptin. There was not significance decrease in the iSGLT-2; therefore alogliptin had been excellence (p = 0.0002). On alogliptin, there was a maximum decrease in HbA1c (-0.8%; p < 0.0001) without changes in the groups of other iDPP-4 and iSGLT-2. By the end of follow-up, the proportions of patients with targeted HbA1c were 85% (alogliptin), 63% (SUMs), 67% (metformin), and 38% (iSGLT-2). Alogliptin provided retention of glycemic control more often than other iDPP-4 (p = 0.01). The advantage of alogliptin relative to SUMs (p = 0.007) and metformin (p = 0.03) was noted. In the safety analysis, the alogliptin group had the fewest adverse events, including acute cerebrovascular accident, acute myocardial infarction, and other significant cardiovascular events. The greatest number of adverse events was in the SUMs group. Hypoglycemia occurred only in the SUMs and metformin groups.
Conclusions. Alogliptin has been shown to be superior to other in terms of HbA1c, achievement/maintenance of glycemic targets, and cardiac safety.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.