Современные методы лечения сезонной аллергии: роль антигистаминных препаратов
- Аннотация
- Статья
- Ссылки
- English


Введение
Последние десятилетия во многих странах мира отмечается существенный рост распространенности аллергических заболеваний. К аллергическим заболеваниям, часто развивающимся в весенне-летний и осенний периоды, относится поллиноз. Его распространенность в популяции колеблется от 1,6 до 40,9% [1]. Чаще болеют лица в возрасте 10–40 лет. У детей до трех лет поллиноз встречается редко. Среди детей в возрасте до 14 лет мальчики болеют в два раза чаще, чем девочки. В возрасте от 15 до 40 лет заболеванию в большей степени подвержены лица женского пола. Среди горожан заболеваемость в 4–6 раз выше, чем среди сельских жителей [2].
На показатели распространенности пыльцевой аллергии влияют климатогеографические, экологические, этнографические и диагностические факторы. Пыльцевая аллергия чаще отмечается в регионах с пышным растительным покровом, сухим и жарким климатом. Для каждой климатогеографической зоны характерны свои пыльцевые аллергены. Наиболее высокая распространенность поллиноза наблюдается в Северо-Кавказском, Поволжском и Уральском регионах России (до 80% всех больных аллергическим ринитом). В популяционном исследовании, проведенном в Саратовской области, сезонный аллергический ринит регистрировался у 28,3% населения [3].
Поллиноз (от англ. pollen – пыльца), пыльцевая аллергия, или сенная лихорадка, – классическое аллергическое заболевание, в основе которого лежит аллергическая реакция немедленного типа. Заболевание характеризуется острым аллергическим воспалением слизистых оболочек дыхательных путей, глаз, кожи. Реже в процесс вовлекаются пищеварительная, сердечно-сосудистая, мочеполовая и нервная системы. Заболевание отличается четкой, ежегодно повторяющейся сезонностью, совпадает по времени с пылением определенных растений [2]. Поллиноз не относится к числу тяжелых заболеваний, но существенно снижает качество жизни больных, нарушает сон, негативно влияет на способность к обучению и профессиональную деятельность, а также требует от общества значительных финансовых затрат [4].
Этиология
Из более чем 700 известных видов растений только 50 могут стать причиной поллиноза. Пыльца ветроопыляемых растений, провоцирующая симптомы поллиноза, должна быть легкой и летучей, небольших размеров (до 35 мкм), обладать выраженной антигенной активностью. Большое значение имеет концентрация пыльцы в воздухе, она должна составлять 10–50 пыльцевых зерен на 1 см3 [5].
В средней полосе и Европейской части России отмечаются три периода поллиноза, основным проявлением которого становится аллергический риноконъюнктивит. Весенний – с середины апреля до конца мая связан с пылением деревьев (береза, дуб, орешник, ольха, клен, ясень, платан, вяз, тополь). Летний – с начала июня до конца июля обусловлен пылением луговых злаковых трав (тимофеевка, овсяница луговая, ежа сборная, пырей, мятлик луговой, костер, лисохвост, райграс), культивируемых злаков (рожь, кукуруза). Третий пик – летне-осенний – с конца июля до конца октября связан с цветением сорных трав (полынь, лебеда, амброзия, подсолнечник). Несмотря на то что симптомы заболевания беспокоят пациентов ежегодно в одно и то же время, сроки цветения могут варьироваться в разные годы в зависимости от погодных условий.
Между аллергенами различных видов пыльцы имеется сходство. Антигены присутствуют не только в пыльцевых зернах, но и в других частях растений (семена, листья, стебли, плоды). У больных поллинозом развиваются перекрестная пищевая аллергия и непереносимость препаратов растительного происхождения (табл. 1) [5].
Патогенез
Механизм развития поллиноза – это классический пример немедленной IgE-обусловленной аллергической реакции. Главными участниками аллергического воспаления в слизистой оболочке носа, бронхиального дерева, конъюнктивы, обусловленного взаимодействием аллергена со специфическими IgE-антителами, являются тучные клетки, эозинофилы, лимфоциты, эпителиальные и эндотелиальные клетки. Аллергенспецифические IgE-антитела, образующиеся в избытке при контакте с аллергеном у предрасположенных к атопии лиц, фиксируются на высокоаффинных рецепторах к ним на тучных клетках. Это приводит к сенсибилизации слизистой оболочки носа, конъюнктивы. Следующий контакт с аллергеном и связывание последнего с фиксированными на тучных клетках IgE-антителами способствуют активации тучных клеток и секреции медиаторов аллергического воспаления: гистамина, триптазы, кининов, цистеиниловых лейкотриенов С4, D4, E4, фактора активации тромбоцитов. Воздействие медиаторов на эндотелиальные клетки сосудов и нейрорецепторы слизистой оболочки носа, конъюнктивы приводит к возникновению клинических симптомов поллиноза. Это ранняя фаза аллергического ответа. Спустя 6–8 часов развивается поздняя фаза аллергической реакции, не требующая дополнительного контакта с аллергеном. Главными участниками в поздней фазе аллергической реакции являются гистамин, лейкотриены, эозинофильные белки, цитокины.
Гистамин активно участвует в формировании как ранней, так и поздней фазы аллергической реакции, обусловливая подавляющее большинство клинических проявлений поллиноза. Будучи важнейшим медиатором аллергической реакции немедленного типа, гистамин обладает широким спектром биологической активности. Его действие осуществляется за счет активации клеточных поверхностных специфических Н1-, Н2-, Н3-, Н4-рецепторов. Основные эффекты гистамина в результате активации Н1-рецепторов выражаются в повышении проницаемости сосудов, отеке, гиперсекреции, спазме гладкой мускулатуры. Именно эти эффекты гистамина блокируются антигистаминными препаратами [6].
Клинические проявления
К наиболее частым проявлениям поллиноза относятся аллергический ринит (АР) − 95–98%, аллергический конъюнктивит (АК) – 91–95%, пыльцевая бронхиальная астма (БА) – 30–40% [2, 5].
Для поллиноза характерны сезонность и острые, рецидивирующие клинические проявления. Тяжесть сезонного обострения заболевания зависит от концентрации пыльцы в воздухе, длительности пыльцевого сезона, степени индивидуальной чувствительности.
Клиническому течению поллиноза присущ ряд особенностей:
- сезонность, связанная с периодом цветения растений;
- тесная связь с пребыванием в определенной местности;
- сочетание с лекарственной аллергией к препаратам растительного происхождения;
- сочетание с перекрестной пищевой аллергией;
- влияние погоды на течение поллиноза (обострение симптомов в сухую, солнечную, ветреную погоду, тогда как в сырую, дождливую погоду пациенты испытывают некоторое облегчение, что обусловлено снижением концентрации пыльцы в воздухе);
- наличие в период клинических проявлений поллиноза синдрома синергичной аллергии (клинические проявления возникают на другие группы аллергенов, на которые пациенты реагируют вне сезона пыления);
- обострение в сезон пыления хронических заболеваний (ишемическая болезнь сердца, язвенная болезнь и др.);
- асептичность (если не присоединится вторичная инфекция);
- приступообразность (наиболее выраженные проявления в утренние и дневные часы, когда в воздухе сконцентрировано максимальное количество пыльцы).
Наиболее типичное проявление поллиноза – риноконъюнктивальный синдром: зуд и покраснение глаз, ощущение инородного тела в глазах, светобоязнь, слезотечение, в тяжелых случаях блефароспазм. Одновременно имеют место зуд в носу, носоглотке, ушных проходах, профузный насморк, приступы чихания, затруднение носового дыхания, чаще двустороннее, различной интенсивности, гиперемия и мацерация кожи преддверия и крыльев носа, обонятельные расстройства (аносмия или гипоосмия). В аллергическое воспаление могут вовлекаться пазухи носа, носоглотка, слуховые трубы, гортань. Как следствие – развитие синусита, евстахиита, фарингита, ларингита [2, 7].
Аллергический ринит, относящийся к частым проявлениям поллиноза, классифицируется по форме, характеру, тяжести течения, стадии заболевания.
Формы АР:
- сезонный. Возникает при сенсибилизации к пыльцевым и грибковым аллергенам: пыльце деревьев, злаковых и сорных трав, спорам грибов Cladosporium, Penicillium, Alternaria, Aspergillus и др.;
- круглогодичный. Развивается у пациентов с сенсибилизацией к аллергенам клещей домашней пыли, библиотечной пыли, эпидермальным аллергенам животных и птиц, инсектным аллергенам, аллергенам плесневых грибов, пищевых продуктов и лекарственных препаратов при их постоянном приеме, профессиональным аллергенам.
В соответствии с международными согласительными документами по АР (EAACI (European Academy of Allergy and Clinical Immunology – Европейская академия аллергологии и клинической иммунологии)/WAO (World Allergy Organization – Всемирная организация здравоохранения) ARIA (Allergic Rhinitis and its Impact on Asthma – Аллергический ринит и его влияние на астму) 2008, 2010), АР классифицируют:
- по характеру течения: интермиттирующий (симптомы беспокоят менее четырех дней в неделю или менее четырех недель в году), персистирующий (симптомы беспокоят более четырех дней в неделю или более четырех недель в году);
- тяжести течения: легкая степень (незначительные клинические проявления болезни, не нарушающие дневную активность и сон), средняя степень (симптомы нарушают сон, препятствуют работе, учебе, занятиям спортом, качество жизни существенно снижается), тяжелая (симптомы настолько выражены, что пациент в отсутствие соответствующего лечения не может нормально работать, учиться, заниматься спортом, проводить досуг, спать ночью);
- стадии течения (стадия обострения и стадия ремиссии) [8].
При прогрессирующем течении поллиноза в среднем спустя 3–5 лет от начала заболевания часто формируется БА, для которой характерна сезонность проявлений. В большинстве случаев БА сочетается с аллергическим риноконъюнктивитом, но у 4% пациентов встречается как изолированный симптом поллиноза. Для изолированной БА характерно тяжелое течение, формирование астматических статусов.
Около 20% пациентов, страдающих поллинозом, отмечают в сезон пыления причинно-значимых растений головные боли, резкую слабость, потливость, расстройства сна в виде бессонницы или сонливости, раздражительность и плаксивость, ознобы, гипертермию, повышенную утомляемость. Различные сочетания описанных симптомов составляют астенический синдром, обусловленный так называемой пыльцевой интоксикацией. Указанные симптомы наблюдаются при тяжелом течении поллиноза при массивной концентрации пыльцы в воздухе и поддаются терапии глюкокортикостероидами (ГКС), антигистаминными препаратами (АГП) [1, 7].
У ряда лиц наблюдаются кожные проявления аллергии: контактная крапивница, атопический и контактный дерматит. Контактная крапивница характеризуется четкой сезонностью и в единичных случаях может быть единственным клиническим проявлением поллиноза. Контактный аллергический дерматит – редкое проявление поллиноза. Он может возникнуть на открытых участках кожных покровов при контакте с листьями или стеблями растений и проявляется гиперемией кожи с последующими везикулезными высыпаниями на пораженных участках [5]. К клиническим проявлениям перекрестной реактивности относятся синдром оральной аллергии, гастроинтестинальные симптомы, острая крапивница, ангиоотеки и анафилактический шок.
Синдромом оральной аллергии страдают около 40–70% больных поллинозом. Пациенты жалуются на зуд, покалывание и отек губ, языка, неба, глотки, ощущение кома в горле при употреблении в пищу перекрестно-реагирующих продуктов (табл. 1). Гастроинтестинальные симптомы встречаются реже: у больных могут возникать тошнота, боли в животе, кишечные колики, рвота или диарея. Такие реакции возможны и вне сезона пыления. Подобные аллергические состояния могут угрожать жизни пациентов. Это необходимо учитывать при ведении данной группы больных.
Изменения со стороны сердечно-сосудистой и нервной систем носят функциональный характер и не регистрируются вне периода цветения. Сердечно-сосудистые изменения, обусловленные пыльцевой аллергией, характеризуются тахикардией, приглушенными тонами сердца, систолическим шумом на верхушке, повышением артериального давления. Описаны проявления поллиноза в виде пыльцевого аллергического миокардита. К редким проявлениям поллиноза относится поражение урогенитального тракта (вульвовагинит, уретрит, цистит, нефрит) [2].
Диагностика
Поздняя диагностика поллиноза приводит к развитию осложнений, ухудшает прогноз заболевания, снижает качество жизни пациентов. В России только 18% пациентов направляются к специалисту в течение первого года после выявления симптомов сезонного АР. В 30% случаев интервал между появлением симптомов и установлением диагноза составляет два года, в 43% − три года, в 10% случаев – четыре года и более [9].
Обследование пациентов с поллинозом включает:
- сбор данных аллергологического анамнеза, который имеет первостепенное значение в диагностике поллиноза (сезонность проявлений, зависимость от погодных условий, пребывания на улице, за городом, смена места жительства или климата в сезон клинических проявлений, непереносимость ряда пищевых продуктов, а также препаратов растительного происхождения, наследственная предрасположенность) [2, 5];
- осмотр, позволяющий установить типичную клиническую картину заболевания;
- выполнение передней риноскопии и эндоскопического исследования;
- проведение специфической аллергологической диагностики, включающей постановку кожных проб с аллергенами, определение специфических IgE-ангител, выпонение назального провокационного теста со специфическими аллергенами.
Все эти методы специальной диагностики проводятся врачами аллергологами-иммунологами в специально оборудованных аллергологических кабинетах.
Кожные пробы (prick-тесты, скарификационные и внутрикожные) проводятся в фазу ремиссии аллергического заболевания, после отмены АГП и служат уникальным инструментом выявления причинно-значимых аллергенов при условии правильного выполнения и оценки результатов. При невозможности проведения кожного тестирования, трудностях интерпретации последнего, а также в случаях, когда не удается выявить «виновный» аллерген с помощью кожных проб, определяют специфические IgE в сыворотке крови больных. Основными методами определения уровня общего и специфического IgE в практике клинико-диагностических лабораторий признаны радиоизотопный, хемилюминесцентный и иммуноферментный. Последние годы применяется молекулярная аллергодиагностика с использованием тест-системы ImmunoCAP, которая сфокусирована на разделении истинной аллергии и перекрестной реактивности. Молекулярная аллергодиагностика считается диагностическим подходом третьей линии после сбора анамнеза (первая линия), выполнения кожных тестов с аллергенами и определения аллергенспецифических IgE (вторая линия), если исследований первого и второго уровня недостаточно для точного установления диагноза.
Результаты кожных и лабораторных тестов следует обязательно сопоставлять с клиническими симптомами заболевания, поскольку наличие сенсибилизации к аллергенам не всегда сопровождается клиническими проявлениями болезни. В случае расхождения между данными аллергологического анамнеза и результатами кожного тестирования проводят провокационные тесты с аллергенами (назальный, ингаляционный, конъюнктивальный) [10].
При диагностике поллиноза целесообразно проведение:
- исследования носа. При риноскопии обнаруживаются гипертрофия слизистой оболочки носа, особенно нижних и средних носовых раковин, сужение носовых ходов, заполненных слизистыми выделениями, их цвет варьируется от синюшного до бледно-розового. Аппликационная проба с раствором адреналина гидрохлорида 0,1% демонстрирует обратимость назальной обструкции. Проведение риноскопии необходимо для дифференциальной диагностики с другими заболеваниями ЛОР-органов (синуситы, искривление перегородки носа, полипы, опухоли) [11];
- микроскопии мазка из полости носа (подтвердить наличие эозинофилов, уровень которых при АР превышает 10% общего количества клеток);
- риноманометрии – метода измерения носовых потоков и назального сопротивления, основанного на количественном измерении градиента давления и воздушного потока, которые создаются в условиях физиологического носового дыхания. Риноманометрия позволяет получить у больных поллинозом объективные доказательства обструкции носовых путей при воздействии пыльцевых аллергенов и осуществлять мониторинг проводимой терапии [1];
- офтальмоскопии (подтвердить типичную картину АК – отечность век, гиперемию и отечность конъюнктив, в тяжелых случаях блефароспазм, отделяемое скудное, чаще бесцветное, прозрачное, без патологических примесей (кровь, гной и др.)) [12];
- рентгенографии придаточных пазух носа. Может определяться пристеночное затемнение пазух носа. При длительном обострении поллиноза у больного на рентгенограмме определяется симметричное гомогенное затемнение верхнечелюстных пазух, реже решетчатого лабиринта и основных пазух;
- оценки наличия сопутствующих заболеваний (астма, синусит, ларингит, фарингит, хронический средний отит, снижение слуха, головная боль);
- оценки качества жизни (учеба, работа, нарушение сна и социальной активности). Анализируют изменение качества жизни пациентов с пыльцевой аллергией с помощью специальных вопросников PQLQ (Rhinoconjunctivitis Quality of Life Questionnare – Вопросник для оценки качества жизни при риноконъюнктивитах) и WPAI-S (Alergic-Specific Work Productivity and Activity Impairment Questionnaire – Вопросник по аллергенспецифическому нарушению работоспособности) [4];
- изучения функции внешнего дыхания с бронхолитическим тестом. Возможно выявление снижения объемных и скоростных показателей (ОФВ1, ПСВ, МОС), обратимости бронхиальной обструкции, что может свидетельствовать о наличии БА.
Профилактика
Первичная профилактика поллиноза направлена на предупреждение развития пыльцевой аллергии и включает:
- ограничение общей антигенной нагрузки;
- рациональное питание;
- использование методов физического оздоровления и закаливания;
- рациональное озеленение городов (использование неаллергенных растений);
- для родителей с атопическими заболеваниями планирование рождения ребенка вне сезона пыления.
Вторичная профилактика поллиноза, направленная на предупреждение ухудшения состояния у лиц, которые уже страдают поллинозом, предусматривает:
- обучение больного и членов его семьи способам лечения и профилактики пыльцевой аллергии;
- контроль за концентрацией пыльцы в помещении (закрытые окна и двери, кондиционер, увлажнители и очистители воздуха, водные пылесосы);
- пребывание в других климатических зонах в период цветения;
- ограничение выхода на улицу в солнечную ветреную погоду;
- исключение из диеты продуктов с перекрестными аллергенными свойствами;
- ограничение воздействия неспецифических раздражителей (лаки, краски, химикаты);
- своевременную диагностику, адекватную фармакотерапию и аллергенспецифическую иммунотерапию (АСИТ);
- избегание профилактических прививок и плановых оперативных вмешательств в период пыления растений, на пыльцу которых развивается аллергия [2].
Лечение
Основными задачами лечения поллиноза являются устранение симптомов заболевания, снижение риска развития осложнений и повышение качества жизни пациентов. Цель лечения – полный контроль над симптомами поллиноза. Для достижения указанной цели применяются:
- элиминация причинно-значимого аллергена;
- фармакотерапия;
- АСИТ;
- обучение пациента.
К специфическим методам лечения, изменяющим течение болезни, относят элиминацию аллергена и иммунотерапию аллергенами [13].
Обязательным условием выбора тактики лечения остается индивидуальный подход к каждому больному, учитывающий клинические особенности формы и тяжести патологии, а также социальные, поведенческие и психологические аспекты, существенные для данного пациента.
Элиминационные мероприятия. Степень тяжести и течение поллиноза определяются концентрацией пыльцы в воздухе. Элиминация аллергенов уменьшает выраженность проявлений поллиноза и потребность в медикаментозном лечении. При аллергии к пыльце растений пациентам в сезон цветения рекомендуется:
- ограничить время пребывания на улице, особенно в сухую ветреную погоду в утренние часы, когда концентрация пыльцы максимальна;
- пользоваться очистителями воздуха, улавливающими пыльцу растений в помещении;
- менять климатическую зону в период цветения причинно-значимых аллергенов;
- носить темные очки для уменьшения попадания пыльцы на слизистую оболочку глаз;
- по возвращении домой менять одежду, принимать душ.
Не рекомендуется:
- часто проветривать помещения на работе и дома, открывать окна машины, особенно в ранние утренние часы;
- выезжать за город или на природу;
- применять фитопрепараты, косметические средства растительного происхождения;
- проводить профилактические прививки и плановые оперативные вмешательства в период цветения причинно-значимых аллергенов [1].
В большинстве случаев полное исключение контакта с аллергеном по практическим или экологическим причинам невозможно. Тем не менее все возможные меры по уменьшению контакта с аллергеном должны быть предприняты как первый шаг в лечении поллиноза. К числу приемов элиминации аллергена, исключения его контакта со слизистой оболочкой полости носа относится ирригационная терапия, включающая различные методы промывания носа и орошения буферными и солевыми растворами. Особенно важны элиминационные мероприятия для пациентов, имеющих ограничения для приема ряда фармакологических препаратов (беременные и кормящие женщины, дети раннего возраста, больные с тяжелой сопутствующей патологией).
Образовательные программы. Важную роль играют образовательные программы для пациентов. Доказано, что обучение пациентов способно изменить течение заболевания за счет улучшения контроля состояния и качества жизни.
Пациенты должны быть проинформированы о природе заболевания, причинах и механизмах, симптомах поллиноза и доступных методах лечения. Больным необходимо предоставлять информацию о способах элиминации или ограничения контакта с аллергеном, лекарственной терапии.
Аллергенспецифическая иммунотерапия. АСИТ является основным патогенетическим методом лечения аллергического риноконъюнктивита и атопической БА. Иммунотерапия аллергенами – это лечение возрастающими концентрациями и дозами аллергена, вводимого подкожно или сублингвально. Иммунотерапия аллергенами имеет принципиальные преимущества перед другими методами терапии, поскольку не воздействует на симптомы заболевания, но видоизменяет характер реагирования организма на аллерген, вмешивается собственно в патогенез заболевания и поэтому влияет на все патогенетические звенья аллергической реакции. Эффективность иммунотерапии аллергенами выражается в уменьшении продолжительности обострения, выраженности симптомов, уменьшении потребности в медикаментах как базисной, так и симптоматической терапии. АСИТ влияет на течение заболевания, предупреждая переход его легких форм в более тяжелые и трансформацию АР в БА, а также способна предотвратить расширение спектра аллергенов, к которым формируется повышенная чувствительность. АСИТ проводится только под наблюдением врача аллерголога и иммунолога [8].
Медикаментозное лечение
Фармакотерапия занимает важнейшее место в контроле над симптомами поллиноза. Объем медикаментозной терапии и выбор лекарственного средства зависят от многообразия клинических симптомов и соматической патологии. Основу фармакотерапии составляют лекарственные средства, действие которых направлено на основные патогенетические механизмы аллергического воспаления. Сегодня в лечении поллиноза используются лекарственные препараты шести основных групп:
- пероральные и топические АГП;
- топические и системные ГКС;
- стабилизаторы тучных клеток (интраназальные и интраокулярные кромоны);
- топические и оральные деконгестанты;
- интраназальные антихолинергические средства;
- антилейкотриеновые препараты [11].
Не рекомендуются:
- АГП первого поколения (АГП I) для базисного приема в связи с седативным эффектом, негативным влиянием на когнитивные функции, астму и другие сопутствующие заболевания;
- системные ГКС (внутримышечные, пролонгированные) [4].
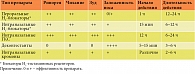
В таблице 2 представлены клинические эффекты различных фармакологических препаратов при аллергическом риноконъюнктивите.
В документе ВОЗ ARIA (2001–2010 гг.) предусмотрен принцип ступенчатой терапии в зависимости от формы и степени тяжести АР [4]. При легком течении АР назначают монотерапию неседативными Н1-блокаторами или АГП местного действия либо препараты кромогликата натрия или антилейкотриеновые препараты. При среднетяжелом течении АР, а также в отсутствие эффекта на первой ступени лечения назначают топические (назальные) ГКС. При тяжелом течении или неэффективности второй ступени терапии используют комбинацию назальных топических ГКС и неседативных пероральных АГП. В отсутствие эффекта рекомендуется увеличить дозу назальных ГКС до максимально разрешенной. При необходимости следует назначить короткий курс деконгестантов (7–10 дней) или системных ГКС (максимально до трех недель) (преднизолон 20–40 мг/сут перорально).
Лечение пыльцевой БА осуществляется по общепринятым стандартам в соответствии с рекомендациями GINA-2016 [14].
Роль АГП в лечении сезонной аллергии
В середине прошлого века были открыты разные классы гистаминовых рецепторов, доказана ответственность Н1-рецепторов за развитие симптомов аллергии. Именно поэтому особое место в лечении аллергических заболеваний занимают АГП. Их действие заключается в блокировании гистаминовых Н1-рецепторов на мембранах клеток различных тканей.
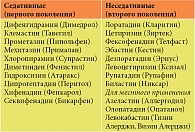
Существуют две группы АГП: первого поколения (седативные) и второго поколения (неседативные). Классификация АГП представлена в табл. 3.
АГП I имеют ряд нежелательных побочных эффектов, обусловленных их низкой специфичностью к Н1-гистаминовым рецепторам (сухость слизистых оболочек, задержка мочи, тахикардия, повышение аппетита и др.), непродолжительным действием (требуют 2–4-кратного применения), липофильностью и высоким прохождением через гематоэнцефалический барьер (выраженное седативное действие), развитием тахифилаксии (быстрое привыкание и снижение эффекта). Применение АГП I ограничивается их побочными эффектами, а также неблагоприятным, потенцирующим взаимодействием с алкоголем, психотропными и снотворными средствами. Кроме того, АГП I противопоказаны при сопутствующей БА. Некоторые АГП I обладают кардиотоксическим эффектом при передозировке, сокращают фазы быстрого сна, снижают способность к обучению и производительность труда, что неоднократно становилось причиной автомобильных катастроф, а также гибели младенцев из-за случайной или преднамеренной передозировки [4].
В соответствии с рекомендациями EAACI, GA2LEN (Global Allergy and Asthma European Network – Европейский консорциум по изучению аллергических заболеваний и бронхиальной астмы), WAO, седативные АГП I больше не должны использоваться в качестве терапии первого выбора, за исключением случаев, когда АГП второго поколения (АГП II) недоступны или преимущества их использования перевешивают риски [15]. В частности, речь идет о парентеральном введении АГП. Как известно, парентеральных форм АГП II пока нет.
АГП II являются высокоселективными блокаторами Н1-гистаминовых рецепторов. Противогистаминное действие этих препаратов проявляется быстро (в течение одного-двух часов) и продолжается до 12–24 часов. Соответственно они применяются один, максимум два раза в сутки. АГП II практически лишены или характеризуются незначительным седативным действием, которое обычно не отличается от эффекта плацебо, не влияют на холинергические и адренергические рецепторы либо такое влияние незначительно. АГП II эффективны в отношении купирования симптомов АР, аллергического конъюнктивита и крапивницы. Причем этот эффект дозозависимый [16].
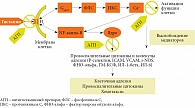
В экспериментальных исследованиях показано, что спектр фармакологической активности АГП II не ограничивается связыванием с H1-гистаминовыми рецепторами, с которыми они взаимодействуют по принципу обратных агонистов, стабилизируя Н1-рецептор в неактивном состоянии [17]. АГП подавляют высвобождение провоспалительных медиаторов (гистамина, лейкотриенов), снижают экспрессию адгезионных молекул (ICAM-1 (inter-cellular adhesion molecule 1) и Р-селектина) и некоторых цитокинов (интерлейкин (ИЛ) 4, ИЛ-6, ИЛ-8, ИЛ-13, ГМ-КСФ (гранулоцитарно-макрофагальный колониестимулирующий фактор)). Эти данные позволяют говорить о наличии у современных АГП противовоспалительного эффекта, опосредованного даун-регуляцией, то есть снижением экспрессии транскрипционных факторов, таких как ядерный фактор каппа B и активирующий протеин 1, отвечающих за синтез провоспалительных цитокинов и адгезионных молекул [18] (рис. 1). Сказанное позволяет предположить наличие у современных АГП противовоспалительного эффекта. Учитывая, что АГП II лишены недостатков своих предшественников, они могут применяться у больных АР и аллергическим конъюнктивитом, и сопутствующей БА.
Согласно федеральным клиническим рекомендациям, при сезонной форме АР профилактическая противоаллергическая терапия должна быть назначена после анализа данных о течении заболевания в предыдущий сезон (выраженность клинических проявлений, эффективность назначенных препаратов и результаты обследования) за одну-две недели до предполагаемого сезонного обострения. Учитывая особенности течения АР, наличие таких феноменов, как минимальное персистирующее воспаление и эффект прайминга, АГП II следует применять на протяжении всего периода цветения и отменять через 2–4 недели после окончания сезона пыления [8, 19].
На отечественном фармацевтическом рынке представлен широкий выбор АГП II. Особого внимания заслуживает новый оригинальный неседативный АГП для облегчения симптомов аллергического риноконъюнктивита и крапивницы – биластин. В нашей стране препарат зарегистрирован в июле 2016 г. под торговым названием Никсар®. Значимый терапевтический эффект наблюдается через час после приема препарата, антигистаминное действие сохраняется в течение 24 часов. Препарат выпускается в виде таблеток, содержащих 20 мг биластина, и рекомендован для однократного применения при симптоматическом лечении аллергического риноконъюнктивита (сезонного и круглогодичного) и крапивницы у взрослых и подростков старше 12 лет. Препарат принимают по одной таблетке за час до еды или через два часа после еды. При почечной недостаточности средней и тяжелой степени тяжести скорость элиминации биластина замедляется, что может привести к увеличению его концентрации в плазме крови. Однако изменение фармакокинетических параметров не оказывает влияния на профиль безопасности биластина, так как его концентрация в плазме крови у пациентов с почечной недостаточностью остается в пределах нормы. При печеночной недостаточности клинически значимых изменений фармакокинетических параметров биластина не происходит, поскольку в печени он метаболизируется незначительно [20]. Механизм действия препарата заключается в селективном блокировании Н1-рецепторов гистамина. Препарат снижает проницаемость капилляров, предупреждает развитие и облегчает течение аллергических реакций немедленного типа, предупреждает индуцированный гистамином спазм гладкой мускулатуры сосудов и внутренних органов. Биластин оказывает антагонистическое воздействие на Н1-гистаминовые рецепторы и не оказывает клинически значимого воздействия на рецепторы серотонина, брадикинина, лейкотриена D4, адрено- и мускариновые рецепторы. Биластин также может тормозить высвобождение гистамина, ИЛ-4 и фактора некроза опухоли из тучных клеток и гранулоцитов, что обеспечивает противовоспалительную активность препарата.
Клиническая эффективность препарата Никсар® (биластин)
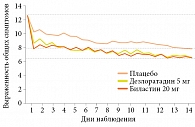
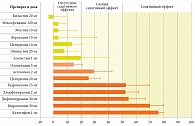
Согласно результатам клинических исследований, биластин высоко эффективен при аллергическом риноконъюнктивите. Терапевтический эффект биластина при сезонном АР оценивали в двух больших международных двойных слепых плацебоконтролируемых исследованиях с участием 1402 пациентов в возрасте от 12 до 70 лет [21, 22]. В исследованиях применялись почти идентичные дизайны, оценки эффективности и безопасности. В обоих исследованиях применяли двойной контроль: плацебо и альтернативный Н1-антигистаминный препарат второго поколения дезлоратадин [21] и цетиризин [22]. В качестве первичного исхода оценивали площадь под кривой общего счета симптомов (TSS – Total Symptom Score), учитывали назальные и неназальные симптомы. Пациенты отмечали симптомы в дневнике с 1-го по 14-й день. Назальные (заложенность, ринорея, чихание и зуд) и неназальные симптомы (глазной зуд, жжение, покраснение, ощущение инородного тела в глазу, слезотечение, зуд в ушах или области неба) ранжировали в баллах от 0 до 3: 0 – отсутствие симптомов; 1 – легкие симптомы, иногда возникающие, но не тревожащие; 2 – умеренно выраженные симптомы, которые появляются часто и беспокоят; 3 – резко выраженные симптомы, которые присутствуют постоянно и нарушают сон и работоспособность [21, 22]. Вторичными исходами служили общая оценка дискомфорта, вызванного ринитом, и общее клиническое впечатление исследователя. Дискомфорт измеряли по Визуальной аналоговой шкале (ВАШ). Общее впечатление врача основывалось на выраженности терапевтического эффекта и побочных явлений. Результаты лечения показали, что общий счет назальных симптомов − чихания, ринореи, зуда и заложенности и неназальных − повышенного слезоотделения, покраснения глаз, зуда в глазах и небе значительно снижался на фоне приема биластина. При использовании дезлоратадина (рис. 2) и цетиризина отмечалась аналогичная эффективность, но биластин отличался лучшим профилем безопасности по сравнению с цетиризином (рис. 3) [22]. Кроме того, биластин значительно уменьшал субъективный дискомфорт, связанный с риноконъюнктивитом, и достоверно улучшал качество жизни пациентов (р < 0,001) [21, 22].
Переносимость и безопасность препарата Никсар® (биластин)
Безопасность биластина оценивали у здоровых добровольцев, которые получали препарат 14 дней. Как показали результаты, препарат в дозах 20–100 мг/сут хорошо переносится, частота неблагоприятных событий не отличается от таковой при использовании плацебо.
В исследованиях с участием пациентов с аллергическим риноконъюнктивитом получены аналогичные результаты.
Биластин метаболизируется незначительно, после однократного применения до 95% принятой дозы выводится в неизмененном виде почками (28,3%) и с желчью (66,5%) [20]. Биластин также не влияет на работу изоферментов цитохрома Р450 (CYP) и не обладает значимым потенциалом лекарственных взаимодействий [23].
Биластин в дозах до 100 мг/сут не вызывает побочных эффектов со стороны сердечно-сосудистой системы, в том числе не изменяет интервал QT. Одновременный прием биластина 20 мг и кетоконазола 400 мг не усиливает изменения на электрокардиограмме [24]. Биластин является субстратом для Р-гликопротеина, который может снижать его способность проникать через гематоэнцефалический барьер и связываться с H1-рецепторами (H1-СР) в головном мозге. Биластин 20 мг не проникает через гематоэнцефалический барьер и не достигает достаточно высоких концентраций для связывания с H1-СР в головном мозге. Важно, что при сравнении с опубликованными данными о H1-СР для других АГП I и II с использованием позитронно-эмиссионной томографии биластин 20 мг демонстрирует одно из наиболее низких значений H1-СР в головном мозге (рис. 4) [25]. Доказано, что биластин не вызывает сонливости, когнитивных расстройств и снижения концентрации внимания, что обусловлено практически полным отсутствием связывания с H1-СР в головном мозге.
В отличие от большинства антагонистов Н1-рецепторов биластин не повышает депрессивное влияние лоразепама на центральную нервную систему и в противоположность другим АГП II, таким как цетиризин, не усиливает депрессивные эффекты алкоголя [26]. Кроме того, биластин не оказывает негативного влияния на способность к вождению автомобиля как после однократного приема, так и при более продолжительном лечении в дозах до 40 мг/сут [27].
Таким образом, биластин соответствует критериям классификации для безопасного неседативного АГП [28]. Биластин 20 мг характеризуется достаточной клинической эффективностью и переносимостью/безопасностью, общим благоприятным соотношением пользы и риска. В частности, препарат не оказывает кардиотоксического эффекта, не влияет на метаболические процессы с участием цитохрома Р450 (CYP), не проникает через гематоэнцефалический барьер и не достигает достаточно высоких концентраций для связывания с H1-гистаминовыми рецепторами в головном мозге. Показано ограниченное воздействие биластина на центральную нервную систему у человека: в исследованиях препарат не усиливал центральный депрессорный эффект алкоголя и лоразепама. Кроме того, однократный или многократный прием биластина 20 мг не нарушает психомоторные характеристики, которые являются важными параметрами функционирования центральной нервной системы при управлении транспортным средством.
Заключение
Своевременная диагностика и адекватное лечение сезонных проявлений аллергии с использованием современных препаратов позволяют добиваться быстрого купирования симптомов поллиноза, улучшать качество жизни пациентов, значительно уменьшать риск развития осложнений.
Современные антигистаминные препараты второго поколения являются эффективными средствами для купирования симптомов сезонной аллергии. Одним из представителей данного класса препаратов является новый оригинальный неседативный препарат Никсар® (биластин), селективно блокирующий Н1-рецепторы и характеризующийся высокой клинической эффективностью и безопасностью в облегчении симптомов аллергического (сезонного и круглогодичного) риноконъюнктивита. На основании этого препарат Никсар® (биластин) можно рекомендовать для лечения аллергического (сезонного и круглогодичного) риноконъюнктивита у взрослых и подростков с 12 лет.
Ye.P. Terekhova
Russian Medical Academy of Continuing Professional Education
Contact person: Yekaterina Petrovna Terekhova, e.p._terekhova57@mail.ru
The study is dedicated to a topical issue of clinical allergology such as diagnostics and treatment of seasonal allergy due to pollen allergens. The data on incidence rate of pollinosis as well as its classification, immunological mechanisms, clinical manifestations, contemporary diagnostics and treatment are presented. A role for modern antihistamines in treating seasonal allergy was analyzed. A mechanism of action for Nixar® (bilastine) as a novel original non-sedating long-acting high affinity to H1-receptor antihistamine is outlined. According to some studies, it was demonstrated that Nixar® (bilastine) is characterized by high efficacy in relieving symptoms of seasonal allergic rhinoconjunctivitis, well tolerated and improves quality of patients’ life.
Уважаемый посетитель uMEDp!
Уведомляем Вас о том, что здесь содержится информация, предназначенная исключительно для специалистов здравоохранения.
Если Вы не являетесь специалистом здравоохранения, администрация не несет ответственности за возможные отрицательные последствия, возникшие в результате самостоятельного использования Вами информации с портала без предварительной консультации с врачом.
Нажимая на кнопку «Войти», Вы подтверждаете, что являетесь врачом или студентом медицинского вуза.